Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
Inhibitory dekarboxylázyStalevo
Shrnutí drog
Co je Stalevo?
Stalevo (Carbidopa levodopa a entacapon) je kombinací několika léků používaných k léčbě parkinsonových symptomů, jako je křeče chroutí na tuhost svalů a špatná kontrola svalů. Levodopa se převede na chemickou látku dopamin v mozku. Příznaky Parkinsonova choroba může být způsobena dopaminem v mozku nízkým hladinami. Carbidopa pomáhá zabránit rozpadu Levodopy, než se může dostat do mozku a projevit se. Při použití s entacaponem Carbidopa a Levodopa zvyšuje hladinu levodopy v těle.
Jaké jsou vedlejší účinky Stalevo?
Stalevo
- kopřivka
- potíže s dýcháním
- Otok vašeho obličeje rty jazyk nebo krk
- nový nebo zhoršující se svalový křeč
- značně zvýšené blikání očí nebo škubání
- mdloby
- průjem
- změny vize
- rozmazané vidění
- bolest očí
- Těžká bolest břicha
- černá nebo dehtová stolička
- zvracení, které vypadá jako káva
- Slabost nebo slabost bolesti svalů
- Změna množství moči
- změny nálady
- zmatek
- halucinace
- myšlenky na sebevraždu
- trvalé bolest v krku
- Snadné krvácení nebo modřiny
- neobvyklá únava
- brnění rukou nebo nohou
- Neobvyklé silné nutkání (zvýšená sexuální nouze v hazardu)
- bolest na hrudi
- horečka
- neobvyklá ztuhlost svalu
- Těžký zmatek
- pocení
- Rychlý nebo nepravidelný srdeční rytmus
- rychlé dýchání a
- Těžká závratě
Získejte lékařskou pomoc okamžitě, pokud máte výše uvedené příznaky.
Mezi běžné vedlejší účinky Stalevo patří:
- průjem
- nevolnost
- zvracení
- bolest hlavy
- závrať
- ospalost
- rozmazané vidění
- bolest žaludku nebo rozrušení
- Ztráta chuti k jídlu
- zácpa
- sucho v ústech
- Změny ve vašem smyslu pro chuť
- vyrážka nebo svědění kůže
- neobvyklé změny kůže
- Svalové křeče
- Bolest zad
- míchání
- úzkost
- obtížnost spánku (nespavost) nebo
- zvláštní sny .
Řekněte svému lékaři, pokud máte vážné vedlejší účinky Stalevo, včetně:
- nedobrovolné pohyby (zejména škubání víčka)
- mdloby or falling
- Obtížnost polykání
- Bolest žaludku/břicha
- trvalé průjem
- změny vize (including rozmazané vidění)
- Black/Tarry stoličky
- bolest svalů
- změny množství moči
- Změny duševní/nálady (například zmatení halucinace myšlenky na sebevraždu)
- známky infekce (např. Přetrvávající bolest v krku) nebo
- Neobvyklé silné nutkání (například zvýšené hazardní hry zvýšily sexuální nutkání).
Pokud máte následující vážné vedlejší účinky, vyhledejte lékařskou péči nebo zavolejte na číslo 911:
- Vážné příznaky očí, jako je ztráta náhlého vidění rozmazané vidění vidění Vision Vision Eye Eye Eye Eye Eye Eye Eye Eye nebo vidět halos kolem světel;
- Vážné příznaky srdce, jako je rychlé nepravidelné nebo bušení srdečního rytmu; třepování v hrudi; dušnost; a náhlé závratě Lightheadedness nebo omdlet;
- Těžká zmatek bolesti hlavy zkroucený řečový rameno nebo slabost nohou Potíže se ztrátou chůze pocitu koordinace Pocit nestabilní velmi tuhé svaly vysoké horečky bohaté pocení nebo třes.
Tento dokument neobsahuje všechny možné vedlejší účinky a mohou dojít k jiným. Další informace o vedlejších účincích najdete u svého lékaře.
Dávkování pro Stalevo
Pro každého pacienta musí být stanovena optimální denní dávka Stalevo. Terapie by měla být individualizována a upravena podle požadované terapeutické odpovědi.
Jaké léky nebo doplňky interagují se Stalevo?
Stalevo může interagovat s apomorfinem cholestyraminem Dobutamin epinefrin Isoniazid isoproterenol Methyldopa Metoklopramid papaverin fenytoin probenecidní antibiotika Medikace krevních tlak Antidepresiva léky k léčbě psychiatrických poruch nachlazení nebo alergie Medicína narkotika narkotiky Plubky Spací svaly uvolňuje léky na záchvaty nebo léky proti úzkosti. Řekněte svému lékaři všechny léky, které užíváte.
Stalevo během těhotenství a kojení
Stalevo by měl být použit pouze tehdy, když je předepsán během těhotenství. Levodopa prochází do mateřského mléka. Není známo, zda Carbidopa nebo entacapon přejdou do mateřského mléka. Před kojením se poraďte se svým lékařem.
Další informace
Naše stalevo (Carbidopa levodopa a entacapon) Vedlejší účinky Drug Center poskytuje komplexní pohled na dostupné informace o možných vedlejších účincích při užívání tohoto léku.Informace o drogách FDA
- Popis léku
- Indikace
- Vedlejší účinky
- Lékové interakce
- Varování
- Předávkovat
- Klinická farmakologie
- Průvodce léky
Popis pro Stalevo
Stalevo je kombinací Carbidopa levodopy a entakaponu pro léčbu Parkinsonovy choroby.
Carbidopa Inhibitor aromatické aminokyseliny dekarboxylace je bílá krystalická sloučenina mírně rozpustná ve vodě s molekulovou hmotností 244,3. Je chemicky označen jako (-)-L- (a-hydrazino- (a-methyl-p- (34-dihydroxybenzen) kyselinu propanové monohydrát. Jeho empirickým vzorcem je C C 10 H 14 N 2 O 4 · H. 2 O a jeho strukturální vzorec je:
 |
Obsah tabletu je vyjádřen z hlediska bezvodého karbidopy, která má molekulovou hmotnost 226,3.
Levodopa Aromatická aminokyselina je bílá krystalická sloučenina mírně rozpustná ve vodě s molekulovou hmotností 197,2. Chemicky je označen jako (-)-L-a-amino-P- (34-dihydroxybenzen) kyselinu propanovou. Jeho empirický vzorec je C 9 H 11 ŽÁDNÝ 4 a jeho strukturální vzorec je:
 |
Entacapon A COMT inhibitor je nitrokatechol-strukturovaná sloučenina s molekulovou hmotností 305,3. Chemický název entakaponu je (e) -2-kyano-3- (34-dihydroxy-5-nitrofenyl) -nn-diethyl-2-propenamid. Jeho empirický vzorec je C 14 H 15 N 3 O 5 a jeho strukturální vzorec je:
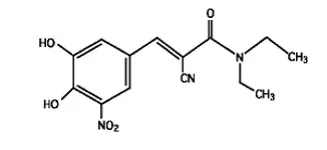 |
Stalevo je dodáván jako tablety v 6 silných stránkách:
Stalevo 50: 12,5 mg Carbidopa 50 mg levodopy a 200 mg entacaponu
Stalevo 75: 18,75 mg Carbidopa 75 mg levodopy a 200 mg entacaponu
Stalevo 100: 25 mg Carbidopa 100 mg levodopy a 200 mg entacaponu
Stalevo125: 31,25 mg Carbidopa 125 mg levodopy a 200 mg entacaponu
Stalevo 150: 37,5 mg Carbidopa 150 mg levodopy a 200 mg entacaponu
Stalevo 200: 50 mg Carbidopa 200 mg levodopy a 200 mg entacaponu
Neaktivní ingredience: Kukuřičný škrob croscarmellose sodný glycerol 85% hypromellose hořčík Stearate Mannitol Polysorbát 80 Povidon sacharóza červeného oxidu železa a oxid titaničitý. Stalevo 50 Stalevo 100 a Stalevo 150 také obsahují žlutý oxid železa.
Použití pro Stalevo
Stalevo je indikováno pro léčbu Parkinsonovy choroby.
Lze použít Stalevo:
- Nahradit (s ekvivalentními silnými stránkami každé ze tří složek) Carbidopa/Levodopa a entacapon dříve podávané jako jednotlivé produkty.
- Pro nahrazení terapie Carbidopa/Levodopa (bez entakaponu), kdy pacienti zažívají příznaky a příznaky opotřebení endové dávky a když užívají celkovou denní dávku levodopy 600 mg nebo méně a nezažili dyskinesii.
Dávkování pro Stalevo
Stalevo by se mělo používat jako náhrada za pacienty již stabilizované na ekvivalentních dávkách karbidopa/levodopy a entakaponu. Někteří pacienti, kteří byli stabilizováni v dané dávce Carbidopa/Levodopa, však mohou být léčeni Stalevo, pokud bylo rozhodnuto přidat entakapon (viz níže ). Terapie by měla být individualizována a upravena podle požadované terapeutické odpovědi.
Informace o dávkování
Optimální denní dávka Stalevo musí být stanovena pečlivou titrací u každého pacienta.
Klinické zkušenosti s denními dávkami nad 1600 mg entacaponu jsou omezené. Maximální doporučená denní dávka Stalevo závisí na použité síle. Maximální počet tablet, které mají být použity ve 24hodinovém období, je menší s nejvyšší pevností (Stalevo 200) než s nižšími pevnými stránkami (viz tabulka 1). Studie ukazují, že periferní dopa dekarboxyláza je nasycena karbidopa při přibližně 70 mg denně až 100 mg denně. Pacienti, kteří dostávají méně než toto množství karbidopy, častěji zažívají nevolnost a zvracení.
Tabulka 1: Maximální doporučená dávka Stalevo za 24 hodin
| Síla dávkování stalevo | Maximální počet tablet za 24 hodin |
| Stalevo 50 Stalevo 75 Stalevo 100 Stalevo 125 Stalevo 150 | 8 |
| Stalevo 200 | 6 |
Převod pacientů z Carbidopa levodopy a entakaponu na Stalevo
Pacienti, kteří jsou v současné době léčeni entacaponem 200 mg s každou dávkou nezveřejněného uvolňování tabletu Carbidopa/Levodopa, se mohou přepnout na odpovídající sílu Stalevo obsahujícího stejné množství levodopy a karbidopy. Například pacienti, kteří dostávají jeden tablet karbidopy/levodopy 25 mg/100 mg a jeden tablet entacaponu 200 mg v každé podávání, mohou přepnout na jeden stalevo 100 tabletu (obsahující 25 mg Carbidopa 100 mg levodopy a 200 mg entacaponu).
Převod pacientů z produktů Carbidopa a Levodopa na Stalevo
Neexistuje žádná zkušenost s převodem pacientů, kteří jsou v současné době léčeni formulacemi s prodlouženým uvolňováním produktů Carbidopa/Levodopa nebo Carbidopa/Levodopa, které nejsou kombinovány v poměru 1: 4 karbidopy k levodopě.
Pacienti s anamnézou mírných nebo závažných dyskineze nebo užívání více než 600 mg složky levodopy denně budou pravděpodobně vyžadovat snížení jejich denní dávky levodopy při přidání entakaponu. Protože nastavení dávky jednotlivé složky Carbidopa nebo Levodopa není možné, u produktů s pevnou dávkou zpočátku titrují pacienty na dávku, která je tolerována a která splňuje jejich individuální terapeutickou potřebu pomocí samostatného tabletu Carbidopa/Levodopa (poměr 1: 4) plus entakaponovou tabletu. Jakmile byla stanovena individuální dávka pacienta karbidopy/levodopy plus entakaponová dávka pomocí dvou samostatných tablet; Přepněte pacienta na odpovídající jediný tablet Stalevo.
Pokud je vyžadováno méně levodopy, snižujte celkovou denní dávku karbidopy/levodopy buď snížením pevnosti Stalevo v každé podání nebo snížením frekvence podávání prodloužením času mezi dávkami.
Současné užívání s jinými léky proti Parkinsonově chorobě
Anticholinergní činidla dopamin Agonisté monoamin oxidáza (MAO) - B inhibitory B amantadin a další standardní léky pro Parkinsonovu chorobu mohou být použity současně, zatímco Stalevo se podává; Může však být vyžadováno úpravy dávkování doprovodných léků nebo Stalevo.
Snížení nebo přerušení dávkování
Vyhněte se přerušení dávkování stalevo, protože hyperpyrexie byla hlášena u pacientů, kteří náhle přerušili nebo snižovali jejich používání levodopy [viz Varování a preventivní opatření ].
Důležité pokyny pro správu
Nerozdělujte tablety Stalevo Crush ani žvýkat. Spravujte pouze jeden tablet v každém intervalu dávkování. Všechny silné stránky Stalevo obsahují 200 mg entacaponu. Kombinace více tablet nebo částí tablet k dosažení vyšší dávky levodopy může vést k předávkování entakaponem.
Spravujte Stalevo s jídlem nebo bez něj. Stravování s vysokým obsahem tuku však může zpozdit absorpci levodopy asi o 2 hodiny [viz Klinická farmakologie ].
Jak dodáno
Formy a silné stránky dávkování
Každá stalevo tableta poskytovaná v 6 pevných stránkách s jednou dávkou obsahuje Carbidopa a Levodopa v poměru 1: 4 a dávku entakaponu 200 mg. Stalevo (Carbidopa levodopa a entacapon) se dodává jako tablety potažené filmem pro perorální podání v následujících 6 silných stránkách:
Stalevo 50 Filmové tablety obsahující 12,5 mg karbidopy 50 mg levodopy a 200 mg entacaponu. Kulaté bi-konvexní tablety jsou nahnědlé nebo šedé červené a vyražené LCE 50 na jedné straně.
Stalevo 75 Filmové tablety obsahující 18,75 mg karbidopy 75 mg levodopy a 200 mg entacaponu. Oválné tablety jsou světle nahnědlé červené netvoření a vyraženy s kódem LCE 75 na jedné straně.
Stalevo 100 Tablety potažené filmem obsahující 25 mg Carbidopa 100 mg levodopy a 200 mg entacaponu. Oválné tablety jsou nahnědlé nebo šedé červené a vyraženy LCE 100 na jedné straně.
Stalevo 125 Tablety potažené filmem obsahující 31,25 mg Carbidopa 125 mg levodopy a 200 mg entacaponu. Tablety ve tvaru oválu jsou světle nahnědlé červené netvoření a vyraženy s kódem LCE 125 na jedné straně.
Stalevo 150 Tablety potažené filmem obsahující 37,5 mg Carbidopa 150 mg levodopy a 200 mg entacaponu. Tablety ve tvaru prodlouženého elipsy jsou nahnědlé nebo šedé červené a vyražené LCE 150 na jedné straně.
Stalevo 200 Filmové tablety obsahující 50 mg karbidopy 200 mg levodopy a 200 mg entacaponu. Tablety ve tvaru oválu jsou tmavě nahnědlé červené netrámené a vyraženy LCE 200 na jedné straně.
Skladování a manipulace
Stalevo (Carbidopa levodopa a entacapon) jsou dodávány jako tablety potažené filmem pro ústní podávání v následujících šesti silných stránkách:
Stalevo 50 film-coated tablets obsahující 12,5 mg karbidopy 50 mg levodopy a 200 mg entacaponu.
Kulaté bi-konvexní tablety jsou nahnědlé nebo šedé červené a vyražené LCE 50 na jedné straně.
HDPE láhev 100 tablet NDC 52427-805-01
Stalevo 75 film-coated tablets obsahující 18,75 mg karbidopy 75 mg levodopy a 200 mg entacaponu.
Tablety ve tvaru oválu jsou světle nahnědlé červené netvoření a vyraženy s kódem LCE 75 na jedné straně.
HDPE láhev 100 tablet NDC 52427-809-01
Stalevo 100 film-coated tablets obsahující 25 mg karbidopy 100 mg levodopy a 200 mg entacaponu.
Tablety ve tvaru oválu jsou nahnědlé nebo šedé červené a vyražené LCE 100 na jedné straně.
HDPE láhev 100 tablet NDC 52427-816-01
Stalevo 125 film-coated tablets obsahující 31,25 mg Carbidopa 125 mg levodopy a 200 mg entacaponu.
Tablety ve tvaru oválu jsou světle nahnědlé červené netvoření a vyraženy s kódem LCE 125 na jedné straně.
HDPE láhev 100 tablet NDC 52427-827-01
Stalevo 150 film-coated tablets obsahující 37,5 mg Carbidopa 150 mg levodopy a 200 mg entacaponu.
Tablety ve tvaru prodlouženého elipsy jsou nahnědlé nebo šedé červené a vyražené LCE 150 na jedné straně.
HDPE láhev 100 tablet NDC 52427-834-01
Stalevo 200 film-coated tablets obsahující 50 mg karbidopy 200 mg levodopy a 200 mg entacaponu.
Tablety ve tvaru oválu jsou tmavě nahnědlé červené netrámené a vyraženy LCE 200 na jedné straně.
HDPE láhev 100 tablet NDC 52427-842-01
Skladovat při 25 ° C (77 ° F); Výlety jsou povoleny na 15 ° C až 30 ° C (59 ° F až 86 ° F).
[Vidět Teplota místnosti s kontrolou USP .]
Vydejte se v těsném kontejneru (USP).
Vyrobeno: Orion Corporation Orion Pharma Orionintie 1 FI-02200 ESPOO Finsko. Distribuováno: Almatica Pharma LLC Morristown NJ 07960 USA. Revidováno: květen 2020
Vedlejší účinky for Stalevo
Následující nežádoucí účinky jsou podrobněji diskutovány ve varováních a preventivních úsecích označování:
- Usínání během činností každodenního života a somnolence [viz Varování a preventivní opatření ]
- Hypotenze /Ortostatická hypotenze a synkopa [viz Varování a preventivní opatření ]
- Dyskinesie [viz Varování a preventivní opatření ]
- Deprese a sebevražda [viz Varování a preventivní opatření ]
- Halucinace/Psychotické chování [viz Varování a preventivní opatření ]
- Kontrola impulsů a/nebo nutkavé chování [Viz Varování a preventivní opatření ]
- Hyperpyrexie a zmatek vznikající Varování a preventivní opatření ]
- Průjem a kolitida [viz Varování a preventivní opatření ]
- Rhabdomyolýza [viz Varování a preventivní opatření ]
- Peptické onemocnění vředů [viz Varování a preventivní opatření ]
Zkušenosti z klinických studií
Vzhledem k tomu, že klinické studie jsou prováděny za velmi proměnlivých podmínek, výskyt nežádoucích účinků (počet jedinečných pacientů, kteří mají nepříznivou reakci spojenou s léčbou/celkovým počtem léčených pacientů) pozorovanými v klinických studiích léčiva, nelze přímo porovnat s výskytem nepříznivých reakcí v klinických studiích s jiným lékem a nemusí odrážet incidence inverzích pozorovaných v klinické praxi.
Entacapon
Nejčastěji pozorované nežádoucí účinky (incidence nejméně o 3% větší než výskyt placeba) v dvojitě slepé karbidopa-levododopa-placebo kontrolní studie entakaponu (n = 1003 pacientů) spojené s používáním karbidopalevodopa- entacapone samotného a nepatřilo se k ekvivalentní frekvenci platetorovaného pacienta: dysinea na nanuea, naiseea hyperheea, napakované na nauseea hypertikovou a nepatřilo se k ekvivalentní frekvenci. Bolest břicha zvrací sucho v ústech a zbarvení moči.
Výskyt rozdílu léčby pro předčasné přerušení studie pro entacapon s inhibitorem levodopy a dopa dekarboxylázy v dvojitě zaslepených placebem kontrolovaných studiích byl 5%. Výskyt rozdílu léčby pro nejčastější příčiny přerušení studie byl 2% u průjmu a 1% pro další specifické nežádoucí účinky včetně psychiatrických důvodů dyskineze/ hyperkinezie nevolnost nebo břišní bolesti.
Výskyt nežádoucí reakce v kontrolovaných klinických studiích entacaponu
Tabulka 2 uvádí léčbu vznikající nežádoucí účinky, ke kterým došlo u alespoň 1% pacientů léčených Carbidopa/Levodopa a 200 mg entacaponu, kteří se účastnili dvojitě zaslepených placebem kontrolovaných studií a které byly v této skupině numericky častější než ve skupině Carbidopa/Levodopa plus placebo. V těchto studiích byl do Carbidopa/Levodopa (nebo benserazid/levodopa) přidán entakapon nebo placebo.
Tabulka 2: Shrnutí pacientů s nežádoucími účinky po zahájení podávání zkušebního léčiva nejméně 1% ve skupině entacaponu a větší než placebo
| Nežádoucí reakce třídy systémových orgánů | Carbidopa/Levodopa plus entacapon (n = 603) % pacientů | Carbidopa/Levodopa plus placebo (n = 400) % pacientů |
| Poruchy kůže a připojení | ||
| Pocení se zvýšilo | 2 | 1 |
| Poruchy muskuloskeletálního systému | ||
| Bolest zad | 5 | 3 |
| Poruchy centrálního a periferního nervového systému | ||
| Dyskinesie | 25 | 15 |
| Hyperkinesie | 10 | 5 |
| Hypokineze | 9 | 8 |
| Závrať | 8 | 6 |
| Speciální smysly další poruchy | ||
| Ochutnejte zvrácenost | 1 | 0 |
| Psychiatrické poruchy | ||
| Úzkost | 2 | 1 |
| Spavost | 2 | 0 |
| Míchání | 1 | 0 |
| Poruchy gastrointestinálního systému | ||
| Nevolnost | 14 | 8 |
| Průjem | 10 | 4 |
| Bolest břicha | 8 | 4 |
| Zácpa | 6 | 4 |
| Zvracení | 4 | 1 |
| Ústa suchá | 3 | 0 |
| Dyspepsia | 2 | 1 |
| Nadýmání | 2 | 0 |
| Zánět žaludku | 1 | 0 |
| Gastrointestinální poruchy č | 1 | 0 |
| Poruchy dýchacího systému | ||
| Dušnost | 3 | 1 |
| Krvácení a srážení destiček Poruchy | ||
| Purpura | 2 | 1 |
| Poruchy močového systému | ||
| Zbarvení moči | 10 | 0 |
| Tělo jako celo generální poruchy | ||
| Únava | 6 | 4 |
| Astenia | 2 | 1 |
| Poruchy mechanismu odporu | ||
| Infekce bakteriální | 1 | 0 |
Zážitek z postmarketingu
Od zavedení trhu byly identifikovány následující spontánní zprávy o nepříznivých událostech dočasně spojených s entacaponem nebo Stalevoem a nejsou uvedeny v tabulce 2. Protože tyto reakce jsou uváděny dobrovolně z populace neznámé velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo provést příčinný vztah k entakaponu nebo stalevoru.
Byla hlášena hepatitida s hlavně cholestatickými rysy.
Účinky pohlaví a věku na nežádoucí účinky
Nebyly zaznamenány žádné rozdíly v míře nežádoucích účinků, které lze přičíst samotnému entakaponu podle věku nebo pohlaví.
Lékové interakce for Stalevo
Mao inhibitory
Pacienti, kteří dostávají neselektivní inhibitory MAO a levodopa a entakapon Carbidopa, mohou být ohroženi zvýšeným adrenergním tónem. Proto je použití Stalevo kontraindikováno u pacientů, kteří dostávají neselektivní inhibitory MAO [viz Kontraindikace ].
Léky metabolizované katechol-o-methyltransferázou (COMT)
Drugs known to be metabolized by COMT such as isoproterenol epinephrine norepinephrine dopamine dobutamine alpha-methyldopa apomorphine isoetherine and bitolterol should be administered with caution in patients receiving entacapone regardless of the route of administration (including inhalation) as their interaction may result in increased heart rates possibly arrhythmias and excessive changes in blood pressure [Viz Varování a preventivní opatření ].
Antihypertenzivní agenti
Symptomatický Posturální hypotenze došlo k tomu, že k léčbě pacientů dostávajících antihypertenzivní léčiva byla přidána Carbidopa/Levodopa. Při zahájení terapie stalevovým nastavením dávkování antihypertenziva léčiva může být vyžadováno.
Tricyklická antidepresiva
Zprávy o nežádoucích účincích včetně hypertenze a dyskineze vyplývající z souběžného použití tricyklického antidepresiva a Carbidopa/Levodopa.
Antagonisté receptoru dopaminu D2
Antagonisty receptoru dopaminu D2 (např. Metoklopramidové fenothiaziny butyrofenony risperidon) mohou snížit terapeutické účinky levodopy.
Isoniazid
Isoniazid may reduce the therapeutic effects of levodopa a dose increase may be necessary.
Phable
Příznivé účinky levodopy na Parkinsonovu chorobu byly hlášeny, že se zvrátí fenytoinem. Pacienti užívající fenytoin s Carbidopa/Levodopa by měli být pečlivě pozorováni pro ztrátu terapeutické odpovědi. U pacientů, kteří dostávají fenytoin, by mělo být zvýšeno dávkování stalevo.
Papaverine
Příznivé účinky levodopy na Parkinsonovu chorobu byly hlášeny, že se zvrátí Papaverine. Pacienti užívající papaverin s Carbidopa/Levodopa by měli být pečlivě pozorováni pro ztrátu terapeutické odpovědi. U pacientů, kteří dostávají papaverin, by se mělo zvýšit dávkování stalevo.
Železné soli
Železové soli nebo multi vitamíny obsahující železné soli by měly být podávány opatrně. Železné soli mohou tvořit cheláty s levodopou karbidopu a entakaponem a následně snižovat biologickou dostupnost levodopské karbidopy a entakaponu.
Léky, o nichž je známo, že narušují biliární vylučování glukuronidace a střevní beta-glukuronidáza
Protože většina vylučování entakaponu je přes dokonce Upozornění by mělo být provedeno, pokud je známo, že léky narušují biliární vylučování glukuronidace a střevní beta-glukuronidázou souběžně s entacaponem. Mezi ně patří probenecidový cholestyramin a některá antibiotika (např. Erytromycin rifampicin ampicilin a chloramfenikol).
Léky metabolizované přes CYP2C9 (např. Coumadin)
Dávka Stalevo by měla být upravena jako klinicky potřebná u pacientů s použitím jiných léčiv metabolizovaných prostřednictvím CYP2C9. Studie interakce u zdravých dobrovolníků entacaponu zvýšila AUC R-warfarinu v průměru o 18% a hodnoty INR v průměru o 13%. Případy zvýšeného INR u pacientů souběžně byly hlášeny během použití entacaponu po schválení. Monitorování INR se tedy doporučuje, když je zahájena stalevo léčba u pacientů, kteří dostávají warfarin.
Varování pro Stalevo
Zahrnuto jako součást OPATŘENÍ sekce.
Opatření pro Stalevo
Následující nežádoucí účinky popsané v této části se týkají alespoň jedné ze složek Stalevo (tj. Levodopa karbidopa a/nebo entakaponu) na základě bezpečnostních zkušeností v klinických studiích (zejména klíčových pokusech) nebo v ponorkových zprávách.
Usínání během činností každodenního života a somnolence
Pacienti s Parkinsonovou chorobou léčených Stalevo nebo jinými produkty Carbidopa/Levodopa hlásili, že náhle usínají bez předchozího varování před ospalostí, zatímco se zabývají činnostmi každodenního života (včetně provozu motorových vozidel). Některé z těchto epizod vyústily v nehody. Ačkoli mnoho z těchto pacientů hlásilo somnolence při užívání entacaponu, někteří nevnímali varovné signály, jako je nadměrná ospalost, a věřili, že byli upozorněni bezprostředně před událostí. Některé z těchto událostí bylo hlášeno až jeden rok po zahájení léčby.
Spavost was reported in 2% of patients taking entacapone a 0% in placebo in controlled trials. It is reported that falling asleep while engaged in activities of daily living always occurs in a setting of pre-existing somnolence although patients may not give such a history. For this reason prescribers should reassess patients for ospalost or sleepiness especially since some of the events occur well after the start of treatment. Prescribers should also be aware that patients may not acknowledge ospalost or sleepiness until directly questioned about ospalost or sleepiness during specific activities. Patients who have already experienced somnolence a/or an episode of sudden sleep onset should not participate in these activities during treatment with Stalevo.
Před zahájením léčby Stalevo radí pacientům o potenciálu rozvíjet ospalost a konkrétně se zeptat na faktory, které mohou zvýšit toto riziko, jako je použití souběžných uklidňujících léků a přítomnost poruch spánku. Pokud se pacient rozvíjí denní ospalost nebo epizody usínání během činností, které vyžadují aktivní účast (např. Konverzace konzumace atd.), Měl by být Stalevo obvykle ukončen [viz viz Dávkování a podávání a Varování a preventivní opatření ]. If the decision is made to continue Stalevo patients should be advised not to drive a to avoid other potentially dangerous activities. There is insufficient information to establish whether dose reduction will eliminate episodes of falling asleep while engaged in activities of daily living.
Hypotenze Orthostatic Hypotenze And Syncope
Zprávy o synkopě byly obecně častější u pacientů v obou léčebných skupinách, kteří měli předchozí epizodu zdokumentované hypotenze (ačkoli epizody synkopy získané historií nebyly samy o sobě dokumentovány vitálním měřením znaků). Hypotenze ortostatická hypotenze a synkopa jsou pozorovány u pacientů léčených léky, které zvyšují centrální dopaminergní tón včetně Stalevo.
Dyskinesie
Dyskinesie (nedobrovolné movements) may occur or be exacerbated at lower dosages a sooner with Stalevo than with preparations containing only carbidopa a levodopa. The occurrence of dyskinesias may require dosage reduction.
V klíčových studiích byl výskyt rozdílu léčby dyskineze 10% a pro Carbidopa-Levodopa plus 200 mg entakaponu. Přestože snižování dávky levodopy může tento vedlejší účinek zlepšit, mnoho pacientů v kontrolovaných studiích pokračovalo v častých dyskinezích navzdory snížení jejich dávky levodopy. Výskyt rozdílu léčby při výběru studie pro dyskinezi byl 1% pro carbidopa-levodopa-etacapon.
Deprese a sebevražda
Všichni pacienti by měli být pečlivě pozorováni pro rozvoj deprese se souběžnými sebevražednými tendencemi. Pacienti s minulými nebo současnými psychónami by měli být léčeni opatrností.
Halucinace a/nebo psychotické chování
Dopaminergní terapie u pacientů s Parkinsonovou chorobou byla spojena s halucinacemi. Halucinace vedly k přerušení léčiva a předčasnému stažení z klinických studií u 0,8% a 0% pacientů léčených entakaponem levodopy Carbidopa a Carbidopa Levodopa. Halucinace vedly k hospitalizaci u 1,0% a 0,3% pacientů ve skupinách entacaponu levodopy karbidopy a levodopy Carbidopa. Agitace se vyskytla u 1% pacientů léčených entacaponem karbidopy levodopa a 0% léčených levodopou Carbidopa.
Kontrola impulsů a/nebo nutkavé chování
Zprávy o postmarketingu naznačují, že pacienti léčeni anti-parkinsonovým léky mohou zažít intenzivní nouze k hazardu se zvýšené sexuální nutkání intenzivní nutkání nekontrolovatelně utratit peníze a další intenzivní nutkání. Pacienti nemusí být schopni kontrolovat tyto nutkání při užívání jedné nebo více léků, které se obecně používají k léčbě Parkinsonovy choroby a které zvyšují centrální dopaminergní tón, včetně entacaponu užívané s levodopou a karbidopou. V některých případech, i když ne všechna tato nouzová nouze byla hlášena, že se zastavila, když byla dávka anti-parkinsonových léků snížena nebo přerušena. Protože pacienti nemusí tyto chování rozpoznat jako neobvyklé, je důležité, aby se předepisující lékaři konkrétně zeptali pacientů nebo jejich pečovatelů o vývoji nových nebo zvýšených hazardních nouze sexuálních nutkání nekontrolovaných výdajů nebo jiných nutkání při léčbě entakaponem. Lékaři by měli zvážit redukci dávky nebo zastavit Stalevo, pokud se pacient vyvine takové nutkání při užívání Stalevo [viz Dávkování a podávání Varování a preventivní opatření ].
ATHERACE-Engergent Hyperpyrexia a zmatek
Případy hyperpyrexie a zmatku připomínající neuroleptický maligní syndrom (NMS) byly hlášeny ve spojení se snižováním dávky nebo stažení terapie levodopou a entakaponem Carbidopa. V některých případech však byly hlášeny hyperpyrexie a zmatek po zahájení léčby entakaponem. Hyperpyrexie a zmatek jsou neobvyklé, ale mohou být život ohrožující s různými rysy, včetně hyperpyrexie/horečky/hypertermické rigidity Nedobrovolné pohyby Změněné vědomí/duševní stav změny delirium Autonomická dysfunkce Tachykardie TACHYPNEEA Hyper- nebo Hypotension Laboratory (E.G. Fuzonní fosfonóza, stvořiná fosfonóza, stvořitelná fosfokin. myoglobinurie a zvýšený sérový myoglobin).
Pokud pacient potřebuje přerušit nebo snížit svou denní dávku Stalevo, dávka by měla být pomalu snižována s dohledem poskytovatele zdravotní péče [viz viz Dávkování a podávání ]. Specific methods for tapering entacapone have not been systematically evaluated.
Průjem And Colitis
V klinických studiích průjmu entakaponu se vyvinula u 60 z 603 (NULL,0%) a 16 ze 400 (NULL,0%) pacientů léčených 200 mg entacaponu nebo placeba v kombinaci s inhibitorem levodopy a dopa dekarboxylázy. U pacientů léčených průjmem entakaponu byl obecně mírný až střední závažnost (NULL,6%), ale byl považován za závažný v 1,3%. Průjem mělo za následek stažení u 10 z 603 (NULL,7%) pacientů 7 (NULL,2%) s mírným a středním průjmem a 3 (NULL,5%) s těžkým průjmem. Průjem se obecně vyřešil po přerušení entacaponu. Dva pacienti s průjmem byli hospitalizováni. Průjem se obvykle představuje do 4 až 12 týdnů po spuštění entacaponu, ale může se objevit již v prvním týdnu a již mnoho měsíců po zahájení léčby. Průjem může být spojen s dehydratací hubnutí a hypokalémií.
Postmarketingové zkušenosti ukázaly, že průjem může být známkou mikroskopické kolitidy vyvolané léčivem primárně lymfocytární kolitidou. V těchto případech byl průjem obvykle mírný až těžký vodnaté a nebloody občas spojený s úbytkem hmotnosti a hypokalémií břicha břicha břicha. Ve většině případů průjem a další symptomy související s kolitidou se při zastavení léčby entakaponem vyřešily nebo se výrazně zlepšily. U některých pacientů s biopsií potvrdila, že průjem kolitidy se po ukončení entacaponu vyřešil nebo významně se zlepšil, ale po retrénování entacaponem se opakoval.
Pokud je podezření na prodloužený průjem, který souvisí se Stalevo, by se měla lék přerušit a zvažována vhodná lékařská terapie. Pokud příčina prodlouženého průjmu zůstává nejasná nebo pokračuje po zastavení entakaponu, je třeba zvážit další diagnostické vyšetřování včetně kolonoskopie a biopsií.
Rhabdomyolýza
Případy těžké rabdomyolýzy byly hlášeny s entakaponem, pokud jsou použity v kombinaci s karbidopa a levodopou. Těžká prodloužená motorická aktivita včetně dyskineze může pravděpodobně odpovídat za rabdomyolýzu. Většina případů se projevila myalgií a zvýšené hodnoty kreatin fosfokinázy (CPK) a myoglobinu. Některé reakce také zahrnovaly horečku a/nebo změnu vědomí. Je také možné, že rhabdomyolýza může být výsledkem syndromu popsaného v hyperpyrexii a zmatku z hlediska abstinentně-engorges [viz viz Varování a preventivní opatření ].
Interakce s léky metabolizovanými společností COMT
Léky, o nichž je známo, že jsou metabolizovány COMT, jako je isoproterenol epinefrin norepinefrin dopamin dobutamin alfa-methyldopa apomorfin isoetherin a bitolterol, by měl být podáván s opatrností u pacientů, kteří dostávají entakapon bez ohledu na způsob podávání, a to, že jejich interakce by měla být zvýšená a/nebo nebo byla zvýšená krevní tlak a/nebo/nebo se zvyšoval arhthatia.
Fibrotické komplikace
Případy retroperitoneální fibrózy plicní infiltráty pleurálního výtoku a pleurálního zahušťování byly u některých pacientů léčeny dopaminergní látky odvozenými z ergotu. Tyto komplikace se mohou vyřešit, když je léčivo přerušeno, ale úplné rozlišení se vždy nevyskytuje. Ačkoli tyto nežádoucí účinky mohou souviset s ergolinovou strukturou těchto sloučenin, je také zvažována možná kauzální role léčiv odvozených od negotu (např. Entacapon levodopa), která zvyšuje dopaminergní aktivitu. Očekávaný výskyt fibrotických komplikací je tak nízký, že i kdyby entakapon způsobil tyto komplikace podobné míře podobné těm, které lze připsat jiným dopaminergním terapiím, je nepravděpodobné, že by byl detekován v kohortě velikosti vystavené entacaponu během jeho klinického vývoje. Během klinického vývoje entakaponu byly hlášeny čtyři případy plicní fibrózy; 3 z těchto pacientů byly také léčeny pergolidem a 1 bromokriptinem. Doba léčby entakaponem se pohybovala od 7 měsíců do 17 měsíců.
Peptické onemocnění vředů
Stejně jako u léčby levodopy Stalevo může zvýšit možnost horního gastrointestinálního krvácení u pacientů s anamnézou peptického vředu.
Poškození jater
Pacienti s poškozením jater by měli být léčeni opatrností [viz Klinická farmakologie ]. As with levodopa periodic evaluation of hepatic function is recommended during extended therapy.
Laboratorní testy
Abnormality v laboratorních testech mohou zahrnovat zvýšení testů jaterních funkcí, jako je alkalická fosfatáza Sgot (AST) SGPT (ALT) laktická dehydrogenáza a bilirubin. Abnormality v krvi močovina Byly také hlášeny test dusíku a pozitivních coombů. Během podávání Stalevo jsou běžné hladiny kreagenu a kyseliny močoviny v krvi kreagenu a kyseliny močové než u levodopy.
Stalevo may cause a false-positive reaction for urinary ketone bodies when a test tape is used for determination of ketonuria . This reaction will not be altered by boiling the urine specimen. False-negative tests may result with the use of glucose-oxidase methods of testing for glucosuria. Cases of falsely diagnosed pheochromocytoma in patients on carbidopa/levodopa therapy have been reported very rarely.
Při interpretaci hladiny katecholaminů a jejich metabolitů u pacientů na terapii Carbidopa/Levodopa by měla být opatrná opatrnost.
Informace o poradenství pro pacienta
Usínání během činností každodenního života a somnolence
Poraďte pacientům o možném sedaci účinků spojených se Stalevo, včetně somnolence a možnosti usínání při zachování činností každodenního života. Protože somnolence může být častým nežádoucím reakcí s potenciálně závažnými důsledky, že pacienti by neměli řídit motorové vozidlo provozovat těžké stroje nebo se zapojit do jiných potenciálně nebezpečných činností, dokud nezískají dostatečné zkušenosti se Stalevo, aby určili, zda to ovlivňuje jejich mentální a/nebo motorový výkon nepříznivě [viz viz [Viz [Viz [Viz [Viz Varování a preventivní opatření ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Před podáním léků na sedaci alkoholu nebo jiných depresiv CNS (např. Benzodiazepiny antipsychotics antidepresiva atd.) Z důvodu možných aditivních účinků v kombinaci se stalevo radí pacientům, aby hovořili se svým předepisovaným zdravotním předpiserem nebo jinými depresivy CNS (např. Benzodiazepiny antipsychotiky atd.).
Hypotenze Orthostatic Hypotenze And Syncope
Doporučují pacientům, že se mohou vyvinout symptomatická (nebo asymptomatická) posturální (ortostatická) hypotenze nebo netorostatickou hypotenzi při užívání stalevo. Hypotenze/ortostatická hypotenze se může během počáteční terapie častěji vyskytovat častěji. Po sezení nebo ležení by se pacienti neměli rychle zvyšovat, zejména pokud tak učinili po delší dobu a zejména při zahájení léčby Stalevo.
Poraďte pacientům o potenciálu synkopy u pacientů pomocí agonistů dopaminu. Z tohoto důvodu informujte pacienty o možnosti synkopy při užívání Stalevo [viz Varování a preventivní opatření ].
Dyskinesies
Informujte pacienty, že Stalevo může způsobit a/nebo prohloubit již existující dyskinesii [viz Varování a preventivní opatření ].
Halucinace a/nebo psychotické chování
Informujte pacienty, že při užívání Stalevo může dojít k halucinacím a dalším psychotickému chování [viz Varování a preventivní opatření ].
Kontrola impulsů a/nebo nutkavé chování
Poraďte pacientům, že mohou zažít kontrolu impulsu a/nebo nutkavé chování při užívání jednoho nebo více léků používaných k léčbě Parkinsonovy choroby včetně Stalevo. Zeptejte se pacientů na vývoj nových nebo zvýšených hazardních nutkání sexuálních nutkání o naléhavé nouze o nekontrolované výdaje nebo jiné intenzivní nutkání při léčbě Stalevo. Doporučují pacientům, aby informovali svého lékaře nebo poskytovatele zdravotní péče, pokud zažívají nové nebo zvýšené nouze v hazardních hrách, zvýšená sexuální nutkání nebo jiné intenzivní nutkání při bití Stalevo. Lékaři by měli zvážit redukci dávky nebo zastavit léky, pokud se pacient vyvine takové nutkání při užívání Stalevo [viz Varování a preventivní opatření ].
ATHERACE-Engergent Hyperpyrexia a zmatek
Doporučují pacientům, že mohou vyvinout horečku a zmatek jako součást syndromu připomínajícího NM a pravděpodobně s jinými klinickými rysy (např. Svalová rigidita autonomní hyper- nebo hypotenze atd.). K tomuto syndromu horečky a zmatení se může objevit zejména se snížením dávky nebo stažení Stalevo, ale může se také vyvinout po zahájení léčby. Doporučujte pacientům, aby kontaktovali svého poskytovatele zdravotní péče, pokud si přejí přerušit nebo snížit dávku Stalevo a kontaktovat poskytovatele zdravotní péče, pokud vyvinou horečku a zmatek [viz viz Varování a preventivní opatření ].
Průjem And Colitis
Informujte pacienty, že průjem se může vyskytnout u Stalevo a může mít zpožděný nástup. Někdy může být prodloužený průjem způsoben kolitidou (zánět tlustého střeva). Pacienti s průjmem by měli pít tekutiny, aby udrželi přiměřenou hydrataci a sledovali úbytek hmotnosti. Pokud je průjem spojený se stalevo prodloužený, očekává se, že lék povede k rozlišení. Pokud průjem pokračuje po zastavení Stalevo, může být zapotřebí další diagnostická vyšetřování. V některých případech může být průjem s kolitidou [viz viz Varování a preventivní opatření ].
Rhabdomyolýza
Poraďte pacientům, že se mohou vyvinout rabdomyolýza a myalgii, pokud zažijí prodlouženou motorickou aktivitu včetně dyskineze. Tato událost může být také spojena s horečkou a zmatkem [viz Varování a preventivní opatření ].
Nevolnost And Zvracení
Informujte pacienty, že stalevo může způsobit nevolnost a zvracení se může objevit častěji během počáteční terapie a může vyžadovat nastavení dávky.
Pokyny pro použití
Poskytněte pacientům, aby užívali Stalevo pouze podle předepsaného. Poskytněte pacientům, aby v každém intervalu dávkování užívali pouze jeden tablet Stalevo. Poskytněte pacientům, aby nebrali více tablet nebo dalších částí tablet k dosažení vyšší dávky levodopy. Doporučujte pacientům, aby nerozdělili nebo žvýkali Stalevo.
Informujte pacienta, že Stalevo je formulace karbidopy/levodopy kombinovaných s entacaponem, který je navržen tak, aby zahájil uvolňování přísad do 30 minut po požití. Je důležité, aby byl Stalevo přijato v pravidelných intervalech podle harmonogramu nastíněného lékařem. Upozorněte pacienta, aby nezměnil předepsaný dávkový režim a nepřidal žádné další antiparkinsonovské léky, včetně jiných přípravků Carbidopa/Levodopa, aniž by se nejprve konzultoval lékaře.
Doporučujte pacientům, že na konci dávkovacího intervalu se mohou vyskytnout epizody (opotřebení léčivého efektu), ale může dojít k nepředvídatelnému z epizod. Doporučujte pacientovi, aby informoval poskytovatele zdravotní péče o možnou úpravu léčby, pokud taková odpověď představuje problém pro každodenní život pacienta.
Poraďte pacientům, že tmavé zbarvení (červené hnědé nebo černé) se může po užití Stalevo objevit v moči slin nebo potu. Ačkoli se zdá, že barva je klinicky nevýznamné oděvy, mohou být zbarveny.
Doporučujte pacientům, že změna stravy na potraviny s vysokým obsahem bílkovin může zpozdit absorpci levodopy. Nadměrná kyselost také zpožďuje vyprazdňování žaludku, čímž zpožďuje absorpci levodopy. Železové soli (například v multi-vitaminových tabletách) mohou také snížit účinnost Stalevo.
Těhotenství
Poskytněte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud otěhotní nebo mají v úmyslu otěhotnět během terapie [viz Použití v konkrétních populacích ].
Laktace
Poskytněte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud mají v úmyslu kojit nebo kojí kojence [viz viz Použití v konkrétních populacích ].
Neklinická toxikologie
Zhodnocení mutageneze karcinogeneze plodnosti
Karcinogeneze
U potkanů ústní podávání karbidopa-levodopa po dobu 2 let nevedlo k žádnému důkazu karcinogenity v dávkách přibližně 2krát (karbidopa) -4krát (levodopa) maximální doporučenou lidskou dávku (MRHD).
U myší a potkanů byly provedeny dvouleté studie karcinogenity entakaponu. U myší nebylo pozorováno zvýšení nádorů při perorálních dávkách 100 200 a 400 mg/kg/den. Při nejvyšší dávce testované expozice plazmy (AUC) byly 4krát vyšší než u lidí při maximální doporučené denní dávce (MRDD) 1600 mg. U potkanů podávaných perorálních dávek 20 90 nebo 400 mg/kg/den byla u mužů při nejvyšší testované dávce pozorována zvýšený výskyt renálních tubulárních adenomů a karcinomů. Plazmatické AUC při vyšší dávce, které nejsou spojeny se zvýšenými nádory ledvin (90 mg/kg/den), byly přibližně 5krát vyšší než u lidí na MRDD entacaponu.
Karcinogenní potenciál entakaponu podávaný v kombinaci s karbidopa-levodopa nebyl vyhodnocen.
Mutageneze
Carbidopa byla mutagenní v testu in vitro bakteriální reverzní mutace (AMES) v přítomnosti a nepřítomnosti metabolické aktivace a v testu in vitro myší lymfom thymidin kinázy (TK) v nepřítomnosti metabolické aktivace. Carbidopa byla negativní v testu in vivo myší mikronukleus.
Entacapon was mutagenic a clastogenic in the in vitro mouse lymphoma tk assay in the presence a absence of metabolic activation a was clastogenic in cultured human lymphocytes in the presence of metabolic activation. Entacapon either alone or in combination with carbidopa-levodopa was negative in the in vivo mouse micronucleus a in the Ames assays.
Poškození plodnosti
V reprodukčních studiích nebyly u potkanů nalezeny žádné účinky na plodnost, které dostávaly Carbidopa-Levodopa v dávkách přibližně 2krát (karbidopa) -4krát (levodopa) MRHD.
U potkanů léčených orálně entakaponem (až 700 mg/kg/den) nebyly pozorovány žádné účinky na plodnost nebo obecnou reprodukční výkonnost. Plazmatické expozice (AUC) při nejvyšší testované dávce byly přibližně 30krát vyšší než u lidí na MRHD entacaponu. Zpožděné páření bylo patrné u žen při nejvyšší testované dávce.
Použití v konkrétních populacích
Těhotenství
Shrnutí rizika
Neexistují žádné přiměřené údaje o vývojovém riziku spojeném s používáním Stalevo u těhotných žen. U zvířat byla podávání Carbidopa-Levodopa nebo entakaponu během těhotenství spojeno s vývojovou toxicitou, včetně zvýšené incidence fetálních malformací (viz Data ). Odhadované riziko na pozadí hlavních vrozených vad a potratu v uvedené populaci není známo. V americké obecné populaci jsou odhadovaná rizika na pozadí hlavních vrozených vad a potratu u klinicky uznávaných těhotenství 2 až 4% a 15 až 20%.
Data
Údaje o zvířatech
In nonclinical studies in which carbidopa-levodopa was administered to pregnant animals increased incidences of visceral and skeletal malformations were observed in rabbits at all doses and ratios of carbidopa-levodopa tested which ranged from 10 times (carbidopa)-5 times (levodopa) to 20 times (carbidopa)-10 times (levodopa) the maximum recommended human dose (MRHD) 1600 mg/den. U potkanů došlo ke snížení počtu živých štěňat dodávaných přehradami, které dostávaly přibližně dvakrát (karbidopa)-pětkrát (levodopa) MRHD v celé organogenezi. U myší dostávajících až 20násobek MRHD Carbidopa-Levodopa nebyly pozorovány žádné účinky na malformační frekvence.
Ve studiích vývoje embryí-fetálních těhotenství dostávaly dávky až 1000 mg/kg/den (potkanů) nebo 300 mg/kg/den (králíci) během organogeneze. Zvýšený výskyt variací plodu byl patrný u vrhů u potkanů léčených nejvyšší dávkou v nepřítomnosti zjevných příznaků mateřské toxicity. Expozice entakaponu v plazmě matek (AUC) spojená s touto dávkou byla přibližně 34krát vyšší než u lidí na MRHD. Zvýšené frekvence potratů a pozdní/celkové resorpce a snížená hmotnost plodu byla pozorována u vrhů králíků ošetřených mateřskými toxickými dávkami 100 mg/kg/den (plazmatická auc méně než u lidí na MRHD) nebo vyšší. V těchto studiích nedošlo k žádnému zvýšení míry malformace.
Když byl entacapon podáván ženám potkanům před pářením a během časného těhotenství byl pozorován zvýšený výskyt anomálií plodu (makroftalmie mikrofthalmia anofthalmie) u vrhů přehrad léčených dávkami 160 mg/kg/dnů (plazmové AUCs sedmkrát, které u lidí v Mrhd) nebo větší v Mrhd) nebo větší v Mrhd) nebo větší v Mrhd) nebo větší než v Mrhd) nebo větší než u lidí) nebo větší. Podávání až 700 mg/kg/den (plazmatické AUC 28krát, které u lidí na MRHD) na potkany během druhé části těhotenství a během laktace neprokázaly žádný důkaz vývojového poškození u potomků.
Laktace
Shrnutí rizika
Levodopa byla detekována v lidském mléce po podání karbidopy-levodopy. Neexistují žádné údaje o přítomnosti entacaponu nebo karbidopy v lidském mléce účinky levodopy karbidopy nebo entakaponu na kojené dítě nebo účinky na produkci mléka. Může však dojít k inhibici laktace, protože levodopa snižuje sekreci prolaktinu [viz Klinická farmakologie ]. Carbidopa a entacapone are excreted in rat milk. In lactating rat oral administration of radiolabeled entacapone resulted in levels of entacapone a/or metabolites in milk up to 2 to 3 times that in plasma. The developmental a health benefits of breastfeeding should be considered along with the mother's clinical need for Stalevo a any potential adverse effects on the breastfed infant from Stalevo or from the underlying maternal condition.
Dětské použití
Bezpečnost a účinnost u pediatrických pacientů nebyla stanovena.
Geriatrické použití
Z celkového počtu subjektů v klinických studiích Stalevo 43,8% bylo 65 let a více, zatímco 7,2% bylo 75 let a více. Mezi těmito subjekty a mladšími subjekty a další hlášené klinické zkušenosti nebyly pozorovány žádné celkové rozdíly v oblasti bezpečnosti nebo účinnosti; Větší citlivost některých starších jedinců však nelze vyloučit.
Stalevo tablets have not been studied in Parkinsonova choroba patients or in healthy volunteers older than 75 years [see Klinická farmakologie ].
Poškození ledvin
Poškození ledvin neovlivňuje farmakokinetiku entakaponu. Neexistují žádné studie o farmakokinetice levodopy a karbidopy u pacientů s poškozením ledvin [viz viz Klinická farmakologie ].
Poškození jater Or Biliary Obstruction
Neexistují žádné studie o farmakokinetice karbidopy a levodopy u pacientů s poškozením jater. Stalevo by měl být podáván opatrně pacientům s biliární obstrukcí nebo jaterním onemocněním, protože biliární vylučování se zdá být hlavní cestou vylučování entacaponu a jaterního zhoršení mělo významný vliv na farmakokinetiku entacaponu, kdy bylo 200 mg entacapone podáno samostatně [viz viz [viz viz [viz viz [viz viz [viz viz [viz viz [viz [viz Klinická farmakologie ].
Informace o předávkování Stalevo
Příznaky a příznaky předávkování
V publikované literatuře je hlášeno jen velmi málo případů předávkování s levodopou. Na základě dostupných informací lze očekávat, že akutní příznaky předávkování inhibitorem levodopy a dopa dekarboxylázy vzniknou z dopaminergní nadměrné stimulace. Dávky několika gramů mohou mít za následek poruchy CNS se zvyšující se pravděpodobností kardiovaskulárního rušení (např. Tachykardie hypotenze) a závažnější psychiatrické problémy při vyšších dávkách. Izolovaná zpráva o rabdomyolýze a další přechodné renální nedostatečnosti naznačuje, že předávkování levodopou může vést ke sekundárnímu nadměrné stimulaci systémových komplikací sekundárních komplikací.
Inhibice COMT léčbou entakaponem je závislá na dávce. Masivní předávkování entacaponem může teoreticky produkovat 100% inhibici enzymu COMT u lidí, čímž se zabrání O-methylaci endogenních a exogenních katecholů.
V klinických studiích byla nejvyšší jediná dávka entakaponu podávaná lidem 800 mg, což vedlo k plazmatické koncentraci 14,1 mcg na ml. Nejvyšší denní dávka poskytovaná lidem byla 2400 mg podávána v jedné studii jako 400 mg šestkrát denně s Carbidopa/Levodopa po dobu 14 dnů u 15 pacientů s Parkinsonovou chorobou a v jiné studii jako 800 mg třikrát denně po dobu 7 dnů u 8 zdravých dobrovolníků. V této denní dávce dosáhly maximální plazmatické koncentrace entacaponu v průměru 2,0 mcg na ml (při 45 minutách ve srovnání s 1,0 mcg na ml a 1,2 mcg na ml s 200 mg entacaponu po 45 minutách). Během této studie byly nejčastěji pozorované nežádoucí účinky břišní bolesti a volné stolice. Denní dávky až 2000 mg entakaponu byly podávány jako 200 mg 10krát denně s Carbidopa/Levodopa nebo Benserazid/Levodopa po dobu nejméně 1 roku u 10 pacientů po dobu nejméně 2 let u 8 pacientů a nejméně 3 roky u 7 pacientů. Celkově však jsou klinické zkušenosti s denními dávkami nad 1600 mg omezené.
Řízení předávkování
Doporučuje se hospitalizace a obecná podpůrná opatření by měla být použita spolu s okamžitým výplachem žaludku a opakovanými dávkami uhlí v průběhu času. To může urychlit eliminaci entakaponu zejména snížením jeho absorpce a reabsorpce z traktu GI. Intravenózní tekutiny by měly být podávány uvážlivě a udržované přiměřené dýchací cesty.
Měla by být monitorována respirační oběhová a renální funkce a použita vhodná podpůrná opatření. Mělo by být zavedeno elektrokardiografické monitorování a pacient pečlivě pozorován pro vývoj arytmií; V případě potřeby by měla být podána příslušná antiarytmická terapie. Je třeba vzít v úvahu možnost, že pacient mohl vzít jiné léky, které zvyšují riziko interakcí s léky (zejména léčiva strukturovaných katechol). K dnešnímu dni nebyla s dialýzou hlášena žádná zkušenost; Proto jeho hodnota při předávkování není známa. Hemodialýza nebo hemoperfúze pravděpodobně nesníží hladiny entakaponu díky své vysoké vazbě na plazmatické proteiny. Pyridoxin není účinný při zvrácení akcí Stalevo.
Kontraindikace pro Stalevo
Stalevo is contraindicated in patients:
- Užívání neselektivních inhibitorů monoamin oxidázy (MAO) (např. Fenelzin a Tranylcypromin). Tyto neselektivní inhibitory MAO musí být přerušeny nejméně dva týdny před zahájením terapie Stalevo.
- S úzkým úhlem glaukom .
Klinická farmakologie for Stalevo
Mechanismus působení
Levodopa
Současné důkazy naznačují, že příznaky Parkinsonovy choroby souvisejí s vyčerpáním dopaminu v corpus striatum. Podávání dopaminu je neúčinné při léčbě Parkinsonovy choroby, protože nepřekročí hematoencefalickou bariéru. Levodopa Metabolický prekurzor dopaminu však překračuje bariéru krve a je pravděpodobně přeměněn na dopamin v mozku. Toto je považováno za mechanismus, podle kterého Levodopa zmírňuje příznaky Parkinsonovy choroby.
Carbidopa
Když je levodopa podávána orálně, je rychle dekarboxylována na dopamin v extracerebrálních tkáních, takže se do centrálního nervového systému transportuje pouze malá část dané dávky. Carbidopa inhibuje dekarboxylaci periferní levodopy, která poskytuje více levodopy k dodání do mozku.
Entacapon
Entacapon is a selective a reversible inhibitor of catechol-O-methyltransferase (COMT).
COMT katalyzuje přenos methylové skupiny S-adenosyl-L-methioninu na fenolickou skupinu substrátů, které obsahují strukturu katecholu. Fyziologické substráty COMT zahrnují dopa katecholaminy (dopamin norepinefrin a epinefrin) a jejich hydroxylované metabolity. Když je Carbidopa COMT zabráněna dekarboxylací levodopy, stane se hlavním metabolizačním enzymem pro levodopu katalyzující jeho metabolismus na 3-methoxy-4-hydroxy-l-fenylalanin (3-OMD).
Farmakokinetika
Farmakokinetika stalevových tablet byla studována u zdravých subjektů (věk 45 let až 75 let). Celkově po podání odpovídajících dávek levodopy karbidopy a entakaponu jako Stalevo nebo jako produkt Carbidopa a Levodopa plus comtan (entacapon) tablety jsou srovnatelné průměrné plazmatické koncentrace levodopy karbidopy a entacaponu.
Absorpce a distribuce
Levodopa i entacapon jsou rychle absorbovány a eliminovány a jejich distribuční objem je mírně malý. Carbidopa je absorbována a eliminována mírně pomaleji ve srovnání s levodopou a entakaponem. Existují značné meziredividuální a intraindividuální změny v absorpci levodopy karbidopy a entacaponu zejména týkající se jeho CMAX.
Účinek potravin na stalevo tabletu nebyl vyhodnocen. Protože Levodopa soutěží s určitými aminokyselinami o transport přes střevní stěnu, může být u některých pacientů po jídle s vysokým obsahem bílkovin narušena absorpce levodopy. Jídla bohatá na velké neutrální aminokyseliny mohou zpožďovat a snížit absorpci levodopy [viz Informace o poradenství pro pacienta ].
Levodopa
Farmakokinetické vlastnosti levodopy po podání jednodádách stalevo (Carbidopa levodopa a entacapon) jsou shrnuty v tabulce 3.
Tabulka 3: Farmakokinetické charakteristiky levodopy s různými silami tabletů Stalevo (průměr ± SD)
| Síla tabletu | AUC0 -∞ (nanogram • H přes ML) | CMAX (nanogram na ml) | Tmax (h) |
| 12,5 mg na 50 mg na 200 mg | 1040 ± 314 | 470 ± 154 | 1,1 ± 0,5 |
| 25 mg na 100 mg na 200 mg | 2910 ± 715 | 975 ± 247 | 1,4 ± 0,6 |
| 37,5 mg na 150 mg na 200 mg | 3770 ± 1120 | 1270 ± 329 | 1,5 ± 0,9 |
| 50 mg na 200 mg na 200 mg | 6115 ± 1536 | 1859 ± 455 | 1,76 ± 0,7 |
Levodopa is bound to plasma protein only to a minor extent (about 10% to 30%).
Carbidopa
Po podání Stalevo jako jedné dávky zdravých mužů a ženských subjektů byla v průměru dosažena maximální koncentrace karbidopy v průměru za 2,5 hodiny až 3,4 hodiny. Průměrná CMAX se pohybovala od přibližně 40 nanogramu na ml do 225 nanogramu na ml a průměrné AUC od 170 nanogramu • h na ml do 1200 nanogram • h na ml s různými stalevovými silami poskytujícími 12,5 mg 25 mg 37,5 mg nebo 50 mg karbidopy.
Carbidopa is approximately 36% bound to plasma protein.
Entacapon
Po podání Stalevo jako jediné dávky zdravým mužským a ženským subjektům byla v průměru dosažena maximální koncentrace entacaponu v plazmě v průměru 0,8 hodiny až 1,2 hodiny. Průměrný CMAX entakaponu byl asi 1200 nanogram na ml až 1500 nanogram na ml a nanogram AUC 1250 • H na ml až 1750 nanagram • h na ml po podání různých stalevových sil, které poskytují 200 mg entacaponu.
Vazba entakaponu v plazmě je 98% v rozmezí koncentrace 0,4 mcg na ml až 50 mcg na ml. Entacapon se váže hlavně na sérový albumin.
Metabolismus a eliminace
Levodopa
Eliminační poločas levodopy Aktivní skupina antiparkinsonovské aktivity byla 1,7 hodiny (rozmezí 1,1 hodiny až 3,2 hodiny).
Levodopa is extensively metabolized to various metabolites. Two major pathways are decarboxylation by dopa decarboxylase (DDC) a O-methylation by COMT.
Carbidopa
Eliminační poločas CARBIDOPA byl v průměru 1,6 hodiny až 2 hodiny (rozmezí 0,7 hodin až 4,0 hodiny).
Carbidopa is metabolized to two main metabolites (α-methyl-3-methoxy-4-hydroxyphenylpropionic acid a α-methyl- 34-dihydroxyphenylpropionic acid). These 2 metabolites are primarily eliminated in the urine unchanged or as glucuronide conjugates. Unchanged carbidopa accounts for 30% of the total urinary excretion.
Entacapon
Eliminační poločas entacaponu byl v průměru 0,8 hodiny až 1 hodinu (NULL,3 hodiny až 4,5 hodiny).
Entacapon is almost completely metabolized prior to excretion with only a very small amount (0.2% of dose) found unchanged in urine. The main metabolic pathway is isomerization to the cis-isomer the only active metabolite. Entacapon a the cis-isomer are eliminated in the urine as glucuronide conjugates. The glucuronides account for 95% of all urinary metabolites (70% as parent a 25% as cis-isomer glucuronides). The glucuronide conjugate of the cis-isomer is inactive. After oral administration of a 14 Dávka C-označená entacaponem 10% značeného rodiče a metabolitu je vylučována močí a 90% ve stolici.
Kvůli krátkému eliminaci poločasu nedochází k skutečné akumulaci levodopy nebo entacaponu, když jsou podávány opakovaně.
Poškození ledvin
Entacapon
Farmakokinetika entakaponu byla zkoumána po jediné 200 mg entakaponové dávce u subjektů s normální střední a vážně narušenou renální funkce bez koálu inhibitoru levodopy a dopa dekarboxylázy. Nebyly nalezeny žádné významné účinky funkce ledvin na farmakokinetiku entakaponu.
Levodopa And carbidopa
Žádné studie o farmakokinetice levodopy a karbidopy u pacientů s poškozením ledvin.
Poškození jater
Entacapon
Hepatální poškození mělo významný vliv na farmakokinetiku entacaponu, když bylo podáno 200 mg entacaponu samostatně. Jedna 200 mg dávka entacaponu bez komosí inhibitoru inhibitoru dekarboxylázy dopa a dopa vykazovala přibližně 2krát vyšší hodnoty AUC a CMAX u pacientů s anamnézou alkoholismu a jaterního poškození (n = 10) ve srovnání s normálními subjekty (n = 10). Všichni pacienti měli biopsii prokázanou cirhózu jater způsobené alkoholem. Podle třídění Child-Pugh mělo 7 pacientů s onemocněním jater mírné poškození jater a 3 pacienti měli střední poškození jater. Vzhledem k tomu, že pouze asi 10% dávky entacaponu je vylučováno močí, protože se zdá, že hlavní cestou vylučování tohoto léčiva je hlavní cestou biliárního vylučování glukuronidu a konjugované glukuronidy. Stalevo by měl být podáván s opatrností pacientům s biliární obstrukcí nebo jaterním onemocněním.
Levodopa And Carbidopa
Neexistují žádné studie o farmakokinetice levodopy a karbidopy u pacientů s jaterním poškozením.
Geriatrické použití
Ve farmakokinetických studiích prováděných u zdravých dobrovolníků po jedné dávce karbidopa-Levodopa- a entacaponu (jako stalevo nebo jako samostatné tablety Carbidopa/Levodopa a Comtan):
Levodopa
AUC Levodopy je významně (v průměru o 10% až 20%) vyšší u starších osob (60 let až 75 let) než mladší subjekty (45 let až 60 let). Neexistuje žádný významný rozdíl v CMAX levodopy mezi mladším (45 až 60 let) a staršími subjekty (60 let až 75 let).
Carbidopa
Neexistuje žádný významný rozdíl v CMAX a AUC karbidopy mezi mladšími (45 let až 60 let) a staršími subjekty (60 až 75 let).
Entacapon
AUC entacaponu je významně (v průměru o 15%) vyšší u starších osob (60 let až 75 let) než mladší subjekty (45 let až 60 let). Neexistuje žádný významný rozdíl v CMAX entacaponu mezi mladším (45 let až 60 let) a staršími subjekty (60 let až 75 let).
Pohlaví
Farmakokinetika following a single dose of carbidopa levodopa a entacapone together either as Stalevo or as separate carbidopa/levodopa a Comtan tablets in healthy volunteers (age range 45 years to 74 years):
Levodopa
Plazmatická expozice (AUC a CMAX) levodopy je významně vyšší u žen než samců (v průměru 40% pro AUC a 30% pro CMAX). Tyto rozdíly jsou primárně vysvětleny tělesnou hmotností. Jiná publikovaná literatura ukázala významný genderový účinek (vyšší koncentrace u žen) i po korekci na tělesnou hmotnost.
Carbidopa
Ve farmakokinetice karbidopy není žádný genderový rozdíl.
Entacapon
Ve farmakokinetice entacaponu není genderový rozdíl.
Studie interakce léčiva
Léčivo metabolizováno COMT
Když byla podávána jediná dávka 400 mg entakaponu společně s intravenózním isoprenalinem (isoproterenol) a epinefrinem bez podávání spolkované levodopy a inhibitoru dopa dekarboxylázy, celkové průměrné maximální změny v srdeční frekvenci během infuze byly asi 50% a 80% vyšší než u placebonů pro isoprenalinu a epinefrin.
Léky, o nichž je známo, že jsou metabolizovány COMT, by měly být podávány s opatrností u pacientů, kteří dostávají entakapon bez ohledu na cestu podávání [viz Lékové interakce ].
Léky metabolizované přes CYP2C9
Díky své afinitě k CYP2C9 může in vitro entakapon potenciálně narušit léčivé produkty s metabolismem závislým na tomto isoenzymu. Ve studii interakce u zdravých dobrovolníků entacapon zvýšil AUC R-Warfarinu v průměru o 18% a hodnoty INR se v průměru zvýšily o 13% [viz viz Lékové interakce ].
Hormonální hladiny
Je známo, že ingredience ve Stalevo Levodopa snižují sekreci prolaktinu a zvyšují růstový hormon úrovně.
Klinické studie
Účinnost entakaponu jako doplňku k levodopě při léčbě Parkinsonovy choroby byla stanovena ve třech 24týdenních multicentrizovaných randomizovaných dvojitě zaslepených placebem kontrolovaných studiích u pacientů s Parkinsonovou chorobou. Ve 2 z těchto studií (studie 1 a 2) onemocnění pacientů kolísalo, tj. Byla charakterizována zdokumentovanými obdobími ON (období relativně dobrého fungování) a vypnutá (období relativně špatného fungování) navzdory optimální levododové terapii. Po 6 měsících léčby došlo také k odběru. Ve třetím studii se pacienti nemuseli zabývat fluktuacemi. Před kontrolovanou částí těchto studií byli pacienti stabilizováni na levodopě po dobu 2 týdnů až 4 týdnů.
U pacientů, kteří nezažívají fluktuace, existují omezené zkušenosti s používáním entakaponu.
Ve studiích 1 a 2 pacienti byli randomizováni, aby dostávali placebo nebo entacapon 200 mg podávané současně s každou dávkou karbidopy/levodopy (až 10krát denně, ale pacienti průměrovali 4 dávky na 6 dávek denně). Dvojitá slepá část obou studií byla dlouhá 6 měsíců. Pacienti pravidelně zaznamenávali čas strávený ve státech ON a OFF v domácích denících po celou dobu studie. V jedné studii provedené v severských zemích byl primárním výsledkem měřítko celkový průměrný čas strávený ve státě ON během 18hodinového deníku zaznamenaného dne (6:00 do půlnoci). V jiné studii byl primárním výsledkem měřítkem podíl probuzení stráveného více než 24 hodin ve stavu ON.
Kromě měření primárního výsledku byla vyhodnocena doba strávená ve stavu off a pacienti byli také hodnoceni hlavami sjednocené stupnice hodnocení Parkinsonovy choroby (UPDR) často používanou vícenásobnou stupnicí hodnocení (část I) aktivity každodenního života (část II) motorické funkce (část III); globální hodnocení klinického stavu a pacienta a pacienta a 7-bodová subjektivní stupnice určená k posouzení globálního fungování Parkinsonovy choroby; a změna v denní dávce Carbidopa/Levodopa.
Jaký typ antibiotiky je cefdinir
Ve studii 1 171 pacientů bylo randomizováno v 16 centrech ve Finsku Norsko Švédsko a Dánsko (studie 1), z nichž všichni dostali souběžnou levodopu plus inhibitor dopa dekarboxylázy (buď Carbidopa/Levodopa nebo Benserazid/Levodopa). Ve studii 2 205 pacientů bylo randomizováno v 17 centrech v Severní Americe (USA a Kanada); Všichni pacienti dostávali souběžnou karbidopu/levodopu.
Výsledky těchto dvou studií zobrazují následující tabulky (tabulka 4 a tabulka 5):
Tabulka 4: Výsledky účinnosti studie 1
| Primární opatření z domácího deníku (z 18hodinového deníku) | |||
| Základní linie | Změnit z výchozí hodnoty v 6. měsíci* | P-hodnota vs. placebo | |
| Hodiny vzhůru | |||
| Placebo | 9.2 | 0,1 | - |
| Entacapon | 9.3 | 1.5 | Méně než 0,001 |
| Trvání včas po první dávce (HRS) | |||
| Placebo | 2.2 | 0.0 | - |
| Entacapon | 2.1 | 0,2 | Méně než 0,05 |
| Sekundární opatření z domácího deníku (z 18hodinového deníku) † | |||
| Hodiny vzhůru volna | |||
| Placebo | 5.3 | 0.0 | - |
| Entacapon | 5.5 | -1.3 | Méně než 0,001 |
| Podíl času probuzení na ‡ (%) | |||
| Placebo | 63.8 | 0,6 | - |
| Entacapon | 62.7 | 9.3 | Méně než 0,001 |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 705 | 14 | - |
| Entacapon | 701 | -87 | Méně než 0,001 |
| Frekvence denního příjmu Levodopy | |||
| Placebo | 6.1 | 0,1 | - |
| Entacapon | 6.2 | - 0,4 | Méně než 0,001 |
| Další sekundární opatření | |||
| Základní linie | Změna z výchozího hodnoty v 6. měsíci | P-hodnota vs. placebo | |
| Globální (celkově) % vylepšená | |||
| Placebo | - | 28 | - |
| Entacapon | - | 56 | Méně než 0,01 |
| Globální (celková) % pacienta vylepšená | |||
| Placebo | - | 22 | - |
| Entacapon | - | 39 | N.S.¶ |
| Celkem UPDRS | |||
| Placebo | 37.4 | -1.1 | - |
| Entacapon | 38.5 | -4.8 | Méně než 0,01 |
| Motor UPDRS | |||
| Placebo | 24.6 | -0.7 | - |
| Entacapon | 25.5 | -3.3 | Méně než 0,05 |
| UPDRS ADL | |||
| Placebo | 11.0 | -0.4 | - |
| Entacapon | 11.2 | -1.8 | Méně než 0,05 |
| *Střední; Hodnoty měsíce 6 představují průměr týdnů 8 16 a 24 podle měření výsledku definovaného protokolem. † Hodnoty P pro sekundární opatření jsou nominální hodnoty p bez jakékoli úpravy pro multiplicitu. ‡ Není to koncový bod pro tuto studii, ale primární koncový bod v severoamerické studii. § nejméně jedna změna kategorie v koncovém bodě. „Nevýznamné. |
Tabulka 5: Výsledky účinnosti studie 2
| Primární opatření z domácího deníku (pro 24hodinový den deníku) | |||
| Základní linie | Změnit z výchozí hodnoty v 6. měsíci* | P-hodnota vs. placebo | |
| Procento vzhůru | |||
| Placebo | 60.8 | 2.0 | - |
| Entacapon | 60.0 | 6.7 | Méně než 0,05 |
| Sekundární opatření z domácího deníku (pro 24hodinový den deníku) † | |||
| Hodiny vzhůru volna | |||
| Placebo | 6.6 | -0.3 | - |
| Entacapon | 6.8 | -1.2 | Méně než 0,01 |
| Hodiny vzhůru | |||
| Placebo | 10.3 | 0,4 | - |
| Entacapon | 10.2 | 1.0 | N.S. ‡ |
| Levodopa Total Daily Dose (mg) | |||
| Placebo | 758 | 19 | - |
| Entacapon | 804 | -93 | Méně než 0,001 |
| Frekvence denního příjmu Levodopy | |||
| Placebo | 6.0 | 0,2 | - |
| Entacapon | 6.2 | 0.0 | N.s. ‡ |
| Další sekundární opatření† | |||
| Základní linie | Změna z výchozího hodnoty v 6. měsíci | P-hodnota vs. placebo | |
| Globální (celkově) % vylepšená | |||
| Placebo | - | 21 | - |
| Entacapon | - | 34 | Méně než 0,05 |
| Globální (celková) % pacienta vylepšená | |||
| Placebo | - | 20 | - |
| Entacapon | - | 31 | Méně než 0,05 |
| Celkem UPDRS¶ | |||
| Placebo | 35.6 | 2.8 | - |
| Entacapon | 35.1 | -0.6 | Méně než 0,05 |
| Motor UPDRS ¶ | |||
| Placebo | 22.6 | 1.2 | - |
| Entacapon | 22.0 | -0.9 | Méně než 0,05 |
| UPDRS ADL¶ | |||
| Placebo | 11.7 | 1.1 | - |
| Entacapon | 11.9 | 0.0 | Méně než 0,05 |
| *Střední; Hodnoty měsíce 6 představují průměr týdnů 8 16 a 24 podle měření výsledku definovaného protokolem. † Hodnoty P pro sekundární opatření jsou nominální hodnoty p bez jakékoli úpravy pro multiplicitu. ‡ Není významné. § nejméně jedna změna kategorie v koncovém bodě. ¶Score změna v koncovém bodě podobně jako severská studie. |
Účinky na čas se nelišily podle věku závažnosti onemocnění pohlaví na základě dávky levodopy a souběžné léčby dopaminovým agonisty nebo selegilinem.
Stažení entacaponu
Ve studii 2 náhlé stažení entacaponu bez změny dávky karbidopy/levodopy vedlo k významnému zhoršení fluktuací ve srovnání s placebem. V některých případech byly příznaky o něco horší než na začátku, ale vrátily se k přibližně základní závažnosti do 2 týdnů po zvýšení dávky levodopy v průměru o 80 mg. Ve studii 1 Podobně bylo pozorováno významné zhoršení parkinsonovských symptomů po odběru entacaponu, jak bylo hodnoceno 2 týdny po odběru léčiva. V této fázi byly příznaky přibližně při začátku závažnosti po zvýšení dávky levodopy o asi 50 mg.
Ve třetí placebem kontrolované studii (studie 3) bylo celkem 301 pacientů randomizováno ve 32 centrech v Německu a Rakousku. V této studii jako v ostatních 2 studiích byl podáván entacapon 200 mg s každou dávkou inhibitoru levodopy a dopa dekarboxylázy (až 10krát denně) a částmi UPDRS II a III a celkový den denně včas byly primárními měřeními účinnosti. Výsledky primárních opatření i pro některá sekundární opatření jsou uvedeny v tabulce 6.
Tabulka 6: Výsledky účinnosti studie 3
| Primární opatření | |||
| Základní linie | Změna z výchozího hodnoty v 6. měsíci | P-hodnota vs. placebo (LOCF) | |
| Updrsadl* | |||
| Placebo | 12.0 | 0,5 | - |
| Entacapon | 12.4 | -0.4 | Méně než 0,05 |
| Motor UPDRS* | |||
| Placebo | 24.1 | 0,1 | - |
| Entacapon | 24.9 | -2.5 | Méně než 0,05 |
| Hodiny vzhůru (Home Diary)† | |||
| Placebo | 10.1 | 0,5 | - |
| Entacapon | 10.2 | 1.1 | N.S. ‡ |
| Sekundární opatření od | |||
| Základní linie | Změna z výchozího hodnoty v 6. měsíci | P-hodnota vs. placebo | |
| Celkem UPDRS * | |||
| Placebo | 37.7 | 0,6 | - |
| Entacapon | 39.0 | -3.4 | Méně než 0,05 |
| Procento vzhůru (Home Diary) ** | |||
| Placebo | 59.8 | 3.5 | - |
| Entacapon | 62.0 | 6.5 | N.s. ‡ |
| Hodiny vzhůru volna (Home Diary) | |||
| Placebo | 6.8 | -0.6 | - |
| Entacapon | 6.3 | -1.2 | 0.07 |
| Levodopa Total Daily Dose (mg)* | |||
| Placebo | 572 | 4 | - |
| Entacapon | 566 | -35 | N.s. |
| Frekvence denního příjmu levodopy* | |||
| Placebo | 5.6 | 0,2 | - |
| Entacapon | 5.4 | 0.0 | Méně než 0,01 |
| Globální (celkově) % vylepšené. | |||
| Placebo | - | 34 | - |
| Entacapon | - | 38 | N.S. ‡ |
| *Celková populace; Změna skóre v koncovém bodě. † Kolísající populace s 5 dávkami až 10 dávek; Změna skóre v koncovém bodě. ‡ Není významné. Hodnoty §p pro sekundární opatření jsou nominální hodnoty P bez jakékoli úpravy pro multiplicitu. ¶Totalská populace; Alespoň jedna změna kategorie v koncovém bodě. |
Informace o pacientovi pro Stalevo
Usínání během činností každodenního života a somnolence
Poraďte pacientům o možném sedaci účinků spojených se Stalevo, včetně somnolence a možnosti usínání při zachování činností každodenního života. Protože somnolence může být častým nežádoucím reakcí s potenciálně závažnými důsledky, že pacienti by neměli řídit motorové vozidlo provozovat těžké stroje nebo se zapojit do jiných potenciálně nebezpečných činností, dokud nezískají dostatečné zkušenosti se Stalevo, aby určili, zda to ovlivňuje jejich mentální a/nebo motorový výkon nepříznivě [viz viz [Viz [Viz [Viz [Viz Varování a preventivní opatření ]. Advise patients that if increased somnolence or episodes of falling asleep during activities of daily living (e.g. conversations eating driving a motor vehicle etc.) are experienced at any time during treatment they should not drive or participate in potentially dangerous activities until they have contacted their physician.
Před podáním léků na sedaci alkoholu nebo jiných depresiv CNS (např. Benzodiazepiny antipsychotics antidepresiva atd.) Z důvodu možných aditivních účinků v kombinaci se stalevo radí pacientům, aby hovořili se svým předepisovaným zdravotním předpiserem nebo jinými depresivy CNS (např. Benzodiazepiny antipsychotiky atd.).
Hypotenze Orthostatic Hypotenze And Syncope
Doporučují pacientům, že se mohou vyvinout symptomatická (nebo asymptomatická) posturální (ortostatická) hypotenze nebo netorostatickou hypotenzi při užívání stalevo. Hypotenze/ortostatická hypotenze se může během počáteční terapie častěji vyskytovat častěji. Po sezení nebo ležení by se pacienti neměli rychle zvyšovat, zejména pokud tak učinili po delší dobu a zejména při zahájení léčby Stalevo.
Poraďte pacientům o potenciálu synkopy u pacientů pomocí agonistů dopaminu. Z tohoto důvodu informujte pacienty o možnosti synkopy při užívání Stalevo [viz Varování a preventivní opatření ].
Dyskinesies
Informujte pacienty, že Stalevo může způsobit a/nebo prohloubit již existující dyskinesii [viz Varování a preventivní opatření ].
Halucinace a/nebo psychotické chování
Informujte pacienty, že při užívání Stalevo může dojít k halucinacím a dalším psychotickému chování [viz Varování a preventivní opatření ].
Kontrola impulsů a/nebo nutkavé chování
Poraďte pacientům, že mohou zažít kontrolu impulsu a/nebo nutkavé chování při užívání jednoho nebo více léků používaných k léčbě Parkinsonovy choroby včetně Stalevo. Zeptejte se pacientů na vývoj nových nebo zvýšených hazardních nutkání sexuálních nutkání o naléhavé nouze o nekontrolované výdaje nebo jiné intenzivní nutkání při léčbě Stalevo. Doporučují pacientům, aby informovali svého lékaře nebo poskytovatele zdravotní péče, pokud zažívají nové nebo zvýšené nouze v hazardních hrách, zvýšená sexuální nutkání nebo jiné intenzivní nutkání při bití Stalevo. Lékaři by měli zvážit redukci dávky nebo zastavit léky, pokud se pacient vyvine takové nutkání při užívání Stalevo [viz Varování a preventivní opatření ].
ATHERACE-Engergent Hyperpyrexia a zmatek
Doporučují pacientům, že mohou vyvinout horečku a zmatek jako součást syndromu připomínajícího NM a pravděpodobně s jinými klinickými rysy (např. Svalová rigidita autonomní hyper- nebo hypotenze atd.). K tomuto syndromu horečky a zmatení se může objevit zejména se snížením dávky nebo stažení Stalevo, ale může se také vyvinout po zahájení léčby. Doporučujte pacientům, aby kontaktovali svého poskytovatele zdravotní péče, pokud si přejí přerušit nebo snížit dávku Stalevo a kontaktovat poskytovatele zdravotní péče, pokud vyvinou horečku a zmatek [viz viz Varování a preventivní opatření ].
Průjem And Colitis
Informujte pacienty, že průjem se může vyskytnout u Stalevo a může mít zpožděný nástup. Někdy může být prodloužený průjem způsoben kolitidou (zánět tlustého střeva). Pacienti s průjmem by měli pít tekutiny, aby udrželi přiměřenou hydrataci a sledovali úbytek hmotnosti. Pokud je průjem spojený se stalevo prodloužený, očekává se, že lék povede k rozlišení. Pokud průjem pokračuje po zastavení Stalevo, může být zapotřebí další diagnostická vyšetřování. V některých případech může být průjem s kolitidou [viz viz Varování a preventivní opatření ].
Rhabdomyolýza
Poraďte pacientům, že se mohou vyvinout rabdomyolýza a myalgii, pokud zažijí prodlouženou motorickou aktivitu včetně dyskineze. Tato událost může být také spojena s horečkou a zmatkem [viz Varování a preventivní opatření ].
Nevolnost And Zvracení
Informujte pacienty, že stalevo může způsobit nevolnost a zvracení se může objevit častěji během počáteční terapie a může vyžadovat nastavení dávky.
Pokyny pro použití
Poskytněte pacientům, aby užívali Stalevo pouze podle předepsaného. Poskytněte pacientům, aby v každém intervalu dávkování užívali pouze jeden tablet Stalevo. Poskytněte pacientům, aby nebrali více tablet nebo dalších částí tablet k dosažení vyšší dávky levodopy. Doporučujte pacientům, aby nerozdělili nebo žvýkali Stalevo.
Informujte pacienta, že Stalevo je formulace karbidopy/levodopy kombinovaných s entacaponem, který je navržen tak, aby zahájil uvolňování přísad do 30 minut po požití. Je důležité, aby byl Stalevo přijato v pravidelných intervalech podle harmonogramu nastíněného lékařem. Upozorněte pacienta, aby nezměnil předepsaný dávkový režim a nepřidal žádné další antiparkinsonovské léky, včetně jiných přípravků Carbidopa/Levodopa, aniž by se nejprve konzultoval lékaře.
Doporučujte pacientům, že na konci dávkovacího intervalu se mohou vyskytnout epizody (opotřebení léčivého efektu), ale může dojít k nepředvídatelnému z epizod. Doporučujte pacientovi, aby informoval poskytovatele zdravotní péče o možnou úpravu léčby, pokud taková odpověď představuje problém pro každodenní život pacienta.
Poraďte pacientům, že tmavé zbarvení (červené hnědé nebo černé) se může po užití Stalevo objevit v moči slin nebo potu. Ačkoli se zdá, že barva je klinicky nevýznamné oděvy, mohou být zbarveny.
Doporučujte pacientům, že změna stravy na potraviny s vysokým obsahem bílkovin může zpozdit absorpci levodopy. Nadměrná kyselost také zpožďuje vyprazdňování žaludku, čímž zpožďuje absorpci levodopy. Železové soli (například v multi-vitaminových tabletách) mohou také snížit účinnost Stalevo.
Těhotenství
Poskytněte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud otěhotní nebo mají v úmyslu otěhotnět během terapie [viz Použití v konkrétních populacích ].
Laktace
Poskytněte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud mají v úmyslu kojit nebo kojí kojence [viz viz Použití v konkrétních populacích ].
