Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
Kortikosteroidy, aktuálníKenalog sprej
Shrnutí drog
Co je kenalog sprej?
Kenalog Spray (triamcinolon acetonid) je aktuální kortikosteroid označený pro reliéf svědění v důsledku podráždění kůže. Kenalog sprej je k dispozici jako a generická droga .
Jaké jsou vedlejší účinky kenalogového spreje?
Mezi běžné vedlejší účinky kenalogového spreje patří podráždění a suchost. Mezi závažné vedlejší účinky kenalogového spreje patří:
- Těžká vyrážka na pokožku
- dušnost
- potíže polykání a
- infekce kůže
Dávkování pro kenalog sprej
Kenalog sprej je dodáván ve dvou velikostech 63 a 100 mg plechovky v síle 0,147 mg na gram. Pokyny pro použití spreje jsou uvedeny na štítku. Kenalogový sprej může být aplikován na jakoukoli oblast těla, i když je třeba dbát na to, aby bylo zakryté oči a že se při stříkání po obličeji vyhýbá vdechování spreje.
Jaké léčivé látky nebo doplňky interagují s kenalogovým sprejem?
Kenalog sprej může interagovat s jinými léky. Řekněte svému lékaři všechny léky a doplňky, které používáte.
Kenalog sprej během těhotenství nebo kojení
Neexistují žádné adekvátní a dobře kontrolované studie u těhotných žen na teratogenních účincích z topicky aplikovaných kortikosteroidů, jako je kenalog sprej. Proto by se během těhotenství měly používat lokální kortikosteroidy, pouze pokud potenciální výhoda ospravedlňuje potenciální riziko pro plod. Topicky aplikované kortikosteroidy by se neměly používat u těhotných pacientů ve velkém množství nebo po delší dobu. Není známo, zda je použití kenalogového spreje detekovatelné v mateřském mléce. Pokud jsou lokální kortikosteroidy podávány ošetřovatelské ženě, by mělo být opatrno opatrně. Kenalog sprej by měl být používán opatrně u dětí z důvodu většího poměru povrchu kůže k tělesné hmotnosti k tomu, aby byly více náchylné k syndromu potlačení nadlectvů a intrakraniální hypertenze, z nichž všechny byly hlášeny u dětí, které dostávají topické kortikosteroidy.
Další informace
Naše středisko drog pro vedlejší účinky kenalogu poskytuje při užívání tohoto léku komplexní pohled na dostupné informace o potenciálních vedlejších účincích.
Informace o drogách FDA
Pouze pro dermatologické použití
Ne pro oftalmické použití
Popis pro kenalog sprej
The topical corticosteroids constitute a class of primarily synthetic steroids used as anti-inflammatory and antipruritic agents. The steroids in this class include triamcinolone acetonide. Triamcinolone acetonide is designated chemically as 9-fluoro-11β 16α 17 21-tetrahydroxypregna-1 4-diene-3 20-dione cyclic 16 17-acetal with acetone. The structural formula is:
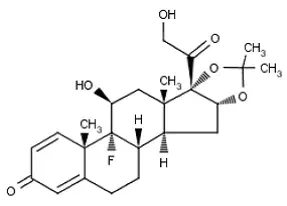 |
C 24 H 31 Fo 6
Dvousekundová aplikace, která pokrývá plochu přibližně velikost ruky, dodává množství triamcinolonového acetonidu nepřesahující 0,2 mg. Po postřiku nevolatilního vozidla zbývajícího na kůži obsahuje přibližně 0,2% triamcinolon acetonid. Každý gram spreje poskytuje 0,147 mg triamcinolon acetonidu ve vehikulu isopropyl palmitátového dehydratovaného alkoholu (NULL,3%) a izobutanového hnacího látky.
Jak dlouho vydrží účinky soma
Použití pro kenalog sprej
Kenalog sprej (triamcinolon acetonid topický aerosol USP) je indikován pro reliéf zánětlivých a pruritických projevů kortikosteroid-reagujících dermatóz.
Dávkování pro kenalog sprej
Pokyny pro použití spreje jsou uvedeny na štítku. Příprava může být aplikována na jakoukoli oblast těla, ale když je nastříkána ohledně péče o obličej, aby se zjistilo, že jsou zakryté oči a že se vyhýbá vdechování spreje.
Sprej je hořlavý; Při použití tohoto produktu se vyhněte plameni nebo kouření.
Tři nebo čtyři aplikace denně kenalogového spreje (triamcinolon acetonid topický aerosol) jsou obecně dostatečné.
Jak dodáno
Kenalog sprej (triamcinolon acetonid topický aerosol USP)
63 g ( NDC 10631-093-62) Aerosol Can.
100 g ( NDC 10631-093-07) Aerosol Can.
Skladování a manipulace
Skladovat při pokojové teplotě; Vyvarujte se nadměrného tepla. Obsah pod tlakem; Nepřipsačujte se ani nesparujte. Udržujte mimo dosah dětí.
Chcete-li nahlásit podezření na nežádoucí účinky, kontaktujte FDA na 1-800-FDA-1088 nebo WWW. FDA. jít v/medwatch.
Ranbaxy Jacksonville FL 32257 USA. Revidováno v červenci 2011
Vedlejší účinky pro kenalog sprej
The following local adverse reactions are reported infrequently with topical corticosteroids but may occur more frequently with the use of occlusive dressings (reactions are listed in an approximate decreasing order of occurrence): burning itching irritation dryness folliculitis hypertrichosis acneiform eruptions hypopigmentation perioral dermatitis allergic contact dermatitis maceration of the skin secondary infection skin atrophy striae amiliaria.
Interakce léčiva pro kenalog sprej
Žádné informace.
může příliš mnoho KepPra způsobit záchvaty
Varování pro kenalog sprej
Žádné informace.
Opatření pro kenalog sprej
Generál
Systémová absorpce lokálních kortikosteroidů vyvolala reverzibilní hypothalamicko-hypofýz-nadledvinovou (HPA) a u některých pacientů se u některých pacientů projevily projevy hyperglykémie a glukosurie Gushingové.
Podmínky, které zvyšují systémovou absorpci, zahrnují aplikaci účinnějších steroidů využívajících při velkých povrchových plochách prodloužených používání a přidání okluzivních obvazů.
Proto pacienti, kteří dostávají velkou dávku jakéhokoli silného topického steroidu aplikovaného na velkou povrchovou plochu nebo pod okluzivním obvazem, by proto měli být pravidelně hodnoceni, aby se dokazovaly o HP a potlačení osy pomocí testů stimulace volného kortizolu a ACTH a pro zhoršení tepelné homeostázy. Pokud dojde k potlačení nebo zvýšení tělesné teploty HP, měl by být učiněn pokus o odstoupení léčiva, aby se snížila frekvence aplikace nahradit méně účinný steroid nebo použít sekvenční přístup.
Obnovení funkce HP A osy a tepelné homeostázy jsou obecně rychlé a úplné po přerušení léčiva. Obavě příznaky a příznaky stažení steroidů mohou nastat vyžadující doplňkové systémové kortikosteroidy.
Děti mohou absorbovat úměrně větší množství topických kortikosteroidů, a proto jsou náchylnější k systémové toxicitě (viz Opatření pediatrické použití ).
Co se používá k léčbě Benicar
Pokud se podráždění vyvine lokální kortikosteroidy, měly by být přerušeny a zavedena vhodná terapie.
V přítomnosti dermatologických infekcí by mělo být zavedeno použití vhodného antimykotického nebo antibakteriálního činidla. Pokud k příznivé reakci nedochází okamžitě, měl by být kortikosteroid přerušen, dokud nebude infekce přiměřeně kontrolována.
Laboratorní testy
Při hodnocení potlačení osy HPA může být užitečný test volného kortizolu v moči a test stimulace ACTH.
Zhodnocení mutageneze karcinogeneze plodnosti
Dlouhodobé studie na zvířatech nebyly provedeny za účelem vyhodnocení karcinogenního potenciálu nebo účinku na plodnost topických kortikosteroidů.
Studie pro stanovení mutagenity s prednisolonem a hydrokortisonem vykazovaly negativní výsledky.
Těhotenství: Teratogenní účinky
Category C. Corticosteroids are generally teratogenic in laboratory animals when administered systemically at relatively low dosage levels. The more potent corticosteroids have been shown to be teratogenic after dermal application in laboratory animals. There are no adequate and well-controlled studies in pregnant women on teratogenic effects from topically applied corticosteroids. Therefore topical corticosteroids should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus. Drugs of this class should not be used extensively on pregnant patients in large amounts or for prolonged periods of time.
Ošetřovatelské matky
Není známo, zda topické podávání kortikosteroidů může vést k dostatečné systémové absorpci, aby se vytvořila detekovatelná množství v mateřském mléce. Systemicky podávané kortikosteroidy jsou vylučovány do mateřského mléka v množství, které pravděpodobně nebudou mít škodlivý účinek na dítě. Pokud jsou však ošetřovatelskou ženu podávány lokální kortikosteroidy.
Dětské použití
Pediatričtí pacienti mohou prokázat větší náchylnost k topickému kortikosteroidskému potlačení osy HPA a syndromu Cushingu než zranění pacienti kvůli většímu poměru povrchu kůže k tělesné hmotnosti.
U dětí, které dostávají lokální kortikosteroidy, byly hlášeny syndrom a intrakraniální hypertenze HPA. Projevy potlačení nadledvin u dětí zahrnují lineární retardaci růstu zpožděné nárůst hmotnosti nízký plazmatický kortizol a absence reakce na stimulaci ACTH. Projevy intrakraniální hypertenze zahrnují vypouklé fontanely bolesti hlavy a bilaterální papiledema.
Podávání topických kortikosteroidů pro děti by mělo být omezeno na nejmenší množství kompatibilní s účinným terapeutickým režimem. Chronická kortikosteroidní terapie může narušit růst a vývoj dětí.
Informace o předávkování pro kenalog sprej
Topicky aplikované kortikosteroidy mohou být absorbovány v dostatečném množství k vytvoření systémových účinků (viz OPATŘENÍ Generál ).
Kontraindikace pro kenalog sprej
Lokální kortikosteroidy jsou kontraindikovány u pacientů s anamnézou přecitlivělosti na některou ze složek příprav.
Klinická farmakologie for Kenalog Spray
Lokální kortikosteroidy sdílejí protizánětlivé antipruritické a vazokonstrikční účinky.
Mechanismus protizánětlivé aktivity topických kortikosteroidů je nejasný. K porovnání a predikci potence a/nebo klinické účinnosti topických kortikosteroidů se používají různé laboratorní metody včetně vazokonstrikčních testů. Existují důkazy, které naznačují, že existuje rozpoznatelná korelace mezi vazokonstrikční účinností a terapeutickou účinností u člověka.
Rozdíl mezi Sprintec a Tri Sprintec
Farmakokinetika
Rozsah perkutánní absorpce topických kortikosteroidů je určen mnoha faktory, včetně vehikula, integrita epidermální bariéry a použití okluzivních obvazů.
Lokální kortikosteroidy mohou být absorbovány z normální neporušené kůže. Zánět a/nebo jiné procesy onemocnění v kůži zvyšují perkutánní absorpci.
Jakmile jsou absorbovány kůží lokální kortikosteroidy zpracovávány farmakokinetickými cestami podobnými systémově podávanými kortikosteroidy. Kortikosteroidy jsou vázány na plazmatické proteiny v různých stupních. Kortikosteroidy jsou metabolizovány primárně v játrech a poté jsou vylučovány ledvinami. Některé z aktuálních kortikosteroidů a jejich metabolitů jsou také vylučovány do dokonce .
Informace o pacientovi pro kenalog sprej
Pacienti používající kenalog sprej by měli dostávat následující informace a pokyny:
- Tento lék má být používán jako pokyn lékařem. Je pouze pro externí použití; Vyvarujte se kontaktu s očima a inhalací spreje.
- Pacienti by měli být doporučeni, aby tento lék nepoužívali pro jinou poruchu, než na kterou byla předepsána.
- Ošetřená oblast kůže by neměla být ovázaná nebo jinak zakrytá nebo zabalena jako okluzivní, pokud není nařízena lékařem.
- Pacienti by měli hlásit jakékoli známky místních nežádoucích účinků.
- Rodičům dětských pacientů by mělo být doporučeno, aby nepoužívali pevně padnoucí plenky nebo plastové kalhoty na dítě léčené v oblasti plenky, protože tyto oděvy mohou představovat okluzivní obvazy.
- Nepoužívejte kenalogový sprej na podpaží nebo třísla, pokud není nasměrován váš lékař.
- Pokud není vidět žádné zlepšení do 2 týdnů, kontaktujte svého lékaře.
- Při používání kenalogového spreje nepoužívejte jiné produkty obsahující kortikosteroidy, aniž byste se nejprve poradili s lékařem.
- Kenalog Spray je hořlavý. Při použití kenalogového spreje se vyhněte tepelným plamenům nebo kouřením.
