Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
Antikonvulziva, jinéFintepla
Shrnutí drog
Co je to Fintepla?
Fintepla (fenfluramin) je Antikonvulziva Používá se k léčbě záchvatů spojených s Dravetovým syndromem u pacientů ve věku 2 let a starší.
Jaké jsou vedlejší účinky Finteply?
Fintepla
- kopřivka
- potíže s dýcháním
- Otok vašeho obličeje rty jazyk nebo krk
- změny nálady nebo chování
- úzkost
- panické útoky
- potíže se spánkem
- impulzivita
- míchání
- nepřátelství
- agrese
- neklid
- hyperaktivita (mentálně nebo fyzicky)
- zvýšená deprese
- Myšlenky na sebepoškození
- bolest na hrudi
- Bušící srdeční rytmus
- Flutteting v hrudi
- dušnost
- modrá barevná kůže nebo rty
- Otok ve vašich dolních nohách
- neobvyklá únava
- slabost
- Lightheadedness
- Ztráta chuti k jídlu
- hubnutí
- Zhoršující se záchvaty
- rozmazané vidění
- Vize tunelu
- Bolest očí nebo zarudnutí
- Vidět halos kolem světla
- nevolnost
- zvracení
- Těžká bolest hlavy
- rozmazané vidění
- Bušení do krku nebo uší
- krvácení z nosu
- horečka
- pocení
- halucinace
- Chvění
- Rychlá srdeční frekvence
- ztuhlost svalu
- Twitching
- zpomalený růst (u dětí)
- ztráta koordinace a
- průjem
Získejte lékařskou pomoc okamžitě, pokud máte výše uvedené příznaky.
Mezi vedlejší účinky Fintepla patří:
- snížená chuť k jídlu
- ospalost
- sedace
- letargie
- průjem
- zácpa
- Abnormální echokardiogram
- únava
- Cítíte se dobře (malátnost)
- slabost
- Problémy s koordinací svalů
- Porucha rovnováhy
- Porucha chůze
- zvýšený krevní tlak
- slintání/nadbytek slinění
- horečka
- infekce horních cest dýchacích
- zvracení
- hubnutí
- pády a
- status epilepticus
Pokud máte následující vážné vedlejší účinky, vyhledejte lékařskou péči nebo zavolejte na číslo 911:
- Vážné příznaky očí, jako je ztráta náhlého vidění rozmazané vidění vidění Vision Vision Eye Eye Eye Eye Eye Eye Eye Eye nebo vidět halos kolem světel;
- Vážné příznaky srdce, jako je rychlé nepravidelné nebo bušení srdečního rytmu; třepování v hrudi; dušnost; a náhlé závratě lightheadness nebo omdlení;
- Těžká zmatek bolesti hlavy zkažená paže řeči nebo slabost nohou Potíže se ztrátou chůze pocitu koordinace Nestabilní velmi tuhé svaly vysoké horečky bohaté pocení nebo třes.
Tento dokument neobsahuje všechny možné vedlejší účinky a mohou dojít k jiným. Další informace o vedlejších účincích najdete u svého lékaře.
Dávkování pro Fintepla
Počáteční počáteční a údržbářská dávka FintePLA je 0,1 mg/kg dvakrát denně, což může být zvýšeno každý týden na základě účinnosti a snášenlivosti.
Fintepla u dětí
U pacientů ve věku a starších a starších byla stanovena bezpečnost a účinnost Fintepla pro léčbu záchvatů spojených s Dravetovým syndromem. Bezpečnost a účinnost finteply u pacientů mladších 2 let nebyla stanovena.
Dystonie a další extrapyramidové příznaky spojené s metoklopramidem jsou častější u pediatrických pacientů než u dospělých. Kromě toho novorozenci mají sníženou hladinu NADH-Cytochrom B5 reduktázy, což je činí náchylnější k methemoglobinemii možnou nežádoucí reakcí užívání metoklopramidu u novorozenců.
Jaké léčivé látky nebo doplňky interagují s Finteplou?
Fintepla může interagovat s jinými léky, jako jsou:
- rifampin
- StiriPentol Plus Clobazam
- Cyproheptadin
- Silné 5-HT1A 5- HT1D 5-HT2A nebo 5-HT2C serotonin Antagonisté receptoru a
- Léky volně prodejné léky nebo bylinné doplňky, které zvyšují serotonin, jako jsou selektivní inhibitory zpětného vychytávání serotoninu (SSRIS) serotonin-norepinefrin inhibitory zpětného vychytávání (SNRIS) Tricyklická antidepresiva Inhibitory monoamin oxidázy
Řekněte svému lékaři všechny léky a doplňky, které používáte.
Fintepla během těhotenství a kojení
Řekněte svému lékaři, pokud jste těhotná nebo plánujete otěhotnět před použitím Finteply; Není známo, jak by to ovlivnilo plod. Existuje registr expozice těhotenství, který monitoruje výsledky těhotenství u žen vystavených antiepileptickým lékům (AED), jako je Fintepla během těhotenství. Není známo, zda Fintepla přejde do mateřského mléka. Před kojením se poraďte se svým lékařem.
Další informace
Naše fintepla (fenfluramin) ústní roztok CIV Vedlejší účinky Drug Center poskytuje komplexní pohled na dostupné informace o možných vedlejších účincích při užívání tohoto léku.
Nejedná se o úplný seznam vedlejších účinků a mohou dojít k dalším. Zavolejte svého lékaře, kde najdete lékařskou radu ohledně vedlejších účinků. Můžete nahlásit vedlejší účinky FDA na 1-800-FDA-1088.
Informace o drogách FDA
- Popis léku
- Indikace
- Vedlejší účinky
- Lékové interakce
- Varování
- Předávkovat
- Klinická farmakologie
- Průvodce léky
VAROVÁNÍ
Chlopní srdeční choroby a plicní arteriální hypertenze
Existuje souvislost mezi serotonergními léky s aktivitou agonisty receptoru 5-HT2B, včetně fenfluraminu (aktivní složka ve Finteple) a onemocněním chlopní srdeční a plicní arteriální hypertenze [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Hodnocení echokardiogramu jsou vyžadována dříve během a po léčbě finteplou. Výhody versus rizika zahájení nebo pokračujícího fintepla je třeba zvážit na základě zjištění Echokardiogramu [Viz Dávkování a podávání a VAROVÁNÍS AND PRECAUTIONS ].
Kvůli rizikům choroby chlopní srdeční a plicní arteriální hypertenze je k dispozici pouze prostřednictvím omezeného programu v rámci strategie hodnocení rizik a zmírnění (REM) zvané Fintepla REMS [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Popis pro Fintepla
Fintepla perorální roztok obsahuje 2,2 mg/ml fenfluraminu ekvivalentní 2,5 mg/ml hydrochloridové soli.
Hydrochlorid aktivní složky je chemicky označen jako n-ethyl-a-methyl-3- (trifluoromethyl) fenylamin hydrochlorid.
Strukturální vzorec je:
| |
Fenfluramin Hydrochlorid je bílá až bělavá krystalická pevná látka. PKA fenfluraminu je 10,2.
Fintepla je jasné bezbarvé řešení pH 5.
Fintepla obsahuje následující neaktivní složky: Kyselina cherry aroma kyselina citronová ethylparaben hydroxyethylcelulóza methylparaben draselný citrát sukralózy a vody.
Fintepla neobsahuje žádnou složku vyrobenou z obilí obsahujícího lepek (ječmen pšenice nebo žito).
Použití pro Fintepla
Fintepla je indikována pro léčbu záchvatů spojených s Dravetovým syndromem (DS) a Lennox-Gastautovým syndromem (LGS) u pacientů ve věku 2 let a starších.
Dávkování pro Fintepla
Hodnocení před zahájením Fintepla
Před zahájením léčby finteplou získejte hodnocení echokardiogramu, aby bylo možné vyhodnotit chlopní srdeční choroby a plicní arteriální hypertenzi [viz viz Hodnocení během a po podání Finteply a VAROVÁNÍS AND PRECAUTIONS ].
Informace o dávkování
Fintepla se má podávat orálně a může být užívána s jídlem nebo bez něj.
Dravetův syndrom
- Počáteční dávka a údržba u pacientů s Dravetovým syndromem je 0,1 mg/kg dvakrát denně, což může být zvýšeno týdně na základě účinnosti a snášenlivosti. Tabulka 1 poskytuje doporučený plán titrace v případě potřeby.
- Pacienti s Dravetovým syndromem, který není na doprovodu StiriPentolu, kteří tolerují Fintepla při 0,1 mg/kg dvakrát denně a vyžadují další snížení záchvatů, může těžit ze zvýšení dávky až do maximálního doporučeného dávkování údržby 0,35 mg/kg dvakrát denně (maximální denní dávka 26 mg).
- Pacienti s Dravetovým syndromem, kteří užívají souběžný ShiriPentol Plus Clobazam, kteří tolerují Fintepla při 0,1 mg/kg dvakrát denně a vyžadují další snížení záchvatů, může těžit z zvýšení dávky až do maximálního doporučeného údržby dávky 0,2 mg/kg dvakrát denně (maximální denní dosava 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [Viz 17 mg) [ Lékové interakce ].
Lennox-Gastaut Syndrom
- Počáteční počáteční dávka u pacientů se syndromem Lennox-Gastautu je 0,1 mg/kg dvakrát denně, což by mělo být zvýšeno týdně na základě snášenlivosti. Tabulka 1 poskytuje doporučený plán titrace.
- Pacienti se syndromem Lennox-Gastautu, kteří nejsou na souběžném StiriPentolu, kteří tolerují Fintepla, by měli být titrováni k doporučené dávkování údržby 0,35 mg/kg dvakrát denně (maximální denní dávka 26 mg).
- Pacienti se syndromem Lennox-Gastautu s doprovodným StiriPentolem plus Clobazamem, kteří tolerují Fintepla, by měli být titrováni k doporučené dávkování údržby 0,2 mg/kg dvakrát denně (maximální denní dávka 17 mg) [Viz viz Lékové interakce ].
Tabulka 1: Fintepla Doporučený plán titrace*
| Bez doprovodného StiriPentolu* | S souběžným ShiriPentolem Plus Clobazam | |||
| Dávkování na váze | Maximální celková denní dávka ± | Dávkování na váze | Maximální dávka ± celková denně | |
| Počáteční dávka | 0,1 mg/kg dvakrát denně | 26 mg | 0,1 mg/kg dvakrát denně | 17 mg |
| 7. den | 0,2 mg/kg dvakrát denně | 26 mg | 0,15 mg/kg dvakrát denně | 17 mg |
| Den 14 ** | 0,35 mg/kg dvakrát denně | 26 mg | 0,2 mg/kg dvakrát denně | 17 mg |
| * U pacientů, kteří nejsou na souběžném StiriPentolu, u kterého je zaručena rychlejší titrace, může být dávka zvýšena každé 4 dny. U pacientů s dávkováním syndromu DRAVET může být podle potřeby zvýšena na základě klinické odpovědi na maximální doporučenou dávkování. ** U pacientů s dávkováním syndromu Lennox-Gastautu by mělo být zvýšeno, jak je tolerováno na doporučenou dávkování údržby (tj. Den 14). ± pro maximální dávkování se souběžným použitím silných inhibitorů CYP1A2 nebo CYP2D6 u pacientů s těžkým poškozením ledvin nebo u pacientů s jaterním postižením viz viz Modifikace dávkování u pacientů se souběžným používáním silných inhibitorů CYP1A2 nebo CYP2D6 (DS a LGS) pro dávkování u pacientů se závažným poškozením ledvin (DS a LGS) pro dávkování u pacientů s mírným středním a závažným poškozením jater (DS a LG) (DS a LG) (DS a LG)) |
Modifikace dávkování u pacientů se souběžným použitím silných inhibitorů CYP1A2 nebo CYP2D6 (DS a LGS)
U pacientů se souběžným používáním Fintepla se silným inhibitorem CYP1A2 nebo CYP2D6 je doporučeno maximální celkovou denní dávku 20 mg bez doprovodu doprovodným ShiriPentolem a 17 mg se souběžným StiriPentolem plus Clobazam [Viz viz [Viz [Viz [Viz [Viz [Viz [Viz [viz Lékové interakce ].
Modifikace dávkování u pacientů s těžkým poškozením ledvin (DS a LGS)
U pacientů s těžkým poškozením ledvin (odhadovaná míra glomerulární filtrace (EGFR) 15 až 29 ml/min/1,73 m 2 ) Doporučuje se maximální celková denní dávka 20 mg bez doprovodného straši Použití v konkrétních populacích ].
Modifikace dávkování u pacientů s mírným středním a těžkým poškozením jater (DS a LGS)
Viz tabulka 2 pro úpravy dávkování a doporučení pro pacienty s poškozením jater [viz Použití v konkrétních populacích ].
Tabulka 2: Modifikace a doporučení pro dávkování Fintepla pro pacienty s bezpatickým poškozením
| Klasifikace poškození jater | Bez doprovodného StiriPentolu* | S souběžným ShiriPentolem Plus Clobazam |
| Maximální celková denní dávka | Maximální celková denní dávka | |
| Mírný (Child-Pugh A) | 20 mg | 13 mg* |
| Mírný | 20 mg | Použijte nedoporučené |
| Těžké (Child-Pugh C) | 17 mg | Použijte nedoporučené |
| * titrujte podle doporučení [viz Informace o dávkování |
Hodnocení během a po podání Finteply
Chcete -li vyhodnotit onemocnění chlopně a plicní arteriální hypertenzi, získejte hodnocení echokardiogramu každých 6 měsíců během léčby Finteplou a 3 až 6 měsíců po konečné dávce Finteply [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Pokyny pro správu
Lékárna bude poskytnuta kalibrované měřicí zařízení (buď 3 ml nebo 6 ml perorální stříkačky) a doporučuje se přesně měřit a podávat předepsanou dávku [viz viz Jak dodáno ]. A household teaspoon or tablespoon is not an adequate measuring device a should not be used.
Zlikvidujte jakýkoli nepoužitý ústní roztok Fintepla, který zůstane po 3 měsících poprvé otevření láhve nebo vyřazení po datu na láhvi, podle toho, co je dříve.
Fintepla je kompatibilní s komerčně dostupnými žaludečními a nasogastrickými krmení.
Přerušení finteply
Při přerušení finteply by měla být dávka postupně snižována. Stejně jako u všech antiepileptických léčiv by se mělo vyhnout náhlému přerušení, pokud je to možné, aby se minimalizovalo riziko zvýšené frekvence záchvatů a stavu epilepticus [viz VAROVÁNÍS AND PRECAUTIONS ].
Jak dodáno
Formy a silné stránky dávkování
Orální řešení : 2,2 mg/ml fenfluraminu jako čistá bezbarvá cherry ochucená kapalina.
Fintepla Orální roztok je čistá bezbarvá cherry ochucená kapalina obsahující 2,2 mg/ml fenfluraminu a je dodávána v bílé plastové láhvi s uzavřením odolném proti dítěti následovně:
- Karta obsahující jednu 360 ml láhev ( NDC 43376-322-36)
- Karta obsahující jednu 30 ml láhev ( NDC 43376-322-30)
Před vydáváním lékárníka vloží adaptér stisknutím láhve do výdejní láhve. Lékárna bude poskytovat 3 ml nebo 6 ml kalibrovaných injekčních injekčních stříkaček.
Skladování a manipulace
Ukládat fintepla při teplotě místnosti mezi 20 ° C až 25 ° C (68 ° F až 77 ° F); Exkurze jsou povoleny mezi 15 ° C až 30 ° C (59 ° F až 86 ° F) [viz USP kontrolovaná pokojová teplota].
Neomeďte se ani zamrzněte. Uložte láhev a stříkačku dohromady.
Zlikvidujte jakoukoli nepoužívanou část 3 měsíce po prvním otevření láhve nebo vyřazení po datu na láhvi, podle toho, co je dříve.
Procentuální snížení z výchozí hodnoty ve frekvenci záchvatů kapky
Podíl pacientů (%)
Vyrobeno pro: UCB Inc. Smyrna GA 30080. Revidováno: duben 2025.
Vedlejší účinky for Fintepla
Následující klinicky významné nežádoucí účinky jsou popsány jinde při označování:
- Chlopní srdeční choroby a plicní arteriální hypertenze [viz VAROVÁNÍS AND PRECAUTIONS ]
- Snížená chuť k jídlu a snížená hmotnost [viz VAROVÁNÍS AND PRECAUTIONS ]
- Somnolence sedace a letargie [viz VAROVÁNÍS AND PRECAUTIONS ]
- Sebevražedné chování a myšlenky [viz VAROVÁNÍS AND PRECAUTIONS ]
- Stažení antiepileptických léků [viz VAROVÁNÍS AND PRECAUTIONS ]
- Serotonův syndrom [viz VAROVÁNÍS AND PRECAUTIONS ]
- Zvýšení krevního tlaku [viz VAROVÁNÍS AND PRECAUTIONS ]
- Glaukom [viz VAROVÁNÍS AND PRECAUTIONS ]
Zkušenosti z klinických studií
Protože klinické studie se provádějí za široce proměnlivých podmínek, nežádoucí rychlosti nežádoucí reakce pozorované v klinických studiích léčiva nelze přímo porovnat s mírami v klinických studiích s jiným lékem a nemusí odrážet míru pozorované v praxi.
V kontrolovaných a nekontrolovaných studiích u pacientů s Dravetovým syndromem (DS) 341 pacientů bylo léčeno Finteplou včetně 312 pacientů léčených po dobu více než 6 měsíců 284 pacientů léčených po dobu delší než 1 rok a 138 pacientů léčených více než 2 roky.
V kontrolovaných a nekontrolovaných studiích u pacientů se syndromem Lennox-Gastautu (LGS) bylo 262 pacientů léčeno Finteplou včetně 219 pacientů léčených po dobu delší než 6 měsíců 172 pacientů léčených po dobu více než 1 rok a 127 pacientů léčených po dobu více než 2 let.
Dravetův syndrom
V placebem kontrolovaných studiích u pacientů s DS, kteří zabývali doprovodným standardem péče, bylo 122 pacientů léčeno Finteplou a 84 pacientů dostávalo placebo [viz viz Klinické studie ]. The duration of treatment in these trials was 16 weeks (Studie 1) or 17 weeks (Studie 2).
Ve studii 1 a studie 2 byl průměrný věk 9 let (rozmezí 2 až 19 let) a přibližně 46% pacientů byly ženy a 74% bílých. Všichni pacienti dostávali alespoň jeden další AED.
Ve studii 1 a studie 2 byla míra přerušení v důsledku jakékoli nežádoucí reakce 13% 0% a 7% u pacientů léčených fintepla 0,7 mg/kg/den 0,2 mg/kg/den a 0,4 mg/kg/den v kombinaci s StiriPentolem ve srovnání s 6% u pacientů na placebo. Nejčastějším nežádoucím reakcí vedoucím k přerušení u pacientů léčených jakoukoli dávkou finteply byla somnolence (3%).
Nejběžnější nežádoucí účinky, ke kterým došlo u pacientů léčených finteplou (incidence nejméně 10% a větší než placebo), byly snížené chuť k jídlu; somnolence sedace letargie; průjem; zácpa; abnormální echokardiogram; Únava malátnost astenia; Porucha ataxie rovnováhy poruchy; Krevní tlak se zvýšil; Hypersecrece slinných slin; Pyrexia; infekce horních cest dýchacích; zvracení; snížená hmotnost; podzim; status epilepticus.
Tabulka 4 uvádí nežádoucí účinky, které byly hlášeny u 5% nebo více pacientů léčených Finteplou a rychlostí vyšší než na placebu během titračních a údržbářských fází studie 1 a studie 2.
Tabulka 4: Nežádoucí účinky u 5% nebo více pacientů léčených Finteplou a Graeter než placebo v placebem kontrolovaných studiích pro Dravetový syndrom (studie 1 a 2)
| Nežádoucí reakce | Fintepla Dose Group | Kombinovaná placebo skupina (2) | ||
| Studie 1 | Studie 2 | |||
| 0,2 mg/kg/den | 0,7 mg/kg/den | 0,4 mg/kg/den (1) | ||
| N = 39 % | N = 40 % | N = 43 % | N = 84 % | |
| Snížená chuť k jídlu | 23 | 38 | 49 | 8 |
| Somnolence Sedation Lethargie | 26 | 25 | 23 | 11 |
| Abnormální echokardiogram (3) | 18 | 23 | 9 | 6 |
| Průjem | 31 | 15 | 23 | 6 |
| Zácpa | 3 | 10 | 7 | 0 |
| Únava malátnost Astenia | 15 | 10 | 30 | 5 |
| Porucha rovnováhy ataxie narušení chůze | 10 | 10 | 7 | 1 |
| Abnormální chování | 0 | 8 | 9 | 0 |
| Zvýšil se krevní tlak | 13 | 8 | 0 | 5 |
| Hypersecrece slintavých slin | 13 | 8 | 2 | 0 |
| Hypotonie | 0 | 8 | 0 | 0 |
| Vyrážka | 8 | 8 | 5 | 4 |
| Prolaktin krve se zvýšil | 0 | 5 | 0 | 0 |
| Zimnice | 0 | 5 | 2 | 0 |
| Snížená aktivita | 0 | 5 | 0 | 1 |
| Dehydratace | 0 | 5 | 0 | 0 |
| Nespavost | 0 | 5 | 5 | 2 |
| Pyrexia | 15 | 5 | 21 | 14 |
| Stereotypy | 0 | 5 | 0 | 0 |
| Infekce horních cest dýchacích | 21 | 5 | 7 | 10 |
| Zvracení | 10 | 5 | 5 | 8 |
| Hmotnost se snížila | 13 | 5 | 7 | 1 |
| Croup | 5 | 3 | 0 | 1 |
| Infekce uší | 8 | 3 | 9 | 5 |
| Gastroenteritida | 8 | 3 | 2 | 0 |
| Zvýšená srdeční frekvence | 5 | 3 | 0 | 2 |
| Podrážděnost | 0 | 3 | 9 | 2 |
| Rhinitida | 8 | 3 | 7 | 2 |
| Tremor | 3 | 3 | 9 | 0 |
| Močová inkontinence | 5 | 3 | 0 | 0 |
| Snížená glukóza krve | 0 | 0 | 9 | 1 |
| Bronchitida | 3 | 0 | 9 | 1 |
| Kontuze | 5 | 0 | 0 | 0 |
| Ekzém | 0 | 0 | 5 | 0 |
| Enuresis | 5 | 0 | 0 | 0 |
| Podzim | 10 | 0 | 0 | 4 |
| Bolest hlavy | 8 | 0 | 0 | 2 |
| Zánět hrtanu | 0 | 0 | 5 | 0 |
| Negativismus | 5 | 0 | 0 | 0 |
| Status epilepticus | 3 | 0 | 12 | 2 |
| Infekce močových cest | 5 | 0 | 5 | 0 |
| Virová infekce | 0 | 0 | 5 | 1 |
| (1) 0,4 mg/kg/den was not an intermediate dose. Patients on the 0,4 mg/kg/den dose were also taking concomitant StiriPentol Plus Clobazam which increases exposure of Fintepla. (2) Pacienti ve skupinách s placebem ze studií 1 a 2 byli sdruženi. (3) Sestával ze stopy a mírné mitrální regurgitace a stopování aortální regurgitace, které jsou považovány za fyziologickou |
Lennox-Gastaut Syndrom
V placebem kontrolované studii s pacienty s LG, kteří zabírali doprovodnou úroveň péče AED (studie 3) 176 pacientů bylo léčeno Finteplou a 87 pacientů dostávalo placebo [viz viz Klinické studie ]. The duration of treatment in this trial was 16 weeks. The mean age was 13.7 years (range 2 to 35 years) a 29% of patients were at least 18 years of age 45% of patients were female a 79% were White. All patients were receiving at least one other AED.
Míra vysazení v důsledku jakékoli nežádoucí reakce byla 6% a 5% u pacientů léčených fintepla 0,7 mg/kg/den a 0,2 mg/kg/den ve srovnání s 1% u pacientů na placebu. Nejčastější nežádoucí účinky vedoucí k přerušení u pacientů léčených jakoukoli dávkou Finteply byly záchvaty (2%) a somnolence (2%).
Běžné nežádoucí účinky, ke kterým došlo u pacientů léčených Finteplou (incidence alespoň 10% a větší než placebo), byly průjem; snížená chuť k jídlu; únava; spavost; zvracení.
Tabulka 5 uvádí nežádoucí účinky, které byly hlášeny u 5% nebo více pacientů léčených Finteplou a rychlostí vyšší než na placebu během titrační a údržby fáze studie 3.
Tabulka 5: Nežádoucí účinky u 5% nebo více pacientů léčených Finteplou a větší než placebo v placebem kontrolované studii pro syndrom Lennox Gastaut (studie 3)
| Nežádoucí reakce | Fintepla Dose Group | ||
| Studie 3 | Skupina placeba | ||
| 0,2 mg/kg/den | 0,7 mg/kg/den | ||
| N = 89 % | N = 87 % | N = 87 % | |
| Snížená chuť k jídlu | 20 | 36 | 12 |
| Únava malátnost Astenia | 14 | 24 | 16 |
| Somnolence Sedation Lethargie | 12 | 22 | 16 |
| Průjem | 11 | 13 | 5 |
| Zácpa | 6 | 9 | 6 |
| Zvracení | 14 | 8 | 6 |
| Hmotnost se snížila | 2 | 8 | 2 |
| Infekce horních cest dýchacích | 8 | 7 | 3 |
| Záchvat | 9 | 5 | 7 |
| Podrážděnost | 8 | 3 | 6 |
Echokardiografické bezpečnostní hodnocení onemocnění chlopní srdeční a plicní arteriální hypertenze
Onemocnění chlopní srdeční a plicní arteriální hypertenze byly hodnoceny v placebokontrolních a otevřených studiích prodloužení prostřednictvím echokardiografie po dobu až 3 let v délce pro 341 pacientů s DS a 263 pacientů s LGS [viz viz LGS [viz viz pacienty [viz LGS [ VAROVÁNÍS AND PRECAUTIONS ]. Screening for valvular heart disease assessed for mild or greater aortic regurgitation or moderate or greater mitral regurgitation a assessed for additional characteristics of VHD (e.g. valve thickening or restrictive valve motion).
V těchto klinických studiích dva pacienti s LG vykazovali mírnou aortální regurgitaci (AR), ale ani jeden pacient neměl žádné srdeční příznaky nebo symptomy ani důkaz o chloptických strukturálních změnách.
Žádný pacient neměl VHD. Míra mírného AR je v souladu s mírami pozorovanou v období screeningu před léčbou (3 pacienti v LGS a 1 pacienta v klinických studiích DS).
Zážitek z postmarketingu
Během použití Finteply byly identifikovány následující nežádoucí účinky. Protože tyto reakce jsou hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo vytvořit kauzální vztah k expozici léčiva.
Psychiatrické poruchy : agrese
Lékové interakce for Fintepla
Vliv jiných léků na Fintepla
StiriPentol Plus Clobazam
Společné podávání Fintepla s ShiriPentolem Plus Clobazam s nebo bez valproátu zvyšuje koncentrace plazmy fenfluraminu [viz viz Klinická farmakologie ]. If Fintepla is coadministered with StiriPentol Plus Clobazam the maximum daily dosage of Fintepla is 0,2 mg/kg dvakrát denně (maximum daily dosage of 17 mg) [see Dávkování a podávání ].
Silné induktory CYP1A2 CYP2B6 nebo CYP3A
Společné podávání Fintepla se silnými induktory CYP1A2 CYP2B6 nebo CYP3A sníží koncentrace plazmy fenfluraminu, které mohou snížit účinnost Fintepla [viz viz Klinická farmakologie ].
Doporučuje se zabránit souběžnému podávání silných induktorů CYP1A2 CYP2B6 nebo CYP3A. Je -li nutné monitorovat pacienta pro sníženou účinnost a zvážit zvýšení dávky FintePa podle potřeby monitorovat souběžné podávání silného induktoru CYP1A2 CYP2B6 nebo CYP3A; Nepřekračujte však maximální denní dávku Finteply [viz Dávkování a podávání ].
Pokud je během udržovací léčby vysazen silný induktor CYP1A2 CYP2B6 nebo CYP3A, zvažte postupné snížení dávkování finteply před zahájením induktoru [viz viz [viz viz [viz VAROVÁNÍS AND PRECAUTIONS ].
Silné inhibitory CYP1A2 nebo CYP2D6
Společné podávání Fintepla se silnými inhibitory CYP1A2 nebo CYP2D6 zvýší koncentrace plazmy fenfluraminu [viz viz Klinická farmakologie ]. If Fintepla is coadministered with strong CYP1A2 or CYP2D6 inhibitors the maximum daily dosage of Fintepla is 20 mg [see Dávkování a podávání ].
Je -li během udržovací léčby finteplou zvažte postupné zvýšení dávky fintepla na dávku doporučenou bez inhibitorů CYP1A2 nebo CYP2D6, zvažte postupné zvýšení dávkování fintepla zvažte postupné zvýšení dávky fintepla na dávku na dávku doporučené dávkování dávkování dávkování na dávku doporučené bez inhibitorů CYP1A2 nebo CYP2D6 zvažte postupné zvýšení dávky doporučené bez inhibitorů CYP1A2 nebo CYP16; Nepřekračujte však maximální denní dávku Finteply [viz Dávkování a podávání ].
Pokud je Fintepla podváděna se spiriPentolem a silným inhibitorem CYP1A2 nebo CYP2D6 nepřesahují maximální denní dávku Finteply 17 mg [viz viz Dávkování a podávání ].
Účinky antagonistů receptoru serotoninu
Cyproheptadin a silný 5-HT1A 5-HT1D 5-HT2A a 5-HT2C antagonisté receptoru serotoninu mohou snížit účinnost FintePLA. Pokud jsou cyproheptadin nebo silný 5-HT1A 5-HT1D 5-HT2A nebo 5-HT2C antagonisty serotoninu serotoninu receptoru, by měli být podávány s pacienty s Fintepla, by měly být vhodně monitorovány.
Serotonergní léky
Současné podávání fintepla a léků (např. Ssris snris tcas mao inhibitory trazodon atd.) Volně prodejné léky (např. Dextromethorphan) nebo bylinné doplňky (např. St. Johns Wort), které zvyšují serotonin) [viz viz syndrom [Viz syndrom [Viz syndrom sérotoninu [viz syndrom sérotoninu [vidět VAROVÁNÍS AND PRECAUTIONS ]. Concomitant use of Fintepla is contraindicated within 14 days of taking MAOIs. Use Fintepla with caution in patients taking other medications that increase serotonin.
Varování pro Fintepla
Zahrnuto jako součást 'OPATŘENÍ' Sekce
Opatření pro Fintepla
Chlopní srdeční choroby a plicní arteriální hypertenze
Fintepla can cause valvular heart disease (VHD) a pulmonary arterial hypertension (PAH). There is a known association between serotonergic drugs with 5-HT2B receptor agonist activity including fenfluramine (the active ingredient in Fintepla) a valvular heart disease a pulmonary arterial hypertension. Although no patients receiving Fintepla developed valvular heart disease or pulmonary arterial hypertension in clinical trials for DS a LGS of up to 3 years in duration cases of valvular heart disease a pulmonary arterial hypertension have been reported during use of Fintepla in the postmarketing setting [see Varování a Nežádoucí účinky ].
Kvůli tomuto riziku je vyžadováno monitorování srdce před zahájením léčby během léčby a po uzavření léčby fintepla. Sledování srdečního monitorování prostřednictvím echokardiogramu může identifikovat důkaz o onemocnění chlopní srdeční a plicní arteriální hypertenzi před tím, než se pacient stane symptomatickým napomáhám včasné detekci těchto stavů.
Monitorování
Před zahájením léčby musí pacienti podstoupit echokardiogram, aby vyhodnotili chlopní srdeční choroby a plicní arteriální hypertenzi.
Echokardiogramy by se měly opakovat každých 6 měsíců a jednou 3-6 měsíců po léčbě s Finteplou.
Přední lékař musí zvážit výhody versus rizika zahájení nebo pokračující léčby Finteplou, pokud je některá z následujících znaků pozorována prostřednictvím Echo:
- Valvulární abnormalita nebo nová abnormalita prostřednictvím echokardiogramu.
- VHD, jak ukazuje mírná nebo větší aortální regurgitace nebo střední nebo větší mitrální regurgitace s dalšími charakteristikami VHD (např. Zhušťování chlopně nebo restriktivní pohyb ventilu).
- PAH, jak ukazuje zvýšený tlak pravého srdce/plicní tepny (PASP> 35 mm Hg).
Fintepla is available only through a restricted program under a REMS [see Fintepla REMS Program ].
Fintepla REMS Program
Fintepla is available only through a restricted distribution program called the Fintepla REMS program because of the risk of valvular heart disease a pulmonary arterial hypertension [see Chlopní srdeční choroby a plicní arteriální hypertenze ].
Mezi pozoruhodné požadavky programu Fintepla REMS patří:
- Předepisující musí být certifikováni zápisem do programu Fintepla REMS.
- Předepsatelé musí poradit s pacientům, kteří dostávají finteplu o riziku chlopní srdeční choroby a plicní arteriální hypertenze, jak rozpoznat příznaky a příznaky chlopní srdeční choroby a plicní arteriální hypertenzi Potřeba základní linie (předběžné úpravy) a léčby srdeční léčby a srdeční léčba po finále.
- Pacienti se musí zapsat do programu REMS a splnit probíhající monitorovací požadavky [viz Chlopní srdeční choroby a plicní arteriální hypertenze ].
- Lékárna musí být certifikována zápisem do programu REMS a musí se vzdát pouze pacientů, kteří jsou oprávněni dostávat Fintepla.
- Velkoobchodníci a distributoři se musí distribuovat pouze do certifikovaných lékáren.
Další informace jsou k dispozici na adrese www.finteplarems.com nebo telefonicky na čísle 1-877-964-3649.
Snížená chuť k jídlu a snížená hmotnost
Fintepla can cause decreases in appetite a weight. In placebo-controlled studies for DS (Studie 1 a Studie 2 combined) approximately 37% of patients treated with Fintepla reported as an adverse reaction snížená chuť k jídlu a approximately 9% reported snížená hmotnost as compared to 8% a 1% respectively of patients on placebo. In the placebocontrolled study for LGS (Studie 3) approximately 28% of patients treated with Fintepla reported as an adverse reaction snížená chuť k jídlu a approximately 5% reported snížená hmotnost as compared to 15% a 2% respectively of patients on placebo [see Nežádoucí účinky ]. By the end of the controlled studies 19% (Studies 1 a 2 combined) of DS patients a 7% (Studie 3) of LGS patients treated with Fintepla had a measured decrease in weight of 7% or greater from their baseline weight compared to 2% (Studie 1 a 2) a 0% (Studie 3) of patients on placebo. This measured decrease in weight appeared to be dose-related. In the controlled studies for DS 26% of patients on Fintepla 0,7 mg/kg/den (Studie 1) 19% of patients on Fintepla 0,4 mg/kg/den in combination with stiripentol (Studie 2) a 13% of patients taking Fintepla 0,2 mg/kg/den (Studie 1) experienced at least a 7% decrease in weight from baseline. In the controlled study for LGS 9% of patients on Fintepla 0,7 mg/kg/den (Studie 3) a 6% of patients on Fintepla 0,2 mg/kg/den (Studie 3) experienced at least a 7% decrease in weight from baseline. Approximately half of the patients with LGS a most patients with DS resumed the expected measured increases in weight during the open-label extension studies. Given the frequency of these adverse reactions the growth of pediatric patients treated with Fintepla should be carefully monitored. Weight should be monitored regularly during treatment with Fintepla a dose modifications should be considered if a decrease in weight is observed.
Somnolence sedace a letargie
Fintepla can cause somnolence sedace a letargie. In controlled studies for DS (Studie 1 a Studie 2 combined) the incidence of somnolence sedace a letargie was 25% in patients treated with Fintepla compared with 11% of patients on placebo. In the controlled study for LGS (Studie 3) the incidence of somnolence sedace a letargie was 19% in patients treated with Fintepla compared with 16% of patients on placebo. In general these effects may diminish with continued treatment [see Nežádoucí účinky ].
Jiné depresivy centrálního nervového systému (CNS), včetně alkoholu, by mohly tyto účinky Fintepla zesilovat. Předepsatelé by měli sledovat pacienty z hlediska somnolence a sedace a měli by pacientům doporučit, aby řídili ani nepracují stroje, dokud nezískají dostatečné zkušenosti s Finteplou, aby posoudili, zda nepříznivě ovlivňuje jejich schopnost řídit nebo provozovat strojní zařízení.
Sebevražedné chování a myšlenky
Antiepileptická léčiva (AED) včetně Fintepla zvyšují riziko sebevražedných myšlenek nebo chování u pacientů užívajících tyto léky za jakoukoli indikaci. Pacienti léčeni AED pro jakoukoli indikaci by měli být sledováni pro vznik nebo zhoršení sebevražedných myšlenek nebo chování deprese nebo jakékoli neobvyklé změny v náladě nebo chování.
Společené analýzy 199 placebem kontrolovaných klinických studií (mono- a pomocní terapie) 11 různých AED, která nezahrnovala Fintepla, ukázaly, že pacienti randomizovaní k jednomu z AED měli přibližně dvojnásobek rizika (upravené relativní riziko 1,8 95% CI: 1,2 2.7) sebevražedného myšlení nebo chování, které byly náhodné na placebo. V těchto studiích, které měly střední dobu léčby po 12 týdnech, byla odhadovaná míra sebevražedného chování nebo myšlenky u 27863 pacientů léčených AED o 0,43% ve srovnání s 0,24% u 16029 placebem ošetřených pacientů, kteří představují přibližně jeden případ sebevražedného myšlení nebo chování u každých 530 pacientů. U pacientů léčených léčivem byly čtyři sebevraždy ve studiích a u pacientů ošetřených placebem, ale počet je příliš malý na to, aby umožnil jakýkoli závěr o drogovém účinku na sebevraždu.
Zvýšené riziko sebevražedných myšlenek nebo chování s AED bylo pozorováno již 1 týden po zahájení léčby léky AED a přetrvávalo po celou dobu hodnocené léčby. Protože většina studií zahrnutých do analýzy nepřesahovala více než 24 týdnů, nebylo možné posoudit riziko sebevražedných myšlenek nebo chování po 24 týdnech.
Riziko sebevražedných myšlenek nebo chování bylo obecně konzistentní mezi drogami v analyzovaných datech. Zjištění zvýšeného rizika u AED různých mechanismů účinku a v celé řadě indikací naznačuje, že riziko se vztahuje na všechna AED používaná pro jakoukoli indikaci. Riziko se v analyzovaných klinických studiích podstatně nelišilo podle věku (5-100 let). Tabulka 3 ukazuje absolutní a relativní riziko podle indikací pro všechny hodnocené AED.
Tabulka 3: Riziko sebevražedných myšlenek nebo chování indikací antiepileptických léků ve sdružené analýze
| Indikace | Pacienti s placebem s událostmi na 1000 pacientů | Pacienti s drogami s událostmi na 1000 pacientů | Relativní riziko: Výskyt událostí u pacientů s drogami/ incidence u pacientů s placebem | Rozdíl rizika: Další pacienti s drogami s příhodou na 1000 pacientů |
| Epilepsie | 1.0 | 3.4 | 3.5 | 2.4 |
| Psychiatric | 5.7 | 8.5 | 1.5 | 2.9 |
| Ostatní | 1.0 | 1.8 | 1.9 | 0.9 |
| Celkový | 2.4 | 4.3 | 1.8 | 1.9 |
Relativní riziko sebevražedných myšlenek nebo chování bylo vyšší v klinických studiích u pacientů s epilepsií než v klinických studiích u pacientů s psychiatrickými nebo jinými podmínkami, ale absolutní rozdíly v riziku byly podobné pro epilepsii a psychiatrické indikace.
Každý, kdo zvažuje předepisování Fintepla nebo jakéhokoli jiného AED, musí vyvážit riziko sebevražedných myšlenek nebo chování s rizikem neléčeného onemocnění. Epilepsie a mnoho dalších nemocí, pro které jsou předepisovány AED, jsou samy spojeny s morbiditou a úmrtností a zvýšeným rizikem sebevražedných myšlenek a chování. Pokud by se během léčby objevily sebevražedné myšlenky a chování, zvažte, zda vznik těchto příznaků u jakéhokoli daného pacienta může souviset s léčenou nemocí.
Stažení antiepileptických léků
Stejně jako u většiny AED Fintepla by měla být obecně stažena postupně kvůli riziku zvýšené frekvence záchvatů a stavu epilepticus. Je -li nutné odstoupit z důvodu vážné nežádoucí reakce, lze vzít v úvahu rychlé přerušení.
Serotonův syndrom
Syndrom serotoninu Potenciálně život ohrožující může dojít u Fintepla, zejména se souběžným podáváním fintepla s jinými serotonergními léky, včetně, ale nejen, selektivní selektivní inhibitory selektivního serotoninu-norepinefrinu inhibitorů (SSRIS) inhibitory (SSSRI) (SSRI) (SSRIS) (SSRIS) (SSRI) antidepresiva (TCAS) Léky dietní stravy Bupropion Triptans (např. Tryptofan), které narušují metabolismus serotoninu (včetně inhibitorů monoamin oxidázy [Maois], které jsou kontraindikovány s Finteplou [viz viz Kontraindikace ] Dextromethorphan Lithium tramadol a antipsychotika se serotonergní agonistickou aktivitou. Pacienti by měli být monitorováni z hlediska vzniku příznaků a symptomů serotoninového syndromu, které zahrnují změny duševního stavu (např. Agitační halucinace kóma) autonomní nestabilita (např. Tachykardie labilní krevní tlak hypertermie) neuromuskulární příznaky (inkorsitace hyperreflexie) a/nebo gastrointestinární příznaky). Pokud je podezření na serotoninový syndrom, měla by být léčba finteplou okamžitě zastavena a měla by být zahájena symptomatická léčba.
Zvýšení krevního tlaku
Fintepla can cause an increase in blood pressure [see Nežádoucí účinky ]. Rare cases of significant elevation in blood pressure including hypertensive crisis has been reported in adult patients treated with fenfluramine including patients without a history of hypertension. In clinical trials of up to 3 years in duration no pediatric or adult patient receiving Fintepla developed a hypertensive crisis. Monitor blood pressure in patients treated with Fintepla.
Glaukom
Fenfluramin může způsobit mydriasi a může srážet uzavření úhlu glaukom . Zvažte přerušení léčby finteplou u pacientů s akutním snížením zrakové ostrosti nebo oční bolesti.
Informace o poradenství pro pacienta
Doporučujte pacientovi, aby si přečetl značení pacienta schváleného FDA ( Průvodce léky a Instructions for Use ).
Informace o správě
Poraďte se s pacienty, kterým je předepsán Fintepla, aby používali ústní dávkovací stříkačky poskytované lékárnou [viz Dávkování a podávání a Pokyny pro použití ]. Instruct patients to discard any unused Fintepla 3 months after first opening the bottle or if the discard after date on the dispensing bottle has passed whichever is sooner [see Jak dodáno ].
Chlopní srdeční choroby a plicní arteriální hypertenze
Poraďte se pacientům, že monitorování srdečního řízení musí být prováděno pomocí echokardiografie pro sledování závažných změn srdeční chlopně nebo vysokého krevního tlaku v tepnách plic [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Fintepla REMS Program
Fintepla is available only through a restricted program called the Fintepla REMS program [see VAROVÁNÍS AND PRECAUTIONS ]. Inform the patient of the following notable requirements:
- Pacienti se musí přihlásit do programu a dodržovat probíhající požadavky na sledování echokardiogramu [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Fintepla is only prescribed by certified health care providers a only dispensed from certified pharmacies participating in the program. Therefore provide patients with the telephone number a website for information on how to obtain the product [see VAROVÁNÍS AND PRECAUTIONS ].
Snížená chuť k jídlu a snížená hmotnost
Poraďte se s pacienty, že během léčby finteplou je častá snížená chuť k jídlu, což může způsobit snížení hmotnosti [viz VAROVÁNÍS AND PRECAUTIONS ].
Somnolence sedace a letargie
Informujte pacienty, že fintepla může způsobit somnolenční sedaci a letargii. Upozorněte pacienti o provozních nebezpečných strojích včetně motorových vozidel, dokud si nejsou přiměřeně jisti, že Fintepla na ně nepříznivě neovlivňuje (např. Narušení úsudku nebo motorických dovedností) [Viz VAROVÁNÍS AND PRECAUTIONS ].
Sebevražedné myšlení a chování
Poraden pacientům jejich pečovatelům a jejich rodinám, že antiepileptická léčiva mohou zvýšit riziko sebevražedných myšlenek a chování a doporučit jim, aby byli ostražití pro vznik nebo zhoršení příznaků deprese jakékoli neobvyklé změny v náladě nebo chování nebo vznik sebevražedných myšlenek nebo myšlenek na sebepoškozování. Pokynujte pečovateli a rodinám pacientů, aby okamžitě nahlásili chování poskytovatelů zdravotní péče [viz [viz VAROVÁNÍS AND PRECAUTIONS ].
Stažení antiepileptických léků (AEDs)
Doporučujte pacientům, aby nepřerušili používání Finteply bez konzultace s poskytovatelem zdravotní péče. Fintepla by se měla normálně postupně stahovat, aby se snížil potenciál pro zvýšenou frekvenci záchvatu a status epilepticus [viz Dávkování a podávání a VAROVÁNÍS AND PRECAUTIONS ].
Serotonův syndrom
Informujte pacienty o riziku serotoninového syndromu, který může být život ohrožující. Poraďte pacientům o příznacích a příznacích syndromu serotoninu a že určité volně prodejné léky a bylinné doplňky mohou toto riziko zvýšit [Viz [Viz VAROVÁNÍS AND PRECAUTIONS ].
Zvýšení krevního tlaku
Informovat pacienty, že Fintepla může způsobit zvýšení krevního tlaku [viz VAROVÁNÍS AND PRECAUTIONS ].
Glaukom
Informujte pacienty, že Fintepla může způsobit mydriasi a může uvíznout glaukom úhlu.
Poskytněte pacientům, aby kontaktovali svého poskytovatele zdravotní péče, pokud mají nějaké akutní snížení zrakové ostrosti nebo oční bolesti [viz VAROVÁNÍS AND PRECAUTIONS ].
Registr těhotenství
Poraďte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud otěhotní nebo mají v úmyslu otěhotnět během terapie Fintepla. Povzbuďte ženy, které berou Finteplu, aby se přihlásily do severoamerického antiepileptického léčiva (NAAED) těhotenství, pokud otěhotní.
Tento registr shromažďuje informace o bezpečnosti antiepileptických léků během těhotenství [viz Použití v konkrétních populacích ].
Neklinická toxikologie
Zhodnocení mutageneze karcinogeneze plodnosti
Karcinogeneze
Perorální podávání fenfluraminu na myši TG.RASH2 (0 4,3 13,0 34,6 nebo 51,8 mg/kg/den) po dobu 26 týdnů a na samci a samice potkanů (0 0,9 2,2 nebo 6,9 mg/kg/den) po dobu 89 a 97 týdnů nevedlo k žádnému důkazům u obou druhů u obou druhů. U potkanů se plazmatické expozice (AUC) fenfluraminu a norfenfluraminu (hlavní metabolit) při nejvyšší testované dávce byly přibližně 5 a 11krát u lidí při maximální doporučené lidské dávce (MRHD) 26 mg/den.
Mutageneze
Fenfluramin byl negativní v in vitro test bakteriální mutace (Ames) a AN nadarmo Mikronukleus a test komety u potkanů.
Poškození plodnosti
Perorální podávání fenfluraminu (0 3,0 6,9 nebo 17,3 mg/kg/den) na samce a samice potkanů před a během páření a pokračování u žen do 7. dne těhotenství vedlo ke snížení plodnosti a zvyšováním spermatu a epideálního vysávání epididy a epididy vedla k nejvyššímu kmenům a impozantním bojovníkem a impozantním kmen. a zvýšená embryolettalita ve střední a vysoké dávce. Tyto dávky byly spojeny s rodičovskou toxicitou. Dávky bez efektu pro nepříznivé účinky na plodnost a reprodukční výkon u potkanů (NULL,9 a 3,0 mg/kg/den u mužů a žen byly spojeny s plazmatickými fenfluraminovými expozicemi (AUC) přibližně 3 a Norfenfluraminové expozice při přibližně 5 a 3krát u lidí v MRHD.
Použití v konkrétních populacích
Těhotenství
Těhotenství Exposure Registry
Existuje registr expozice těhotenství, který monitoruje výsledky těhotenství u žen vystavených antiepileptickým lékům (AED), jako je Fintepla během těhotenství. Povzbuďte ženy, které během těhotenství berou Finteplu, aby se přihlásily do registru těhotenství v severoamerickém antiepileptickém léčivi (Naaed), voláním bezplatného čísla 1-888-233-2334 nebo návštěvou https://www.aedpregnancyregistry.org.
Shrnutí rizika
U těhotných žen neexistují žádné údaje o použití fintepla. Dostupné údaje z epidemiologických studií s fenfluraminem nebo dexfenfluraminem nejsou dostatečné k vyhodnocení rizika potrat vrozených vad nebo jiných nežádoucích matek nebo fetálních výsledků. Fintepla může způsobit sníženou chuť k jídlu a sníženou hmotnost [viz VAROVÁNÍS AND PRECAUTIONS ]; Monitorujte přiměřený přírůstek hmotnosti během těhotenství. Ve studiích na zvířatech podávání fenfluraminu v celé organogenezi (potkana a králíka) nebo během těhotenství a laktace (potkana) vyústila v nepříznivé účinky na vývoj (malformace plodu embryfetální a potomky a zhoršování růstu) v přítomnosti toxicity mateřského mateřského mateřského plazmy (viz hlavní aktivní metabolite (viz hlavní aktivní metabolita (viz hlavní aktivní metabolin (viz jeho aktivní metabolin (viz jeho aktivní metabolin (viz hlavní aktivní metabolita (viz hlavní aktivní metabolin (viz hlavní metabolin (viz hlavní aktivní metabolin (viz hlavní aktivní metabolin (viz hlavní aktivní metabolinu (viz hlavní aktivní metabolin a jeho aktivní metabolinu (viz. Data ).
Odhadované riziko na pozadí hlavních vrozených vad a potratu pro uvedenou populaci není známo. Všechna těhotenství mají riziko na pozadí vrozená vada ztráta nebo jiné nepříznivé výsledky. V americké obecné populaci je odhadované riziko na pozadí hlavních vrozených vad a potratu u klinicky uznávaných těhotenství 2 až 4% a 15 až 20%.
Data
Údaje o zvířatech
Perorální podávání fenfluraminu (0 4,5 8,6 nebo 34,6 mg/kg/den) těhotným potkanům během organogeneze vedlo ke snížení tělesné hmotnosti plodu a výrazné zvýšení fetálních malformací (vnější viscerální a kosterní) při nejvyšší testované dávce. Při dávce bez efektu (NULL,6 mg/kg/den) pro nepříznivé účinky na vývoj embryfetálního vývoje u potkanů mateřských plazmatických expozic (AUC) fenfluraminu a norfenfluraminu (hlavní metabolit) byly přibližně 2 a 5krát u lidí při maximálním doporučeném lidském dávce (MRHD) 26 mg/den.
Perorální podávání fenfluraminu (0 4,3 8,6 13,0 mg/kg/den) těhotným králíkům v celé organogenezi vedlo ke zvýšené úmrtnosti na embryfetální ve všech dávkách a zvýšení malformací plodu (vnější a kosterní) při nejvyšší testované dávce, která byla spojena s toxickou mateřskou mateřskou. Nebyla identifikována dávka bez nepřítomnosti pro nepříznivé účinky na vývoj embryfetálního vývoje u králíků. Při nejnižší dávce testované u králíků (NULL,3 mg/kg/den) byly expozice plazmy mateřského fenfluraminu a norfenfluraminu nižší než u lidí na MRHD.
Orální podávání fenfluraminu (0 4,3 86 nebo 34,6 mg/kg/den) pro samice potkanů během těhotenství a laktace vedlo k výraznému nárůstu mrtvých štěňat a novorozeneckých potomků úmrtí na nejvyšší testované dávce a odkládanému růstu a vývoji reklexu během předchůdců ve všech dobách za všechna doba. Přírůstek tělesné hmotnosti matky byl snížen při všech dávkách během těhotenství a při dvou nejvyšších dávkách během laktace. Nebyla stanovena dávka bez účinků pro nepříznivé účinky na pre- a postnatální vývoj u potkanů. Při nejnižší dávce testované u potkanů (NULL,3 mg/kg/den) byly expozice mateřské plazmy fenfluraminu a norfenfluraminu přibližně 0,5 a 3krát u lidí na MRHD.
Laktace
Shrnutí rizika
Neexistují žádné údaje o přítomnosti fenfluraminu nebo jeho metabolitů v lidském mléce účinky na kojené dítě nebo účinky na produkci mléka.
Vývojové a zdravotní přínosy kojení by měly být zváženy spolu s klinickými potřebami matek Fintepla a případnými nepříznivými účinky na kojené dítě z Finteply nebo ze základního mateřského stavu.
Ženy a muži reprodukčního potenciálu
Neplodnost
Ve studiích na zvířatech vedlo ústní podávání fenfluraminu k nepříznivým reprodukčním účinkům u mužů a žen při klinicky relevantních dávkách v přítomnosti rodičovské toxicity [viz viz Neklinická toxikologie ].
Dětské použití
U pacientů a starších a starších byla stanovena bezpečnost a účinnost Fintepla pro léčbu záchvatů spojených s DS a LGS.
Použití FintePLA pro léčbu záchvatů spojených s DS u pacientů ve věku 2 let a starších je podporováno dvěma randomizovanými dvojitě zaslepenými placebem kontrolovanými studiemi u 202 pacientů ve věku 2 až 18 let. Použití Fintepla pro léčbu záchvatů spojených s LGS je podporováno randomizovanou dvojitě zaslepenou placebem kontrolovanou studií u 263 pacientů ve věku 2 až 35 let včetně 187 pacientů méně než 18 let [viz viz Varování VAROVÁNÍS AND PRECAUTIONS Nežádoucí účinky a Klinické studie ].
Fintepla can cause decreases in appetite a weight. The growth of pediatric patients treated with Fintepla should be carefully monitored.
Bezpečnost a účinnost u pacientů mladších 2 let nebyla stanovena.
Údaje o mladistvých zvířatech
Perorální podávání fenfluraminu (0 3,0 78 nebo 17,3 mg/kg/den) pro mladé potkany po dobu 10 týdnů začínajících postnatálním dnem 7 vedlo ke snížení tělesné hmotnosti a změn neurobehaviorálních (snížená lokomotorická aktivita a deficity učení a paměti) ve všech testovaných dávkách. Neurobehaviorální účinky přetrvávaly po přerušení dávkování. Velikost kosti byla snížena ve středních a vysokých dávkách; Velikost mozku byla snížena při nejvyšší dávce. Pro tyto koncové body bylo pozorováno částečné nebo úplné zotavení. Nebyla identifikována dávka bez účinku pro postnatální vývojovou toxicitu. Nejnižší testovaná dávka (NULL,0 mg/kg/den) byla spojena s plazmatickými expozicemi fenfluraminu (AUC) menší než u lidí při maximální doporučené dávce lidské (MRHD) 26 mg/den a norffenfluraminem (metabolit) expozice (AUC) (AUC) přibližně 2krát u MRHD.
Geriatrické použití
Klinické studie FintePLA pro léčbu DS nebo LGS nezahrnovaly pacienty ve věku 65 let a více, aby určily, zda reagují odlišně od mladších pacientů. Obecně by měl být výběr dávky pro staršího pacienta opatrný, obvykle začínající na dolním konci rozsahu dávkování, což odráží větší frekvenci snížené funkce ledvin nebo srdeční jater a souběžné onemocnění nebo jiné léčivé terapie.
k čemu se používá terazosin HCl
Poškození ledvin
U pacientů s odhadovanou mírou glomerulární filtrace (EGFR) 15 až 29 ml/min/1,73 m 2 Nepřekračujte maximální denní dávku Finteply 20 mg. U pacientů s EGFR 15 až 29 ml/min/1,73 m 2 a concomitant stiripentol use do not exceed the maximum daily dosage of Fintepla of 17 mg [see Dávkování a podávání a Klinická farmakologie ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 .
Poškození jater
Kombinované molární expozice fenfluraminu a norfenfluraminu byly zvýšeny u subjektů s různým stupněm poškození jater (dítě-pugh třída A B a C), což u těchto pacientů vyžaduje úpravu dávky [viz viz [viz dávkování Dávkování a podávání a Klinická farmakologie ].
Informace o předávkování pro Fintepla
Předávkování nebylo pozorováno v programu klinického hodnocení Fintepla. Předávkování fenfluraminu však byla ve vyšších dávkách hlášena aktivní složka ve Finteple než v programu klinického hodnocení. Některé případy byly fatální. Mezi události hlášené po předávkování patří Mydriasis Tachycardia Flushing Tremors/Twitching/Svalsm Spasms Agitation/Neklid/úzkost zvýšila svalový tón/přísnost/opisthotonos respirační tísně nebo selhání a záchvaty. Ve většině fatálních předávkování byly hlášeny zástavy záchvatů a kardiorespirační zatčení.
Neexistuje žádný specifický protijed k předávkování reakce Fintepla. V případě, že by měla být použita standardní lékařská praxe předávkování pro léčbu předávkování drog. Měla by být zajištěna dostatečná okysličení a ventilace dýchacích cest; Doporučuje se monitorování srdečního rytmu a vitálního měření znaků. Aktualizované informace o řízení předávkování s Finteplou by mělo být kontaktováno certifikované středisko pro kontrolu jedu.
Kontraindikace pro Fintepla
Fintepla is contraindicated in patients with:
- Hypersenzitivita na fenfluramin nebo některý z pomocných látek ve Finteple [viz POPIS ]
- Současné použití nebo do 14 dnů od podávání inhibitorů monoamin oxidázy z důvodu zvýšeného rizika syndromu serotoninu [viz viz VAROVÁNÍS AND PRECAUTIONS ]
Klinická farmakologie for Fintepla
Mechanismus působení
Přesný mechanismus, kterým fenfluramin vyvíjí své terapeutické účinky při léčbě záchvatů spojených s Dravetovým syndromem a syndromem Lennox-Gastaut, není znám. Fenfluramin a metabolit norfenfluramin vykazují agonistickou aktivitu v receptorech 5-HT2 serotoninu. Existuje souvislost mezi serotonergními léky s aktivitou agonisty receptoru 5-HT2B, včetně fenfluraminu a norfenfluraminu a chalvulární srdeční choroby a plicní arteriální hypertenze.
Farmakodynamika
Srdeční elektrofyziologie
V dávce čtyřikrát maximální doporučené dávkové fintepla neprodloužilo QT interval, když byl testován v dospělé populaci.
Farmakokinetika
Farmakokinetika fenfluraminu a norfenfluraminu byla studována u zdravých subjektů u pediatrických pacientů s DS a u pediatrických a dospělých pacientů s LGS. Systémová expozice v ustáleném stavu (CMAX a AUC) fenfluraminu byla o něco větší než dávka úměrná v rozmezí dávky 13 až 51,8 mg fenfluraminu dvakrát denně (tj. 1 až 4krát maximální doporučená dávka). U pediatrických pacientů s DS, kteří dostávali fintepla 0,7 mg/kg/den až do celkové denní dávky 26 mg fenfluraminu, geometrický průměrný ustálenou fenfluramin (koeficient variace) byl 68,0 (41%) Ng/ml a AUC0-24H) NG/ML a AUC0-24H.
Vstřebávání
Fenfluramin má čas na maximální plazmatickou koncentraci (TMAX) 3 až 5 hodin v ustáleném stavu. Absolutní biologická dostupnost fenfluraminu je přibližně 68-74%. Nebyl vliv na jídlo na farmakokinetiku fenfluraminu nebo norfenfluraminu.
Rozdělení
Geometrický průměr (CV%) Zjevný objem distribuce (VZ/F) fenfluraminu je 11,9 (NULL,5%) L/kg po perorálním podávání Fintepla u zdravých subjektů. Fenfluramin je 50% vázán na lidské plazmatické proteiny in vitro a binding is independent of drug concentrations.
Odstranění
Eliminační poločas fenfluraminu byl 20 hodin a geometrický průměr (CV%) clearance (CL/F) byl 24,8 (29%) l/h po perorálním podávání Fintepla u zdravých subjektů.
Metabolismus
Více než 75% fenfluraminu je metabolizováno na norfenfluramin před eliminací primárně CYP1A2 CYP2B6 a CYP2D6. Další enzymy CYP zapojené do menšího rozsahu jsou CYP2C9 CYP2C19 a CYP3A4/5. Jak Fenfluramin, tak norfenfluramin jsou farmakologicky aktivní. Norfenfluramin je dále deaminován a oxidován za vzniku neaktivních metabolitů.
Vylučování
Většina perorálně podávané dávky fenfluraminu (větší než 90%) se vylučuje v moči jako fenfluramin norfenfluramin nebo jiné metabolity s fenfluraminem a norfenfluraminem, který účtuje méně než 25% z celkového počtu; Méně než 5% se nachází ve stolici.
Konkrétní populace
Účinek věku (rozmezí: 2 až 50 let) Pohlaví a rasa neměly klinicky smysluplný účinek na farmakokinetiku fenfluraminu.
Pacienti s poškozením ledvin
Ve specializované klinické studii porovnávající farmakokinetiku jedné dávky 0,35 mg/kg fintepla u subjektů s těžkým poškozením ledvin (EGFR <30 mL/min/1.73m 2 stanoveno MDRD) a odpovídající zdravé dobrovolníky Cmax a AUC0-inf fenfluraminu se zvýšily o 20% a 88% a CMAX a AUC0-inf norfenfluraminu se zvýšily o 13% a 21% u subjektů s těžkým snížením ledvin [viz viz [viz [viz Použití v konkrétních populacích ].
Fintepla has not been studied in patients with eGFR <15 mL/min/1.73m 2 (určeno MDRD). Není známo, zda je fenfluramin nebo norfenfluramin dialyzovatelný.
Pacienti s poškozením jater
Ve studii porovnávající farmakokinetiku jediné dávky 0,35 mg/kg fintepla u subjektů s mírným středním nebo závažným jaterním poškozením (dítě-pugh třída A B nebo c) a subjekty s normální játra AUC0-T fenfluraminu se zvýšila o 95% 113% a u subjektů a nevýrazně nepativní. CMAX fenfluraminu se zvýšil o 19% 16% a 29% u subjektů s mírným středním a těžkým poškozením jater. AUC0-T norfenfluraminu se zvýšila o 18% v mírném poškození jater 4% při mírném poškození jater a snížila se o 11% při těžkém poškození jater. CMAX norfenfluraminu se snížil o 21% 36% a 45% u subjektů s mírným středním a těžkým jaterním poškozením. Kombinovaný molární AUC0-T fenfluraminu a norfenfluraminu se zvýšil o 55% 56% a 82% u subjektů s mírným středním a těžkým jaterním poškozením. Kombinovaný molární CMAX fenfluraminu a norfenfluraminu se zvýšil o 7,5% 1,3% a 8% u subjektů s mírným středním a těžkým jaterním poškozením. Maximální denní dávka Finteply by měla být snížena u pacientů s mírným poškozením jater s/bez ShiriPentolu plus Clobazam. Maximální denní dávka Finteply by měla být snížena u pacientů se středním nebo těžkým poškozením jater bez ShiriPentolu plus clobazam [viz viz Dávkování a podávání a Použití v konkrétních populacích ].
Studie interakce léčiva
Klinické studie
Účinek jedné dávky kombinace ShiriPentol Clobazam a valproové kyseliny
Soutěžená sjezdovka s jedinou dávkou Fintepla s jedinou dávkou StiriPentol Clobazam a kyseliny valproové u zdravých dobrovolníků zvýšila AUC0-inf fenfenframinu o 42% a snížila CMAX o 18% a snížila AUC0-72 hodin o 42% a CMAX o 42% a CMAX o 42% a CMAX o 42% a CMAX o 42%. spravováno samo.
Účinek ustáleného stavu ShiriPentol Plus Clobazam s valproátem nebo bez něj
Fenfluramin Pharmakokinetická data byla shromážděna od pacientů po obdržení více fenfluraminových správ ve studii 1 a studie 2. Populační farmakokinetické modelování a simulace byly použity k posouzení účinku StiriPentolu plus clobazam s nebo bez valproátu na fenfluraminové farmakokinetice. Účinek StiriPentol Plus Clobazam s nebo bez valproátu na farmakokinetiku fenfluraminu je větší, když je Fintepla v ustáleném stavu než pro první dávku Finteply. V ustáleném stavu v populaci pacientů se souběžně podává 0,1 mg/kg dvakrát denně (NULL,2 mg/kg/den) maximálně 17 mg/den fintepla s ShiriPentolem plus clobazam s nebo bez valproátu nebo bez valproátu, ve srovnání s auc0-24, a 38% auc0-24, ve srovnání s 0,24, ve srovnání s auc0-24, ve srovnání s auc0-24, ve srovnání s auc0-24, a o 38% auc0-24, ve srovnání s 0,2 auc0-24. Mg/kg/den maximálně 26 mg/den fintepla dávka podávaná samostatně [viz Dávkování a podávání a Lékové interakce ].
Účinek kanabidiolu v ustáleném stavu
Souběžné podávání jedné dávky 0,35 mg/kg fintepla s opakovanými dávkami kanabidiolu zvýšilo AUC0-inf fenfluraminu o 59% a CMAX se ve srovnání s oproti opravné hodnotě o 33% ve srovnání s oproti fintole. Neočekává se, že tato interakce bude klinicky významná.
Účinek silných inhibitorů CYP1A2 nebo CYP2D6
Soutěžená dávka 1 0,35 mg/kg fintepla s fluvoxaminem (silný inhibitor CYP1A2) v ustáleném stavu (50 mg jednou denně) u zdravých dobrovolníků zvýšila Auc0-inf fenfluraminu o 102% a CMAX o 22% a o 22% o 22% zvýšila o 22% o 22% a o 22% o 22% o 22% a o 22% o 22% a o 22% o 22% a o 22% o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a o 22% a CMAX o 22% a CMAX o 22%. Fintepla spravováno samostatně [viz Lékové interakce ].
Soutěžená dávka 1 0,35 mg/kg fintepla s paroxetinem (silný inhibitor CYP2D6) v ustáleném stavu (30 mg jednou denně) u zdravých dobrovolníků zvýšila AUC0-inf fenfluraminu o 81% a CMAX o 13% a porovnával Cmax o 29% o 29% o 29% o 29% o 29% o 29% o 29% a Cmax o 29% o 29% a CMAX o 13% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29% a CMAX o 29%. spravováno samostatně [viz Lékové interakce ].
Vliv silných induktorů CYP1A2 CYP2B6 nebo CYP3A
Soutěžená sjednocení jedné 0,35 mg/kg dávky fintepla s rifampinem (CYP1A2 CYP2B6 a CYP3A Inducent) v ustáleném stavu (600 mg jednou denně) u zdravých dobrovolníků a zvýšila AUC0-inf fenfluraminu o 58% a CMAX o 58% snížila o 58% a CMAX o 58% se zvýšila o 58% a CMAX o 58% a CMAX o 58% a CMAX o 58% a CMAX o 58% a CMAX o 58% a CMAX o 58% a CMAX o 58% a CMAX o 58% a zvýšil AUC. CMAX NORFENFURURAMINE o 13% ve srovnání s Finteplou spravovaným samostatně [viz Lékové interakce ].
Vliv Finteply na jiné drogy
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination did not affect the pharmacokinetics of stiripentol nor the pharmacokinetics of clobazam or its N.desmethyl-metabolite norclobazam nor the pharmacokinetics of valproic acid as compared to the stiripentol Samotná kombinace kyseliny Clobazam a kyseliny valproové. Společná podávání jediné 0,35 mg/kg dávky finteply s opakovanými dávkami kanabidiolu neovlivnilo farmakokinetiku kanabidiolu ve srovnání se samotným kanabidiolem.
Studie in vitro
Fenfluramin je primárně metabolizován CYP1A2 CYP2B6 a CYP2D6 in vitro . Další enzymy CYP zapojené do menšího rozsahu jsou CYP2C9 CYP2C19 a CYP3A4/5.
Vliv fenfluraminu a norfenfluraminu na substráty CYP: Fenfluramin a Norfenfluramin nejsou inhibitory ani induktory CYP1A2 CYP2B6 CYP2C8 CYP2C19 CYP2D6 nebo CYP3A4 nebo CYP3A4 nebo CYP3A4.
Vliv transportérů na fenfluramin a norfenfluramin: fenfluramin a norfenfluramin nejsou substráty transportérů P-G BCRP OAT3 Oct2 nebo MATE2-K.
Účinek FintePLA na transportéry: Fenfluramin a norfenfluramin nejsou inhibitory P-gp BCRP OAT1B1 OATP1B3 OAT1 OAT3 Oct2 MATE1 nebo MATE2-K Transportéry.
Klinické studie
Dravetův syndrom
Účinnost FintePLA pro léčbu záchvatů spojených s DS u pacientů ve věku 2 let a starších byla stanovena ve dvou randomizovaných dvojitě zaslepených placebem kontrolovaných studiích u pacientů ve věku 2 až 18 let.
Studie 1 (N=117) compared a 0,7 mg/kg/den a a 0,2 mg/kg/den dose of Fintepla with placebo in patients who were not receiving stiripentol (NCT02682927 a NCT02826863).
Studie 2 (N=85) compared a 0,4 mg/kg/den dose of Fintepla with placebo in patients who were receiving stiripentol a either clobazam valproate or both (NCT02926898). In both studies patients had a clinical diagnosis of DS a were inadequately controlled on at least one AED or other antiseizure treatment including vagal nerve stimulation or a ketogenic diet. Both trials had a 6-week baseline period during which patients were required to have a minimum of 6 convulsive seizures while on stable AED therapy. Convulsive seizures included tonic clonic generalized tonic-clonic tonic-atonic secondarily generalized tonic-clonic hemiclonic a focal with observable motor signs. The baseline period was followed by raomization into a 2- week (Studie 1) or 3-week (Studie 2) titration period a a subsequent 12-week maintenance period where the dose of Fintepla remained stable.
Ve studii 1 98% pacientů užívalo 1 a 4 souběžné AED. Nejčastěji používanými souběžnými AED (u nejméně 25%pacientů) byly valproát (61%) Clobazam (59%) a topiramát (25%). Ve studii 2 100% pacientů užívalo 2 až 4 souběžné AED. Nejčastěji používanými souběžnými AED (u nejméně 25%pacientů) byly StiriPentol (100%) Clobazam (94%) a valproát (89%).
Primárním koncovým bodem účinnosti v obou studiích byla změna oproti základní linii ve frekvenci křečových záchvatů za 28 dní během kombinovaného 14týdenního (studie 1) nebo 15týdenního období titrace a udržování (tj. Doba léčby). Rovněž byl posouzen střední nejdelší interval mezi křečovými záchvaty.
Ve studii 1 a studie 2 byla snížení frekvence křečového záchvatu za 28 dní statisticky větší pro všechny dávkové skupiny Fintepla ve srovnání s placebem (tabulka 6). Snížení křečových záchvatů bylo pozorováno do 3 až 4 týdnů od startu Fintepla a účinek zůstal obecně konzistentní během 14- nebo 15týdenního ošetření.
Tabulka 6: Změna frekvence křečového záchvatu během lůžkového období léčebného období s Dravetovým syndromem (studie 1 a studie 2)
| Frekvence křečového záchvatu (za 28 dní) | Placebo | Fintepla 0,2 mg/kg/den | Fintepla 0,7 mg/kg/den | Fintepla 0,4 mg/kg/den |
| Studie 1 | N = 39 | N = 38 | N = 40 | Na |
| Medián výchozího období | 29.4 | 18.1 | 18.7 | Na |
| % Rozdíl ve vztahu k placebu* | -31,7% | -70,0% | Na | |
| P-hodnota ve srovnání s placebem | 0.043 | <0.001 | ||
| Studie 2 | N = 42 | Na | Na | N = 43 |
| Medián výchozího období | 11.5 | Na | Na | 15.0 |
| % Rozdíl ve vztahu k placebu* | Na | -59,5% | ||
| P-hodnota ve srovnání s placebem | <0.001 | |||
| *Odvozeno z modelu primární analýzy ± všech 0,4 mg/kg/den pacienti také užívali souběžnou střelec, což zvyšuje expozici Fintepla. |
Obrázek 1 a Obrázek 2 ukazují procento pacientů podle kategorie záchvaty odezvy z výchozí hodnoty při křečové frekvenci záchvatů (za 28 dní) během období léčby ve studii 1 a studie 2.
Obrázek 1: Podíl pacientů podle kategorie odpovědi na záchvaty pro Fintepla a placebo u pacientů s Dravetovým syndromem (studie 1)
| |
Obrázek 2: Podíl pacientů podle kategorie odpovědi na záchvaty pro Fintepla a placebo u pacientů s Dravetovým syndromem (studie 2)
| |
Ve studii 1 3 ze 40 (8%) pacientů ve skupině Fintepla 0,7 mg/kg/den a 3 z 38 (8%) pacientů ve skupině Fintepla 0,2 mg/kg/den nehlásila během 14týdenního období léčby žádné křeče ve srovnání s 0 pacienty ve skupině placebo. Ve studii 2 1 ze 43 (2%) pacientů ve skupině Fintepla 0,4 mg/kg/den během 15týdenního léčebného období ve srovnání s 0 pacienty ve skupině placeba.
Ve studii 1 a studie 2 Fintepla byla spojena se statisticky významným delším intervalem mezi křečovými záchvaty ve srovnání s placebem (obrázek 3).
Obrázek 3: Střední nejdelší interval mezi křečovými záchvaty u pacientů s Dravetovým syndromem (studie 1 a studie 2)
| |
Lennox-Gastaut Syndrom
Účinnost FintePLA pro léčbu záchvatů spojených s LGS u pacientů ve věku 2 let a starší byla stanovena v randomizované dvojitě slepé placebem kontrolované studii u 263 pacientů ve věku 2 až 35 let (studie 3; NCT03355209).
Studie 3 compared a 0,7 mg/kg/den a a 0,2 mg/kg/den dose of Fintepla with placebo.
Pacienti měli diagnózu LGS a byli nedostatečně kontrolováni na alespoň jednom AED se stimulací vagálních nervů nebo bez ketogenní stravy. Studie měla 4týdenní výchozí období, během kterého byli pacienti povinni mít minimálně 8 záchvatů kapky při stabilní terapii AED. Záchvaty kapky byly generalizovány tonicko-klonické sekundárně generalizované tonicky-klonické tonické atonické nebo tonicky atonické záchvaty, které byly potvrzeny, aby vedly k kapkám. Po základní období následovala randomizace do 2týdenního titračního období a do následného 12týdenního období údržby, kdy dávka Fintepla zůstala stabilní.
Ve studii 3 99% pacientů užívalo 1 a 4 souběžné AED. Nejčastěji používanými souběžnými AED (u nejméně 25%pacientů) byly Clobazam (45%) lamotrigin (34%) a valproát (56%).
Primárním koncovým bodem účinnosti ve studii 3 byla střední procentuální změna oproti základní linii ve frekvenci záchvatů kapky za 28 dní během kombinované 14týdenní titrace a údržby (tj. Období léčby). Podíl pacientů, kteří dosáhnou zlepšení (minimálně mnoho nebo velmi zlepšené) v klinickém globálním dojmu změny (CGI-I), jak bylo hodnoceno hlavním vyšetřovatelem, byl sekundárním koncovým bodem.
Ve studii 3 byla střední procento změn z výchozí hodnoty (redukce) ve frekvenci záchvatů kapky za 28 dní pro skupinu dávky 0,7 mg/kg/kg/den ve srovnání s placebem (tabulka 7). Do 2 týdnů od zahájení léčby finteplou bylo pozorováno snížení záchvatů kapky a účinek zůstal obecně konzistentní po dobu 14 týdnů léčby.
Střední snížení procenta z výchozí hodnoty při frekvenci záchvatů kapky za 28 dní pro nižší dávku Fintepla (NULL,2 mg/kg/den) nedosáhlo statistické významnosti ve srovnání s placebem (tabulka 7).
Tabulka 7: Změna frekvence záchvatů kapky během léčebného období u pacientů s Lennox-Gastaut Syndrome (studie 3)
| Frekvence záchvatů kapky (za 28 dní) | Placebo | Fintepla 0,2 mg/kg/den | Fintepla 0,7 mg/kg/den |
| Studie 3 | N = 85* | N = 86* | N = 83* |
| Medián výchozího období Záchvat Frequency | 55.0 | 77.8 | 80.0 |
| Střední procentuální změna oproti základní linii během léčby | -8,7% | -13,2% | -23,7% |
| P-hodnota ve srovnání s placebem | 0,1917 | 0.0037 | |
| *Celkový počet pacientů, na nichž byla založena analýza účinnosti, je menší než celkový počet randomizovaný v dvojitě zaslepené placebem kontrolované studii, protože pacienti s chybějícími údaji byli vyloučeni z analýzy účinnosti. |
Obrázek 4 ukazuje procento pacientů podle kategorie snížení ze základní linie při frekvenci záchvatů za 28 dní během období léčby ve studii 3.
Obrázek 4: Podíl pacientů podle kategorie odpovědi na záchvaty pro Fintepla a placebo u pacientů se syndromem Lennox.gastaut (studie 3)
| |
U pacientů léčených finteplou ve srovnání s placebem byla pozorována numericky větší zlepšení na CGI-I vyšetřovatelem.
Informace o pacientovi pro Fintepla
FinteplaR ®
(Fin-tep-la)
(fenfluramin) Orální roztok
Než začnete přijímat Finteplu a pokaždé, když dostanete doplnění, přečtěte si tento průvodce léky. Mohou existovat nové informace. Tyto informace nezavazují místo rozhovoru s poskytovatelem zdravotní péče o vašem zdravotním stavu nebo léčbě.
Jaké jsou nejdůležitější informace, které bych měl vědět o Finteple?
Fintepla can cause serious side effects including :
1. Problémy s ventily v srdci (onemocnění srdečního srdeční) a vysoký krevní tlak v tepnách plic (plicní arteriální hypertenze) byly spojeny s Finteplou. Váš poskytovatel zdravotní péče provede test s názvem Echokardiogram, aby zkontroloval vaše srdce a na vysoký krevní tlak v tepnách plic, než začnete znovu brát Fintepla každých 6 měsíců během léčby a jednou 3 až 6 měsíců po provedení poslední dávky Finteply.
Okamžitě zavolejte svého poskytovatele zdravotní péče, pokud během léčby finteplou vyvinete některá z těchto příznaků a příznaků problémů s srdcem nebo plicemi:
- dušnost
- bolest na hrudi
- únava nebo slabost
- pocity rychlého třepota
- zejména se zvýšenou aktivitou (palpitace)
- Lightheadedness or mdloby
- nepravidelný puls
- oteklé kotníky nebo nohy
- namodralá barva na rty a kůži (cyanóza)
Kvůli riziku problémů se srdeční chlopní (onemocnění srdečního srdeční) a vysokého krevního tlaku v tepnách plic (plicní arteriální hypertenze) je Fintepla k dispozici pouze prostřednictvím omezeného programu s názvem Fintepla Risk Assentation and Mitigation Strategy (REMS). Než vy nebo vaše dítě obdržíte Finteplu, svého poskytovatele zdravotní péče nebo lékárník zajistí, že pochopíte, jak bezpečně vzít Fintepla. Máte-li jakékoli dotazy ohledně Fintepla, zeptejte se svého poskytovatele zdravotní péče, navštivte www.finteplarems.com nebo zavolejte na číslo 1-877-964-3649.
2. Snížená chuť k jídlu a snížená hmotnost. Snížená chuť k jídlu a snížená hmotnost are both serious a common side effects of Fintepla in people with Dravet syndrome (DS) or Lennox-Gastaut syndrome (LGS).
- Vaše hmotnost by měla být pravidelně kontrolována během léčby s Finteplou.
- Váš poskytovatel zdravotní péče bude možná muset provést změny ve vaší dávce Fintepla, pokud se vaše hmotnost sníží. V některých případech může být nutné Fintepla zastavit.
3. Sedace ospalosti a nedostatek energie (letargie). Jedná se o vážné a běžné vedlejší účinky Fintepla u lidí s Dravetovým syndromem (DS) nebo Lennox-Gastaut Syndrom (LGS). Užívání fintepla s depresivními prostředky centrálního nervového systému (CNS) včetně alkoholu může zvýšit ospalost. Nejezlute provozování těžkých strojů ani nedělejte jiné nebezpečné činnosti, dokud nevíte, jak vás Fintepla ovlivňuje.
4. Stejně jako všechny ostatní antiepileptické léky mohou Fintepla způsobit sebevražedné myšlenky nebo činy u velmi malého počtu lidí (asi 1 z 500).
Okamžitě zavolejte svému poskytovateli zdravotní péče, pokud máte některý z těchto příznaků, zejména pokud jsou nové horší nebo se obáváte:
- myšlenky na sebevraždu nebo umírání
- nová nebo horší úzkost
- Potíže se spánkem (nespavost)
- působí na nebezpečné impulsy
- Pokusy o spáchání sebevraždy
- Cítit se rozrušený nebo neklidný
- Nová nebo horší podrážděnost
- extrémní zvýšení aktivity a mluvení (mánie)
- Nová nebo horší deprese
- panické útoky
- jednat agresivní být naštvaný nebo násilný
- další neobvyklé změny v chování nebo náladě
Jak mohu sledovat časné příznaky sebevražedných myšlenek a akcí?
- Věnujte pozornost jakýmkoli změnám, zejména náhlým změnám v chování nálady, myšlenky nebo pocity.
- Udržujte všechny následné návštěvy u svého poskytovatele zdravotní péče podle plánu.
Sebevražedné myšlenky nebo činy mohou být způsobeny jinými věcmi než léky. Pokud máte sebevražedné myšlenky nebo akcí, váš poskytovatel zdravotní péče může zkontrolovat další příčiny.
5. Nepřestávejte brát Finteplu, aniž byste nejprve mluvili s poskytovatelem zdravotní péče. Zastavení záchvatu, jako je Fintepla, najednou může způsobit, že budete mít záchvaty častěji nebo záchvaty, které se nezastaví (status epilepticus).
Podle potřeby zavolejte svého poskytovatele zdravotní péče mezi návštěvami, zejména pokud se obáváte příznaků.
Co je to Fintepla?
- Fintepla is a prescription medicine used to treat the seizures associated with Dravet syndrome (DS) a Lennox- Gastaut syndrome (LGS) in patients 2 years of age a older.
- Není známo, zda je Fintepla bezpečný a účinný u dětí mladších 2 let.
Neberte si Fintepla, pokud:
- jsou alergické na fenfluramin nebo některá ze složek ve Finteple. Úplný seznam složek ve Finteple naleznete na konci této medikační příručky.
- užívají nebo přestaly užívat léky zvané inhibitory monoamin oxidázy (MAOI) za posledních 14 dní. To může způsobit vážný nebo život ohrožující problém zvaný serotoninový syndrom. Pokud si nejste jisti, zda užíváte jeden z těchto léků, kontaktujte svého poskytovatele zdravotní péče.
Předtím, než vezmete Fintepla, řekněte svému poskytovateli zdravotní péče o všech vašich zdravotních stavech, včetně, pokud jste:
- mít problémy se srdcem
- mít nebo mít hubnutí
- mít nebo mít problémy s depresí nebo sebevražedné myšlenky nebo chování
- mít problémy s ledvinami
- mít problémy s jatery
- jsou těhotné nebo plánují otěhotnět. Sdělte svému poskytovateli zdravotní péče ihned, pokud otěhotníte při převzetí Finteply. Vy a váš poskytovatel zdravotní péče se rozhodnete, zda byste měli vzít Fintepla, když jste těhotná.
- Pokud otěhotníte, když vezmete finteplu, promluvte si se svým poskytovatelem zdravotní péče o registraci u severoamerického antiepileptického registru těhotenství. Do tohoto registru se můžete zaregistrovat voláním 1-888-233-2334 nebo přejít na www.
- aedpregnancyregistry.org. Účelem tohoto registru je shromažďovat informace o bezpečnosti antiepileptických léků během těhotenství.
- jsou kojení nebo plánují kojení. Není známo, zda Fintepla přejde do mateřského mléka. Promluvte si se svým poskytovatelem zdravotní péče o nejlepším způsobu, jak nakrmit své dítě při převzetí Finteply.
Řekněte svému poskytovateli zdravotní péče o všech lécích, které užíváte včetně předpisu a volně prodejných léků vitamínů a bylinných doplňků.
Znát léky, které užíváte. Udržujte jejich seznam, abyste ukázali svého poskytovatele zdravotní péče nebo lékárníka, když získáte nový lék.
Jak mám vzít Fintepla?
- Přečtěte si Pokyny pro použití Na konci této medikační příručky pro informace o správném způsobu použití Fintepla.
- Vezměte Finteplu přesně tak, jak vám říká váš poskytovatel zdravotní péče, abyste to vzali.
- Váš poskytovatel zdravotní péče vám řekne, kolik Fintepla je třeba vzít a kdy to vzít.
- Fintepla may be taken with or without food.
- Změřte svou dávku Finteply pomocí dávkovací stříkačky, která je poskytována lékárnou. Nepoužívejte lžičku domácnosti nebo lžíci.
- Fintepla can be given through gastric a nasogastric feeding tubes
Co bych se měl vyhnout při užívání Finteply?
- Ne Pohon provozuje těžké stroje nebo provádí jiné nebezpečné činnosti, dokud nevíte, jak vás Fintepla ovlivňuje. Fintepla může způsobit, že se budete cítit ospalý.
Jaké jsou možné vedlejší účinky Finteply?
Fintepla may cause serious side effects including:
Pokud máte některý z následujících příznaků serotoninového syndromu, zavolejte svému poskytovateli zdravotní péče.
- Viz „Jaké jsou nejdůležitější informace, které bych měl vědět o Finteple?“
- serotonin syndrome. Syndrom serotoninu je problém ohrožující život, ke kterému může dojít u lidí, kteří vezmou finteplu, zejména pokud je Fintepla užíván s některými dalšími léky, aby zahrnoval:
- Antidepresiva léky zvané Ssris Snris TCAS a Maois
- St. Johns Wort
- Tryptofan
- Dextromethorphan
- lithium
- Tramadol
- Antipsychotika
- Změny duševního stavu, jako je vidět věci, které tam nejsou (halucinace) agitace nebo kóma
- Rychlý srdeční rytmus
- Zvracení nevolnosti
- Změny krevního tlaku
- vysoká teplota těla
- těsné svaly
- Potíže s chůzí
- vysoký krevní tlak (hypertenze). Hypertenze je vážný a běžný vedlejší účinek. Fintepla může způsobit zvýšení krevního tlaku, i když jste nikdy předtím neměli vysoký krevní tlak. Váš poskytovatel zdravotní péče zkontroluje váš krevní tlak, když užíváte Fintepla.
- Zvýšený tlak v oku (glaukom). Příznaky glaukomu mohou zahrnovat:
- červené oči
- snížené vidění
- vidět halos nebo jasné barvy kolem světla
- Bolest očí nebo nepohodlí
- nevolnost nebo zvracení
- rozmazané vidění
Pokud máte některý z těchto příznaků, zavolejte svému poskytovateli zdravotní péče ihned.
Mezi nejčastější vedlejší účinky Finteply při používání k léčbě Dravetova syndromu (DS) patří:
- snížená chuť k jídlu
- průjem
- nízká energie
- ospalost
- problémy s rovnováhou pohybu a chůzí
- zvýšené slintání
- Respirační infekce
- zvýšený krevní tlak
- snížená hmotnost
- zvracení
- horečka
- pády
- zácpa
- záchvaty, které se nezastaví
- Abnormální echokardiogram
- slabost
Mezi nejčastější vedlejší účinky Finteply při použití syndromu Lennox-Gastautu (LGS) patří:
- průjem
- únava
- zvracení
- ospalost
- snížená chuť k jídlu
Nejedná se o všechny možné vedlejší účinky Finteply. Pro více informací se zeptejte svého poskytovatele zdravotní péče nebo lékárníka.
Sdělte svému poskytovateli zdravotní péče, pokud máte jakýkoli vedlejší účinek, který vás vadí nebo z nich nezmizí.
Zavolejte svého lékaře, kde najdete lékařskou radu ohledně vedlejších účinků. Můžete nahlásit vedlejší účinky FDA na 1-800-FDA-1088.
Jak mám ukládat Fintepla?
- Ukládejte fintepla při teplotě místnosti mezi 68 ° F až 77 ° F (20 ° C a 25 ° C).
- Ne Chladit nebo zamrznout.
- Uložte láhev Fintepla a stříkačkou dohromady v čisté oblasti.
- Vyhoďte (zlikvidujte) jakékoli nepoužité fintepla 3 měsíce po prvním otevření láhve nebo pokud po datu na balíčku nebo láhvi uběhlo. Kteroukoli z nich přichází na prvním místě.
Udržujte Fintepla a všechny léky mimo dosah dětí.
Obecné informace o bezpečném a efektivním používání Fintepla.
Léky jsou někdy předepisovány pro jiné účely než ty, které jsou uvedeny v průvodci s léky. Nepoužívejte Fintepla pro podmínku, pro kterou nebyl předepsán. Nedávejte Finteplu jiným lidem, i když mají stejné příznaky, jaké máte. Může jim to poškodit.
Můžete požádat svého lékárníka nebo poskytovatele zdravotní péče o informace o Finteple, která je psána pro zdravotnické pracovníky.
Jaké jsou ingredience ve Finteple?
Aktivní složka: Fenfluramin Hydrochlorid
Neaktivní ingredience: Cherry chuť kyselina citronová ethylparaben hydroxyethylcelulóza methylparaben draselný citrát sukralózy a vody.
Fintepla contains no ingredient made from gluten-containing grain (wheat barley or rye) a contains not more than 0.1% of uhlohydráty který je z chutí cherry.
Tento průvodce medikací byl schválen americkou správou potravin a léčiv.
Pokyny pro použití
Fintepla ®
(Fin-tep-la)
(fenfluramin) Orální roztok 2.2 mg/mL
Než začnete používat ústní řešení Fintepla a pokaždé, když získáte doplnění, přečtete si porozumění a postupujte podle pokynů. Mohou existovat nové informace.
Tyto pokyny pro použití obsahují informace o tom, jak vzít Fintepla. Tyto informace nezavazují místo rozhovoru s poskytovatelem zdravotní péče o vašem zdravotním stavu nebo léčbě.
Co je zahrnuto s Finteplou?
Následující položky jsou zahrnuty pro přípravu a poskytnutí ústní dávky Fintepla:
- 1 láhev ústního roztoku Fintepla (NULL,2 mg/ml)
- 2 opakovaně použitelné ústní stříkačky
| |
Volejte lékárníka na čísle 1-844-288-5007, pokud jste neobdrželi výše uvedené položky nebo pokud je potřebujete pomoci s jejich používáním.
Důležité informace o Finteple
- Fintepla is an oral medicine (taken by mouth) a is given 2krát každý den . Postupujte podle pokynů poskytovatelů zdravotní péče pro přijímání nebo poskytování dávek Finteply.
- Máte -li dotazy ohledně toho, jak připravit nebo dát Fintepla, kontaktujte svého poskytovatele zdravotní péče nebo zavolejte svému lékárníkovi.
- Vždy použijte ústní stříkačky poskytované s Finteplou, abyste se ujistili, že je dána správná dávka. Pokud potřebujete novou injekční stříkačku, kontaktujte svého lékárníka. Ne Použijte lžičku domácnosti nebo lžíci.
Orální injekční stříkačky poskytované finteplou lékárnou.
S Finteplou obdržíte 2 opakovaně použitelné ústní stříkačky.
2 ústní stříkačky, které mohou měřit až 3 ml
NEBO
2 ústní stříkačky, které mohou měřit až 6 ml
| |
Volejte lékárníka na čísle 1-844-288-5007, pokud máte nějaké dotazy ohledně stříkaček poskytovaných s Finteplou.
Části ústní stříkačky
| |
Příprava dávky
Krok 1 . Ujistěte se, že máte:
- Láhev ústního roztoku fintepla a
- Čistá suchá opakovaně použitelná perorální stříkačka, která byla vybavena Finteplou.
Krok 2. Zkontrolujte vyřazení po datu (mm/dd/yyyy).
| |
- Ne Pokud uplynulo datum vyhazování (vyřazení), použijte lék.
- Pokud je datum blízké, kontaktujte vaši lékárnu nebo poskytovatele zdravotní péče a získejte doplnění nebo nový předpis.
- Pokud uplynulo datum, zlikvidujte jakékoli nepoužité fintepla.
Krok 3. Stiskněte dolů a otočte uzávěr odolných proti dětství doleva (proti směru hodinových ručiček) a vyjměte ji z láhve.
- Odložte čepici stranou (neodhoďte).
| |
Krok 4. Ujistěte se, že adaptér je na láhvi.
- Pokud láhev nemá adaptér, kontaktujte lékárníka.
- Vždy nechte adaptér na místě V láhvi medicíny.
| |
Krok 5. V případě potřeby vyjměte ústní stříkačku z jejího obalu.
Používejte pouze ústní stříkačky poskytované s Finteplou.
Pokud je ústní stříkačka poškozena nebo si nemůžete přečíst značky dávky:
- Použijte druhou perorální stříkačku nebo
- Kontaktujte lékárníka a získejte nový.
| |
Krok 6. Ujistěte se, že píst je tlačen až do ústní stříkačky.
| |
Krok 7. Pevně držte láhev léku na tvrdém rovném povrchu.
Krok 8. Zatlačte špičku ústní stříkačky do otvoru adaptéru, dokud jej nelze tlačit dále.
| |
Krok 9. Držte ústní stříkačku a láhev pohromadě a otočte se vzhůru nohama.
| |
Krok 10. Pomalu vytáhněte píst perorální stříkačky, abyste stáhli předepsanou dávku.
| |
| |
| |
Příprava dávky (pokračování)
Krok 11. Zarovnejte konec pílu se značkou pro předepsanou dávku na perorální stříkačce.
Tipy, jak získat správnou dávku
- Pokud vytáhnete příliš mnoho léků:
- Nechte ústní stříkačku v adaptéru.
- Pomalu zatlačte píst zpět do stříkačky, dokud nedosáhnete předepsané dávky.
- Pokud vidíte v léku vzduchové bubliny:
- Nechte ústní stříkačku v adaptéru.
- Vytáhněte píst dále dolů.
- Nechte bubliny stoupat na špičku stříkačky.
- Stiskněte píst celou cestu.
- Pomalu vytáhněte píst do předepsané dávky.
Poznámka: Velmi malé bubliny v kapalině jsou normální.
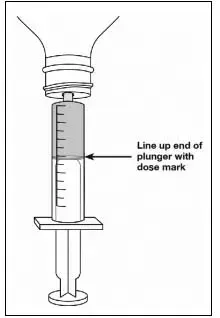
Krok 12. Držte ústní stříkačku a láhev pohromadě a poté otočte láhev pravou stranu nahoru.
| |
Krok 13. Držte láhev pevně jemně vytáhněte ústní stříkačku z adaptéru láhve.
| |
Krok 14. Ujistěte se, že dávka v perorální stříkačce stále odpovídá předepsané dávce.
Pokud se dávka neshoduje:
- Vložte stříkačku zpět do adaptéru.
- Viz kroky 9 až 11 a upravte dávku podle potřeby.
Dávat Fintepla
Krok 15. Umístěte špičku ústní stříkačky na vnitřek tváře.
Krok 16. Jemně zatlačte píst, dokud nebude podáván veškerý lék v ústní stříkačce.
| |
- Ne Squirt nebo násilně zatlačte lék do zadní části krku. To může způsobit dusivání.
Krok 17. Umístěte čepici zpět na láhev pevně otočením čepice doprava (ve směru hodinových ručiček), dokud se nezastaví.
- Vždy nechte adaptér na místě in the bottle
- Čepice se na něj hodí.
| |
Čištění stříkačky
- Opláchněte ústní stříkačku čistou vodou z vodovodu a po každém použití ji nechte sušit.
- Ujistěte se, že opláchnete vnitřek stříkačky a pístu.
Tipy na čištění:
- Vyčistěte vodu z vodovodu do injekční stříkačky a několikrát ji vytlačte, abyste vyčistili stříkačku.
- Odstraňte píst z hlavně ústní stříkačky
- Opláchněte obě části pod vodovodní vodou
- Ujistěte se, že stříkačka a píst jsou před dalším použitím zcela suché.
- Stříkačka je také bezpečná k čištění v myčce nádobí.
| |
Jak mám ukládat Fintepla?
- Ukládejte fintepla při teplotě místnosti mezi 68 ° F až 77 ° F (20 ° C až 25 ° C).
- Ne Chladit nebo zamrznout.
- Udržujte čepici pevně zavřený a láhev vzpřímeně.
- Uložte láhev Fintepla a stříkačkou dohromady v čisté oblasti.
- Vyhoďte (zlikvidujte) jakékoli nepoužité fintepla 3 měsíce po prvním otevření láhve nebo pokud po datu na balíčku nebo láhvi uběhlo. Kteroukoli z nich přichází na prvním místě.
- Udržujte Fintepla a všechny léky mimo dosah dětí.
Tyto pokyny pro použití byly schváleny americkou správou potravin a léčiv.
