Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
Ergot derivátyPravda
Shrnutí drog
Co je Trudhesa?
Trudhesa (dihydroergotamin mesylát) nosní sprej je ergotaminový derivát používaný k léčbě migrény s aurou nebo bez aury u dospělých.
Jaké jsou vedlejší účinky Trudhesa?
Pravda
- kopřivka
- potíže s dýcháním
- Otok vašeho obličeje rty jazyk nebo krk
- pomalý nebo rychlý srdeční rytmus
- Slabost v nohou
- bolest svalů v pažích nebo nohou
- brnění nebo necitlivost
- chlad v rukou a nohou
- modré prsty a prsty
- Těžká bolest žaludku
- Bolest čelisti nebo levé paže
- bolest na hrudi nebo tlak
- Náhlá únava
- slabost na jedné straně těla
- potíže s mluvením
- změny vize
- mentální nebo změny nálady
- zmatek
- vyrážka
- svědění a
- Těžká závratě
Získejte lékařskou pomoc okamžitě, pokud máte výše uvedené příznaky.
Mezi vedlejší účinky Trudhesa patří:
- rýma nosu
- nevolnost
- změněno smysl chuti
- Reakce webu aplikací
- závrať
- zvracení
- ospalost
- bolest v krku a
- průjem.
Pokud máte následující vážné vedlejší účinky, vyhledejte lékařskou péči nebo zavolejte na číslo 911:
- Vážné příznaky očí, jako je ztráta náhlého vidění rozmazané vidění vidění Vision Vision Eye Eye Eye Eye Eye Eye Eye Eye nebo vidět halos kolem světel;
- Vážné příznaky srdce, jako je rychlé nepravidelné nebo bušení srdečního rytmu; třepování v hrudi; dušnost; a náhlé závratě Lightheadedness nebo omdlet;
- Těžká zmatek bolesti hlavy zkroucený řečový rameno nebo slabost nohou Potíže se ztrátou chůze pocitu koordinace Pocit nestabilní velmi tuhé svaly vysoké horečky bohaté pocení nebo třes.
Tento dokument neobsahuje všechny možné vedlejší účinky a mohou dojít k jiným. Další informace o vedlejších účincích najdete u svého lékaře.
Dávkování pro Trudhesa
Doporučená dávka nosního spreje Trudhesa je 1,45 mg (podávána jako jeden měřený sprej 0,725 mg do každé nosní dírky). Dávka může být v případě potřeby opakována minimálně 1 hodinu po první dávce.
Trudhesa u dětí
Bezpečnost a účinnost nosního spreje Trudhesa je u pediatrických pacientů.
Jaké léky nebo doplňky interagují s Trudhesa?
Trudhesa nosní sprej může interagovat s jinými léky, jako jsou:
- Beta-blokátory
- nikotin
- Selektivní inhibitor zpětného vychytávání serotoninu ( Li ) antidepresiva (např. Fluoxetin fluvoxamin paroxetin sertralin)
- Inhibitory proteázy (např. Ritonavir neelfinavir indinavir)
- makrolid Antibiotika (např. Erythromycin Clarithromycin)
- Antimykotiky (např. Ketoconazol itraconazol)
- Triptans a
- Vazokonstriktoři.
Řekněte svému lékaři všechny léky a doplňky, které používáte.
Trudhesa během těhotenství a kojení
Před použitím Trudhesa nosní spreje řekněte svému lékaři, pokud jste těhotná nebo plánujete otěhotnět. Může to zvýšit riziko předčasného porodu a může poškodit plod. Není známo, zda nosní sprej Trudhesa prochází do mateřského mléka; Ergotamin však související léčivo je přítomno v mateřském mléce. Kvůli potenciálu sníženého přísunu mléka a závažných nežádoucích účinků u kojeného dítěte, včetně zvracení průjmu slabého pulsu a nestabilního kojení krevního tlaku, se nedoporučuje během léčby nosním sprejem Trudhesa a po dobu 3 dnů po poslední dávce. Dodávka mateřského mléka během této doby by měla být čerpána a vyřazena.
Další informace
Naše Trudhesa (dihydroergotamin mesylát) nosní postřikové vedlejší účinky lékové účinky poskytuje komplexní pohled na dostupné informace o možných vedlejších účincích při užívání tohoto léku.
Nejedná se o úplný seznam vedlejších účinků a mohou dojít k dalším. Zavolejte svého lékaře, kde najdete lékařskou radu ohledně vedlejších účinků. Můžete nahlásit vedlejší účinky FDA na 1-800-FDA-1088.
Informace o drogách FDA
- Popis léku
- Indikace
- Vedlejší účinky
- Lékové interakce
- Varování
- Předávkovat
- Kontraindikace
- Klinická farmakologie
- Průvodce léky
VAROVÁNÍ
Periferní ischemie po souběžné podávání se silnými inhibitory CYP3A4
Seriferní a/nebo život ohrožující periferní ischémie byla spojena s souběžnou podáváním dihydroergotaminu se silnými inhibitory CYP3A4. Protože inhibice CYP3A4 zvyšuje hladiny séra dihydroergotaminu, je zvýšeno riziko vazospasmu vedoucího k mozkové ischemii a/nebo ischemii končetin. Proto je souběžné použití Trudhesa se silnými inhibitory CYP3A4 kontraindikováno [viz viz Kontraindikace VAROVÁNÍS AND PRECAUTIONS a Lékové interakce ].
Popis pro Trudhesa
Trudhesa (dihydroergotamin mesylát) nosní sprej je jednorázová kombinovaná produktu drog-zařízení obsahující konstitutuentu léčiva dihydroergotaminu mesylátu a složka nosního stříkání.
Chemický název pro mesylát dihydroergotaminu je ergotaman-3 '6' 18-Trione 910-dihydro-12'-hydroxy-2'-methyl-5'- (fenylmethyl)-(5'a)-monomethanesulfonát. Jeho molekulová hmotnost je 679,78 a jeho molekulární vzorec je c 33 H 37 N 5 O 5 • Ch 4 O 3 S.
Chemická struktura je:
 |
Drogová složka je roztok dihydroergotaminu mesylátu. Každý mililitr (ML) roztoku obsahuje dihydroergotamin mesylát 4,0 mg (ekvivalentní 3,43 mg dihydroergotaminu) a následující neaktivní složky: kofein (NULL,0 mg) oxid uhličitý (Q.s.) (50.0 mg) a voda (q.s. až 1.0 ML).
Trudhesa nosní sprej po montáži a aktivaci poskytuje 0,725 mg dihydroergotamin mesylát na sprej. Celková dávka 1,45 mg mesylátu dihydroergotaminu je dodávána ve 2 sprejů. Nosní stříkací zařízení obsahuje hnací látka hydrofluoroalkane-134a (HFA).
Použití pro Trudhesa
Trudhesa je indikována pro akutní léčbu migrény s aurou nebo bez aury u dospělých.
Omezení použití
Trudhesa není indikována pro preventivní léčbu migrény.
Trudhesa není indikována pro léčbu hemiplegické nebo bazilární migrény.
Dávkování pro Trudhesa
Informace o dávkování
Doporučená dávka Trudhesa je 1,45 mg podávána jako dva měřené spreje do nosu (jeden sprej 0,725 mg do každé nosní dírky).
Dávka může být v případě potřeby opakována minimálně 1 hodinu po první dávce. Nepoužívejte více než 2 dávky trudhesa během 24 hodin nebo 3 dávek během 7denního období.
Hodnocení před první dávkou
Před zahájením Trudhesa se doporučuje kardiovaskulární hodnocení [viz viz VAROVÁNÍS AND PRECAUTIONS ]. For patients with risk factors predictive of coronary artery disease who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in the setting of an equipped healthcare facility.
Důležité pokyny pro správu
Trudhesa je pouze pro nosní podání a nesmí být injikován.
Trudhesa musí být sestavena před použitím (viz Pokyny pro použití ). Po otevření lahvičky nebo sestavení produktu použijte nebo zlikvidujte Trudhesa do 8 hodin.
Premine The Sestavené Trudhesa před počátečním použitím uvolněním 4 sprejů. Použijte Trudhesa ihned po aktivaci. Zlikvidujte Trudhesa ihned po použití. Pokud je potřeba další dávka, otevřete a připravte novou Trudhesa.
Jak dodáno
Formy a silné stránky dávkování
Trudhesa (dihydroergotamin mesylát) nosní sprej je kombinovaný produkt s jednou dávkou drog-zařízení obsahující lahvičku dihydroergotamin mesylátu s čistým a bezbarvým až slabě žlutým roztokem a intranazálním doručovacím zařízením. Každý sprej poskytuje 0,725 mg mesylátu dihydroergotaminu.
Trudhesa (dihydroergotamin mesylát) nosní sprej (NULL,725 mg na sprej) je dodáván jako balíček 4 jednorázových jednotek ( NDC 77530-725-04). Každá jednotka jednorázová dávka obsahuje:
- Jedna jantarová skleněná lahvička ( NDC 77530-725-01) obsahující 4 mg dihydroergotamin mesylát v 1 ml čistém a bezbarvé až slabě žlutém roztoku. Zazářatá zátka není vyrobena z latexu přírodního gumy.
- Jedno nosní stříkací zařízení.
Skladování a manipulace
Uložte trudhesa při kontrolované pokojové teplotě 20 ° C až 25 ° C (68 ° F až 77 ° F) pomocí výletů povolených mezi 15 ° C až 30 ° C (59 ° F až 86 ° F). Neomeďte se ani zamrzněte.
Vyrobeno: Mipharm S.P.A. Milano Itálie. Revidováno: září 2021
Vedlejší účinky for Trudhesa
Následující klinicky významné nežádoucí účinky jsou popsány jinde při označování:
- Periferní ischemie po souběžné podávání se silnými inhibitory CYP3A4 [viz viz Varování a VAROVÁNÍS AND PRECAUTIONS ]
- Ischémie myokardu a/nebo infarkt další nepříznivé srdeční příhody a úmrtí [viz VAROVÁNÍS AND PRECAUTIONS ]
- Cerebrovaskulární nežádoucí reakce a úmrtí [viz VAROVÁNÍS AND PRECAUTIONS ]
- Další nežádoucí účinky související s vazospasmem [viz VAROVÁNÍS AND PRECAUTIONS ]
- Zvýšení krevního tlaku [viz VAROVÁNÍS AND PRECAUTIONS ]
- Nadužívejte bolesti hlavy [viz viz VAROVÁNÍS AND PRECAUTIONS ]
- Předčasná práce [viz VAROVÁNÍS AND PRECAUTIONS ]
- Fibrotické komplikace [viz VAROVÁNÍS AND PRECAUTIONS ]
- Místní podráždění [viz VAROVÁNÍS AND PRECAUTIONS ]
Zkušenosti z klinických studií
Protože klinické studie se provádějí za široce měnících se podmínek, nežádoucí rychlost nežádoucí reakce pozorovaná v klinických studiích léčiva nelze přímo porovnat s mírami v klinických studiích s jiným lékem a nemusí odrážet míru pozorované v praxi.
Nežádoucí účinky v placebem kontrolovaných pokusech s dihydroergotaminem (DHE) mesylátovým nosním sprejem [viz viz Klinické studie ]
Ze 1796 pacientů a subjektů léčených dávkami nosních sprejů DHE 2 mg nebo méně v USA a zahraničních klinických studiích 26 (NULL,4%) byla z důvodu nežádoucích účinků přerušena. Nežádoucí účinky spojené s přerušením byly v klesajícím pořadí frekvence: rinitida (13) závratě (2) edém obličeje (2) a každý z jednoho pacienta v důsledku studeného pocení náhodné traumatické deprese volitelná chirurgie zvracet alergii na hypotenzi a paraestsie.
obecný název pro Percocet 10 325
Tabulka 1 shrnuje míru výskytu nežádoucích účinků uváděných nejméně 1% pacientů, kteří dostávali nosní sprej DHE pro léčbu migrény během placebem kontrolovaných klinických studií s dvojitým pohybem a byli častější než u pacientů, kteří dostávali placebo. Nejčastěji hlášené nežádoucí účinky (větší než 1% pacientů, kteří dostávali nosní sprej), byly nevolnosti rýmy pozměněné pocitem reakcí na místo aplikace na místě chuti závratě zvracení somnolence faryngitidy a průjmu. Ve většině případů byly tyto události přechodné a samosprávné a nevedly k přerušení pacienta ze studie.
Tabulka 1 Nežádoucí účinky hlášené nejméně 1% pacientů s nosním sprejem DHE a vyskytovaly se častěji než ve skupině s placebem v migréně placebem kontrolovaných studiích
| A nosní sprej N = 597 % | Placebo N = 631 % | |
| Respirační systém | ||
| Rhinitis | 26 | 7 |
| Pharyngitis | 3 | 1 |
| Gastrointestinální systém | ||
| Nausea | 10 | 4 |
| Vomiting | 4 | 1 |
| Diarrhea | 2 | <1 |
| Speciální smysly jiné | ||
| Altered Sense of Taste | 8 | 1 |
| Web aplikace | ||
| Web aplikace Reaction | 6 | 2 |
| Centrální a periferní nervový systém | ||
| Dizziness | 4 | 2 |
| Somnolence | 3 | 2 |
| Tělo jako celek | ||
| Hot Flashes | 1 | <1 |
| Asthenia | 1 | 0 |
| Muskuloskeletální systém | ||
| Stiffness | 1 | <1 |
Nežádoucí účinky ve studiích s Trudhesa
Během 6 až 12 měsíců byla provedena studie s otevřenou značkou u dospělých (ve věku 18 až 66 let) byla provedena za účelem vyhodnocení bezpečnosti a snášenlivosti opakovaného použití Trudhesa Trudhesa. Celkem 354 pacientů s migrénou dostalo alespoň jednu dávku Trudhesa. Sto osmdesát pět pacientů léčilo v průměru nejméně dvě migrény měsíčně po dobu 6 měsíců a 55 pacientů léčilo v průměru nejméně dvě migrény měsíčně po dobu 12 měsíců. Z pacientů, kteří dostávali alespoň jednu dávku pacientů s Trudhesa 185 (NULL,3%), zažili lokální dráždivé příznaky. Z těchto nejběžnějších lokálních dráždivých symptomů byly nosofaryngitida rinitida nosní nepohodlí produktu Chuť abnormální/dysgeusia sinusitis sinus nepohodlí čichový test abnormální epistaxe faryngitida nosální slizniční porucha změna v úmyslu ucha a rhinorrhea [viz rhinorrhea [viz rhinorrhea [viz rhinorrhea [ VAROVÁNÍS AND PRECAUTIONS ].
Zážitek z postmarketingu
Následující nežádoucí účinky byly identifikovány při použití postratelovaného mesylátu dihydroergotaminu. Protože tyto reakce jsou hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo navázat příčinný vztah k expozici léčiva:
Vasospasm parestezie Hypertenze závratě úzkostná dušnost hlavy propláchnutí průjmové vyrážky zvýšila pocení a pleurální a retroperitoneální fibrózu po dlouhodobém použití dihydroergotaminu. Po použití dihydroergotaminového mesylátu byly hlášeny případy infarktu myokardu a mrtvice [viz viz [viz VAROVÁNÍS AND PRECAUTIONS ].
Lékové interakce for Trudhesa
Inhibitory CYP3A4
V souvislosti s souběžnou podáváním intravenózního podávání dihydroergotaminu a silného inhibitory CYP3A4, jako jsou inhibitory proteázy (např. Ritonavir neelfinavir) makrolidové, (např. Erythromycin a antibiotiky (např. Erythromycin) a inhibitory CYP3A4 (např. Erythromycinové inhibitory (např. Ritonavir nelfinavir (např. Ritonavir indinavir (např. Ritonavir nefinavir (např. Ritonavir nelfinavir, existují vzácné nežádoucí makrolidové inhibitory, jako jsou inhibitory proteázy (např. Ritonavir nelfinavir (např. E. e. itraconazol), což má za následek vazospasmus, který vedl k mozkové ischemii a/nebo ischemii končetin [viz VAROVÁNÍS AND PRECAUTIONS ]. The use of strong CYP3A4 inhibitory with dihydroergotamine is contraindicated [see Kontraindikace ]. Administer moderate CYP3A4 inhibitory (e.g. saquinavir nefazodon flukonazol grapefruit juice fluoxetine fluvoxamine zileuton clotrimazole) with caution.
Triptans
Triptans (serotonin [5-HT] 1B/1D receptor agonists) have been reported to cause coronary artery vasospasm a its effect could be additive with TRUDHESA. Therefore Triptans a TRUDHESA should not be taken within 24 hodiny of each other [see Kontraindikace ].
Beta blokátory
Byly zprávy, že propranolol může zesílit vazokonstriktivní účinek ergotaminu blokováním vazodilační vlastnosti epinefrinu.
Vazokonstriktoři
Trudhesa je kontraindikována pro použití s periferními a centrálními vazokonstriktory, protože tato kombinace může způsobit synergické zvýšení krevního tlaku [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Nikotin
Nikotin may provoke vasoconstriction in some patients predisposing to a greater ischemic response to ergot therapy [see VAROVÁNÍS AND PRECAUTIONS ].
Selektivní inhibitory zpětného vychytávání serotoninu
Slabost hyperreflexie a nekoordinace byla hlášena jen zřídka, když 5-HT 1 Agonisté byli podváděni selektivními inhibitory zpětného vychytávání serotoninu (např. Fluoxetin fluvoxamin paroxetin sertralin).
Zneužívání a závislost drog
Kontrolovaná látka
Trudhesa obsahuje dihydroergotamin (jako mesylátová sůl), což není kontrolovaná látka.
Zneužívání
Zneužívání is the intentional non-therapeutic use of a drug even once for its desirable psychological or physiological effects. Currently available data have not demonstrated drug abuse with dihydroergotamine. However cases of drug abuse in patients on other forms of ergot therapy have been reported.
Závislost
Fyzikální závislost je stav, který se vyvíjí v důsledku fyziologické adaptace v reakci na opakované užívání drog, které se projevuje nápisy a symptomy po prudkém přerušení nebo významné redukci dávky léčiva. V současné době dostupná data neprokázala fyzickou nebo psychologickou závislost s dihydroergotaminem. Byly však hlášeny případy psychologické závislosti u pacientů na jiných formách ergotové terapie.
Varování pro Trudhesa
Zahrnuto jako součást 'OPATŘENÍ' Sekce
Opatření pro Trudhesa
Periferní ischemie po souběžné podávání se silnými inhibitory CYP3A4
Seriferní a/nebo život ohrožující periferní ischemie byla spojena s souběžnou podáváním dihydroergotaminu se silnými inhibitory CYP3A4 včetně inhibitorů proteázy makrolidové antibiotiky a antimykotiky. Protože inhibice CYP3A4 zvyšuje hladiny séra dihydroergotaminu, je zvýšeno riziko vazospasmu vedoucího k mozkové ischemii a/nebo ischemii končetin. Proto je souběžné použití Trudhesa se silnými inhibitory CYP3A4 kontraindikováno [viz viz Kontraindikace a Lékové interakce ].
Ischémie myokardu a/nebo infarkt další srdeční nežádoucí účinky a úmrtí
Existuje potenciál nepříznivých srdečních nežádoucích účinků s léčbou Trudhesa. Po použití dihydroergotaminového mesylátu došlo k vážným nepříznivým srdečním událostem, včetně některých, které byly fatální. Tyto události zahrnovaly akutní infarkt myokardu Lifethereting poruchy srdečního rytmu (např. Komorová tachykardie a komorová fibrilace) koronární tepna vazospasm a přechodnou ischemii myokardu.
Před zahájením Trudhesa se doporučuje kardiovaskulární hodnocení, aby se zjistilo, zda pacient neobsahuje koronární tepnu a ischemické onemocnění myokardu nebo jiného významného základního kardiovaskulárního onemocnění. Pokud během kardiovaskulárního hodnocení je zdravotní anamnéza pacienta (včetně rizikových faktorů) nebo elektrokardiografické zkoumání konzistentní s vazospasmem koronární tepny nebo ischemií myokardu Trudhesa by neměla být podávána [viz viz [viz viz [viz viz [viz viz Kontraindikace ].
For patients with risk factors predictive of coronary artery disease (e.g. hypertension hypercholesterolemia smoker obesity diabetes strong family history of coronary artery disease females who are surgically or physiologically postmenopausal or males who are over 40 years of age) who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in the setting vybaveného zdravotnického zařízení, pokud pacient dříve neobdržel dihydroergotamin mesylát. Během intervalu bezprostředně po prvním použití Trudhesa se u pacientů s rizikovými faktory doporučuje elektrokardiogram elektrokardiogramu, protože ischemie může dojít v nepřítomnosti klinických příznaků.
Cerebrovaskulární nežádoucí účinky a úmrtí
Potenciál nepříznivých cerebrovaskulárních nežádoucích účinků existuje s léčbou Trudhesa. U pacientů léčených mesylátem dihydroergotaminu; a některé vyústily v úmrtí. V řadě případů se zdá být možné, že cerebrovaskulární příhody byly primárním, že mesylát dihydroergotaminu byl podáván v nesprávném přesvědčení, že zažívané příznaky byly důsledkem migrény, když nebyly. Je třeba poznamenat, že pacienti s migrénou mohou být vystaveni zvýšenému riziku určitých cerebrovaskulárních příhod (např. Přechodný ischemický útok na krrci mrtvice). Přerušte Trudhesa, pokud je podezření na cerebrovaskulární událost.
Další nežádoucí účinky související s vazospasmem
Trudhesa jako jiné ergot alkaloidy mohou způsobit vazospastické reakce jiné než vazospasm koronární tepny. U dihydroergotaminu mesylátu byla hlášena periferní vaskulární a tlusté ischemie.
Vasospastické jevy spojené s dihydroergotaminem mesylátem mohou také způsobit bolesti svalů, která se otuchá chlad a cyanóza číslic. U pacientů s kompromitovaným cirkulací může perzistentní vazospasmus vést k gangrénu nebo smrti. Trudhesa by měla být okamžitě přerušena, pokud se vyvinou příznaky nebo příznaky vazokonstrikce.
Pacienti, kteří zažívají jiné příznaky nebo znaky, naznačují snížený arteriální tok, jako je ischemický syndrom tračníku nebo Raynaudův syndrom po použití jakéhokoli 5-HT agonisty včetně Trudhesa, by měl být vyhodnocen poskytovatelem zdravotní péče.
Zvýšení krevního tlaku
Významné zvýšení krevního tlaku bylo hlášeno při vzácných případech u pacientů s anamnézou hypertenze a bez ní ošetřené dihydroergotaminem mesylátem. Trudhesa je kontraindikována u pacientů s nekontrolovanou hypertenzí [viz Kontraindikace ].
Po dávkování bylo pozorováno 18% nárůst průměrného tlaku plicní tepny s dalšími 5-HT 1 Agonista ve studii hodnotící subjekty podstupující srdeční katetrizaci.
Nadužívá bolest hlavy
Nadměrné užívání akutních migrénových léčiv (např. Ergotaminů Triptans opioidů nebo kombinace těchto léků po dobu 10 nebo více dnů za měsíc) může vést k zhoršení bolesti hlavy (tj. Nadměrné bolesti hlavy). Nadměrná bolest hlavy s léky se může vyskytovat jako denní bolesti hlavy podobné migréně nebo jako výrazné zvýšení frekvence migrénových útoků. Může být nezbytná detoxikace pacientů, včetně stažení nadužívaných léků a léčby abstinenčních symptomů (které často zahrnují přechodné zhoršení bolesti hlavy).
Předčasná práce
Na základě mechanismu působení dihydroergotaminu a zjištění z publikované literatury může Trudhesa způsobit předčasnou porod. Vyvarujte se používání Trudhesa během těhotenství [viz Použití v konkrétních populacích ]
Fibrotické komplikace
Potenciál fibrotických komplikací existuje s léčbou Trudhesa. U pacientů po dlouhodobém denním používání dihydroergotaminového mesylátu se objevily zprávy o pleurální a retroperitoneální fibróze. Zřídka prodloužené denní užívání jiných ergotových alkaloidních léčiv je spojeno se srdeční chlopní fibrózou. Vzácné případy byly také hlášeny ve spojení s použitím mesylátu dihydroergotaminu; V těchto případech však pacienti také dostávali léky, o nichž je známo, že jsou spojeny se srdeční chlopní fibrózou.
Podávání Trudhesa by nemělo překročit pokyny pro dávkování a nemělo by být používáno pro chronické denní podávání [viz Dávkování a podávání ].
Místní podráždění
Místní dráždivé příznaky byly hlášeny u 52% pacientů léčených alespoň jednou dávkou Trudhesa v otevřené studii, která umožnila opakované použití Trudhesa po dobu 6 až 12 měsíců. Nejběžnějšími lokálními dráždivými symptomy (nejméně 1%pacientů) byly nosofaryngitida (21%) rinitida (19%) nosní nepohodlí (7%) chuť produktu Abnormální/Dysgeusia (6%) sinusitida (5%) sinusová nepohodlí (4%) Olforově testovací abnormální/ (UPSIT)] (4%) Epistaxe (3%) faryngitida (3%) nosní slizniční porucha (2%) změna vůně (1%) nepohodlí ucha (1%) a nosiště (1%). Pokud dojde k závažné místní podrážděné události z žádného jiného přičitatelného důvodu, která by Trudhesa měla být dočasně pozastavena, dokud se událost nerozhodne. Pokud se událost nerozhodne nebo se opakuje s opětovným výzvou Trudhesa, měla by být trvale přerušena. Podávání Trudhesa by nemělo překročit pokyny pro dávkování a nemělo by být používáno pro chronické denní podávání [viz Dávkování a podávání ].
Nosní tkáň u zvířat ošetřených dihydroergotaminem mesylátem denně vykazovala mírné podráždění sliznice charakterizované slizničními buňkami a hyperplázií přechodných buněk a metaplasií skvamózních buněk. Změny v nosní sliznici potkana po 64 týdnech byly méně závažné než po 13 týdnech. Lokální účinky na respirační tkáň po chronickém intranazálním dávkování u zvířat nebyly hodnoceny.
Informace o poradenství pro pacienta
Doporučujte pacientovi, aby si přečetl značení pacienta schváleného FDA ( Průvodce léky a Pokyny pro použití ).
Kolik koncerty bych měl vzít
Vážné a/nebo život ohrožující reakce se souběžným podáním inhibitorů CYP3A4
Informujte pacienty, že vážná a/nebo život ohrožující periferní ischemie (mozková ischemie a/nebo ischémie končetin) byla spojena s souběžnou podáváním inhibitorů dihydroergotaminu a silné inhibitory CYP3A4, jako je makrolidová antibiotika a proteáza [viz [viz inhibitory [viz Kontraindikace VAROVÁNÍS AND PRECAUTIONS a Lékové interakce ].
Ischémie myokardu a/nebo infarkt další srdeční příhody cerebrovaskulární příhody a úmrtí
Informujte pacienty o riziku vážných srdečních cerebrovaskulárních a jiných událostí souvisejících s vazospasmem. Doporučujte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud si při převzetí Trudhesa vyvinou nějaké rizikové faktory nebo příznaky. Informujte pacienty, že nikotin může vyvolat vazokonstrikci predispozice k větší ischemické odpovědi [Viz VAROVÁNÍS AND PRECAUTIONS ].
Nadužívá bolest hlavy
Informujte pacienty, že užívání léků k léčbě migrénových útoků po dobu 10 a více dní za měsíc může vést k prohloubení bolesti hlavy a povzbudit pacienty, aby zaznamenali frekvenci bolesti hlavy a užívání drog (např. Udržováním deníku bolesti hlavy) [Viz viz VAROVÁNÍS AND PRECAUTIONS ].
Místní podráždění
Poraďte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud mají obtěžující místní podráždění [viz VAROVÁNÍS AND PRECAUTIONS ].
Lékové interakce
Poraďte pacientům, aby informovali své poskytovatele zdravotní péče, pokud berou nebo plánují užívat jakékoli léky na předpis nebo volně prodejné drogy, protože existuje potenciál pro interakce [viz viz Lékové interakce ].
Těhotenství
Poraďte pacientům o riziku předčasného porodu. Poraďte ženám, aby informovaly svého poskytovatele zdravotní péče, zda jsou těhotné nebo mají v úmyslu otěhotnět [viz VAROVÁNÍS AND PRECAUTIONS Použití v konkrétních populacích ]
Laktace
Doporučujte pacientům, aby během léčby s Trudhesou nekojili [viz Použití v konkrétních populacích ].
Důležité pokyny pro správu
Poraďte se s pacienty, že Trudhesa musí být sestavena před použitím a že před podáváním musí být zařízení aktivováno (tj. Čerpeno 4krát). Pokynu pacientů, aby používali nebo zlikvidovali Trudhesa do 8 hodin po otevření lahvičky nebo se sestavení produktu.
Neklinická toxikologie
Zhodnocení mutageneze karcinogeneze plodnosti
Karcinogeneze
Hodnocení karcinogenního potenciálu dihydroergotaminového mesylátu u myší a potkanů nebylo posouzeno.
Mutageneze
Mesylát dihydroergotaminu byl negativní v in vitro test mutagenity (Ames) a pozitivní v in vitro Chromozomální aberace (test čínských křečků v79 čínských křečků s metabolickou aktivací a testy lidské periferní krve). Dihydroergotamin byl negativní nadarmo Testy mikronukleusu u myší a křečka.
Poškození plodnosti
Neexistoval žádný důkaz o zhoršení plodnosti u potkanů podávanými intranazálními dávkami dihydroergotaminu mesylátu až 1,6 mg/den, který byl spojen s plazmatickými expozicemi (AUC) přibližně 3krát, které u lidí při maximální doporučené lidské dávce 2,9 mg/den.
Použití v konkrétních populacích
Těhotenství
Shrnutí rizika
Dostupné údaje z publikované literatury naznačují zvýšené riziko předčasného porodu při použití Trudhesa během těhotenství. Vyvarujte se používání Trudhesa během těhotenství [viz VAROVÁNÍS AND PRECAUTIONS ]. Data collected over decades have shown no increased risk of major birth defects or miscarriage with use of dihydroergotamine mesylate during pregnancy.
In animal studies adverse effects on embryofetal development were observed following administration of dihydroergotamine mesylate during pregnancy (decreased fetal body weight and/or skeletal ossification) in rats and rabbits or during pregnancy and lactation in rats (decreased body weight and impaired reproductive function in the offspring) in rats at doses less than those used clinically and which were not associated with maternal toxicity (see Data ).
Odhadovaná míra hlavních vrozených vad (NULL,2%až 2,9%) a potratu (17%) mezi dodávkami ženám s migrénou jsou podobné míře hlášeným u žen bez migrény. Všechna těhotenství mají na pozadí riziko ztráty vrozených vad nebo jiných nepříznivých výsledků. V americké obecné populaci je odhadované riziko na pozadí hlavních vrozených vad a potratů u klinicky uznávaných těhotenství 2% až 4% a 15% až 20%.
Data
Údaje o zvířatech
Intranazální podávání mesylátu dihydroergotaminu k těhotným potkanům během období organogeneze vedlo ke snížení tělesné hmotnosti plodu a/nebo kosterní ossifikace v dávkách 0,16 mg/den (spojené s plazmatickými expozicemi [AUC] méně než u lidí při maximální doporučené lidské dávce [MRHD] [MRHD] nebo vyšší. U potkanů nebyla identifikována úroveň toxicity embryfetální toxicity. Intranazální podávání mesylátu dihydroergotaminu na těhotné králíky v celé organogenezi vedlo ke snížení kosterní osifikace při 3,6 mg/den. Při dávce bez efektu (NULL,2 mg/den) pro nepříznivé účinky na vývoj embryfetálu u expozice plazmy králíků (AUC) byly menší než u lidí na MRHD.
Intranazální podávání dihydroergotaminu mesylátu na potkanské potkany během těhotenství a laktace vedlo ke snížení tělesné hmotnosti a zhoršené reprodukční funkce (snížené indexy páření) bylo pozorováno u potomků v dávkách 0,16 mg/den nebo vyšší. Nebyla stanovena dávka bez účinku pro nepříznivé vývojové účinky u potkanů.
Účinky na vývoj se objevily v dávkách pod těmi, které v těchto studiích poskytly důkazy o významné toxicitě matky.
Dihydroergotamin-indukovaná retardace růstu intrauterin byla přičítána sníženému průtoku krve uteroplacentální krve v důsledku prodloužené vazokonstrikce děložních cév a/nebo zvýšeného myometriálního tónu.
Laktace
Shrnutí rizika
Neexistují žádné údaje o přítomnosti dihydroergotaminu v lidském mléce; Ergotamin však související léčivo je přítomno v lidském mléce. Existují zprávy o zvracení průjmu slabý puls a nestabilní krevní tlak u kojených kojenců vystavených ergotaminu. Trudhesa může snížit zásobování mlékem, protože může snížit hladinu prolaktinu. Kvůli potenciálu sníženého dodávky mléka a závažných nežádoucích účinků u kojeného dítěte, včetně zvracení průjmu slabého pulsu a nestabilního krevního tlaku, doporučují pacientům kojit během léčby Trudhesou a po dobu 3 dnů po poslední dávce. Dodávka mateřského mléka během této doby by měla být čerpána a vyřazena.
Dětské použití
Bezpečnost a účinnost u pediatrických pacientů nebyla stanovena.
Geriatrické použití
Klinické studie Trudhesa a dalších dihydroergotaminových mesylátových produktů nezahrnuly dostatečný počet subjektů ve věku 65 a starších, aby se určily, zda reagují odlišně od mladších subjektů. Obecně by měl být výběr dávky pro staršího pacienta opatrný, obvykle začínající na dolním konci rozsahu dávkování, což odráží větší frekvenci snížené funkce ledvin nebo srdeční jater a souběžné onemocnění nebo jiné léčivé terapie.
Předávkovat Information for Trudhesa
Příznaky
Nadměrné dávky dihydroergotaminu mohou mít za následek periferní příznaky a příznaky ergotismu. Obecně jsou příznaky akutního předávkování Trudhesa podobné příznakům předávkování ergotaminem, i když může být méně výrazná nevolnost a zvracení s Trudhesou. Mezi příznaky předávkování ergotaminem patří následující: Nesvětlovost brnění bolesti a cyanóza končetin spojených se sníženými nebo chybějícími periferními pulzy; respirační deprese; zvýšení a/nebo snížení krevního tlaku obvykle v tomto pořadí; Zmatek delirium křeče a kóma; a/nebo určitý stupeň zvracení nevolnosti a bolesti břicha.
U laboratorních zvířat byl dihydroergotamin smrtelný, když byl podáván při intravenózních dávkách 44 mg/kg u myší 130 mg/kg u potkanů a 37 mg/kg u králíků.
Zacházení
Zacházení includes discontinuance of the drug local application of warmth to the affected area the administration of vasodilators a nursing care to prevent tissue damage. Up-to-date information about the treatment of overdosage can often be obtained from a certified Regional Poison Control Center.
Kontraindikace for Trudhesa
Trudhesa je kontraindikována u pacientů:
tropické místo
- Se souběžným použitím silných inhibitorů CYP3A4, jako jsou inhibitory proteázy (např. Ritonavir neelfinavir nebo neinavir) makrolidová antibiotika (např. Erythromycin nebo klarithromycin) a antifungály (ketoconazol nebo itrakonazol) [Viz) VAROVÁNÍS AND PRECAUTIONS a Lékové interakce ]
- S ischemickou srdeční chorobou (angina pectoris anamnéza infarktu myokardu nebo zdokumentovaná tichá ischemie) nebo pacienty, kteří mají klinické příznaky nebo nálezy konzistentní s vazospasmem koronární tepny včetně varianty Prinzmetalu [viz viz variantní angina [viz [viz VAROVÁNÍS AND PRECAUTIONS ]
- s nekontrolovanou hypertenzí [viz VAROVÁNÍS AND PRECAUTIONS ]
- s periferním arteriálním onemocněním
- se sepsou
- po vaskulární chirurgii
- s těžkým poškozením jater
- s těžkým poškozením ledvin
- se známou přecitlivělostí na ergot alkaloidy
- s nedávným použitím (tj. Do 24 hodin) od dalších 5-HT 1 Agonisté (např. Sumatriptan) nebo léky obsahující ergotamin nebo ergot [viz viz Lékové interakce ]
- Se souběžným použitím periferních a centrálních vazokonstriktorů, protože tato kombinace může vést k aditivnímu nebo synergickému zvýšení krevního tlaku [viz viz VAROVÁNÍS AND PRECAUTIONS ]
Klinická farmakologie for Trudhesa
Mechanismus působení
Dihydroergotamin se váže s vysokou afinitou k 5-HT 1DA a 5-HT 1db receptory. Terapeutická aktivita dihydroergotaminu v migréně je obecně připisována agonistickým účinkům na 5-HT 1d receptory.
Farmakodynamika
U pacientů s hypertenzí a bez ní bylo hlášeno významné zvýšení krevního tlaku [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Dihydroergotamin má oxytocické vlastnosti [viz viz VAROVÁNÍS AND PRECAUTIONS ].
Farmakokinetika
Vstřebávání
Průměrná doba od dávkování po maximální plazmatickou koncentraci po podání Trudhesa byl přibližně 0,5 hodiny.
Rozdělení
Dihydroergotamin Mesylát je vázán na 93% plazmatický protein. Zjevný distribuční objem v ustáleném stavu je přibližně 800 litrů.
Odstranění
Metabolismus
V lidské plazmě po perorálním podání byly identifikovány čtyři metabolity mesylátů dihydroergotaminu. Hlavní metabolit 8'-Hydroxy dihydroergotamin vykazuje afinitu ekvivalentní svému rodiči pro adrenergní a 5-HT receptory a prokazuje ekvivalentní účinnost v několika modelech venokomstrikční aktivity nadarmo a in vitro . Ostatní metabolity, tj. Dihydrolysová kyselina dihydrolysergík a metabolit vytvořený oxidačním otvorem prolinového kruhu, mají menší význam. Po celkové metabolitech po podání nosní představují pouze 20% až 30% plazmatické AUC. Systémová clearance dihydroergotaminového mesylátu po intravenózním a intramuskulárním podávání je 1,5 l/min. Kvantitativní farmakokinetická charakterizace čtyř metabolitů nebyla provedena.
Vylučování
Hlavní vylučovací trasa dihydroergotaminu je přes žluč ve stolici. Celková vůle těla je 1,5 l/min, což odráží hlavně jaterní vůli. Pouze 6% až 7% nezměněného dihydroergotaminu je po intramuskulární injekci vylučováno v moči. Rénální clearance (NULL,1 l/min) není ovlivněna cestou podávání dihydroergotaminu.
Průměrný zjevný poločas podávání nosního podávání Trudhesa u zdravých subjektů je přibližně 12 hodin.
Konkrétní populace
Nebyly provedeny žádné studie o vlivu renálního nebo jaterního poškození Genderová rasa Etnicita nebo těhotenství na farmakokinetiku dihydroergotaminu [viz viz Kontraindikace Použití v konkrétních populacích ].
Studie interakce léčiva
Inhibitory CYP3A4
Rare reports of ergotism have been obtained from patients treated with dihydroergotamine and macrolide antibiotics (e.g. clarithromycin erythromycin) and from patients treated with dihydroergotamine and protease inhibitors (e.g. ritonavir) presumably due to inhibition of CYP3A metabolism of ergotamine [see Kontraindikace ].
Jiné drogy
Farmakokinetika dihydroergotaminu se nezdálo, že by byla významně ovlivněna souběžným použitím místního vazokonstriktora.
Několik perorálních dávek antagonisty antagonisty P-adrenoceptoru propranololu použitého pro profylaxi migrény nemělo významný vliv na CMAX TMAX nebo AUC dihydroergotaminových dávek až do 4 mg. Propranolol však může zesílit vazokonstriktivní účinek ergotaminu [viz Lékové interakce ].
Účinek perorálních antikoncepcí na farmakokinetiku Trudhesa nebyl studován.
Klinické studie
Účinnost Trudhesa je založena na relativní biologické dostupnosti nosního spreje Trudhesa ve srovnání s dihydroergotaminovým mesylátovým nosním sprejem u zdravých subjektů.
Klinické studie popsané níže byly provedeny pomocí dihydroergotaminového mesylátového nosního spreje.
Účinnost nosního spreje mesylátového mesylátu dihydroergotaminu pro akutní léčbu migrénových bolesti hlavy byla hodnocena ve čtyřech randomizovaných dvojitě slepých placebech kontrolovaných studiích v USA. Populace pacientů pro studie byla převážně žena (87%) a bělošské (95%) s průměrným věkem 39 let (rozmezí 18 až 65 let). Pacienti léčili jednu střední až těžkou migrénu bolest hlavy s jednou dávkou studijních léků a posoudili závažnost bolesti během 24 hodin po léčbě. Reakce bolesti hlavy byla stanovena 0,5 1 2 3 a 4 hodiny po podání a byla definována jako snížení závažnosti bolesti hlavy na mírnou nebo žádnou bolest. Ve studiích 1 a 2 byla použita čtyřbodová stupnice intenzity bolesti; Ve studiích 3 a 4 byla použita pětibodová stupnice k zaznamenání reakce na bolest. Ačkoli bylo povoleno záchranné léky u všech čtyř studií Pacienti byli instruováni, aby je během čtyřhodinového pozorovacího období nepoužívali. Ve studiích 3 a 4 byla celková dávka 2 mg porovnána s placebem. Ve studiích byly hodnoceny 1 a 2 dávky 2 a 3 mg a nevykazovaly žádnou výhodu vyšší dávky pro jednu ošetření. Ve všech studiích pacienti dostávali režim sestávající z 0,5 mg v každé nosní nosní části opakované za 15 minut (a opět za dalších 15 minut pro 3 mg dávku ve studiích 1 a 2).
Procento pacientů, kteří dosáhli reakce na bolest hlavy 4 hodiny po léčbě, bylo významně vyšší u pacientů, kteří dostávali 2 mg dávky dihydroergotaminového mesylátového nosního spreje ve srovnání s těmi, kteří dostávali placebo ve 3 ze 4 studií (viz tabulka 2 a tabulka 3 a obrázek 1 a 2).
Tabulka 2 Studie 1 a 2: Procento pacientů s reakcí hlavy a 2 a 4 hodiny po jediné léčbě studijního léku (dihydroergotamin mesylát nosní sprej nebo placebo)
| N | 2 hodiny | 4 hodiny | ||
| Studie 1 | Nosní sprej dihydroergotaminu mesylátu | 105 | 61%** | 70%** |
| Placebo | 98 | 23% | 28% | |
| Rozdíl od placeba | 37% | 42% | ||
| Studie 2 | Nosní sprej dihydroergotaminu mesylátu | 103 | 47% | 56%* |
| Placebo | 102 | 33% | 35% | |
| Rozdíl od placeba | 14% | 21% | ||
| a Reakce bolesti hlavy byla definována jako snížení závažnosti bolesti hlavy na mírnou nebo žádnou bolest. Reakce bolesti hlavy byla založena na intenzitě bolesti, jak je pacientem interpretováno pomocí čtyřbodové stupnice intenzity bolesti. *Hodnota p <0.01 ** Hodnota p <0.001 |
Tabulka 3 Studie 3 a 4: Procento pacientů s reakcí hlavy a 2 a 4 hodiny po jediné léčbě studijního léku (dihydroergotamin mesylát nosní sprej nebo placebo)
| N | 2 hodiny | 4 hodiny | ||
| Studie 3 | Nosní sprej dihydroergotaminu mesylátu | 50 | 32 | 48%* |
| Placebo | 50 | 20% | 22% | |
| Rozdíl od placeba | 12% | 26% | ||
| Studie 4 | Nosní sprej dihydroergotaminu mesylátu | 47 | 30% | 47% |
| Placebo | 50 | 20% | 30% | |
| Rozdíl od placeba | 10% | 17% | ||
| a Reakce bolesti hlavy byla definována jako snížení závažnosti bolesti hlavy na mírnou nebo žádnou bolest. Odpověď bolesti hlavy byla vyhodnocena na pětibodové stupnici, která obsahovala reakci bolesti. *Hodnota p <0.01 |
Kaplan-meier grafy níže (obrázek 1 a obrázek 2) poskytují odhad pravděpodobnosti, že pacient bude reagovat na jednu 2 mg dávku dihydroergotaminového mesylátového nosního nosního nosu jako funkci času, která byla uplynuta od zahájení léčby.
Obrázek 1 Odhadovaná pravděpodobnost, že pacient reaguje během čtyř hodin po jedné 2 mg dávce dihydroergotaminového mesylátového nosního spreje jako funkce času, který uplynul od zahájení léčby*
| *Obrázek ukazuje pravděpodobnost v průběhu času získávání odpovědi po léčbě dihydroergotaminem mesylátovým nosním sprejem. Reakce bolesti hlavy byla založena na intenzitě bolesti, jak je pacienta interpretována pomocí čtyřpozidní stupnice intenzity bolesti. Pacienti, kteří nedosahují reakce do 4 hodin, byli cenzurováni na 4 hodiny. |
Obrázek 2 Odhadovaná pravděpodobnost, že pacient reaguje na nosní sprej mesylátu dihydroergotaminu během čtyř hodin po dávkování*
| *Obrázek ukazuje pravděpodobnost v průběhu času získávání odpovědi po léčbě dihydroergotaminem mesylátovým nosním sprejem. Odpověď bolesti hlavy byla vyhodnocena na pětibodové stupnici, která obsahovala reakci bolesti. Pacienti, kteří nedosahují reakce do 4 hodin, byli cenzurováni na 4 hodiny. |
U pacientů s nevolností a fonofobií spojenou s migrénou došlo k nižšímu výskytu těchto příznaků po 2 a 4 hodinách po podání nosního spreje mesylátu dihydroergotaminu ve srovnání s placebem.
Pacienti nebyli dovoleny používat další léčbu po dobu 8 hodin před dávkováním studie a během 4hodinové pozorovací doby po studijní léčbě. Po čtyřhodinovém období pozorování bylo pacientům dovoleno používat další léčbu. Pro všechny studie je odhadovaná pravděpodobnost pacientů užívajících další léčbu pro jejich migrény po dobu 24 hodin po jednorázové 2 mg dávce studijní léčby shrnuto na obrázku 3 níže.
Obrázek 3 Odhadovaná pravděpodobnost pacienta za použití další léčby pro migrénu po dobu 24 hodin po buď po buď dihydroergotaminové mesylátové nosní sprej 2 mg (nebo placebo)*
| *Kaplan-Meier graf založený na údajích získaných ze všech studií s pacienty, kteří nepoužívají další léčbu cenzurované do 24 hodin. Všichni pacienti dostali jedinou léčbu studijních léků pro jejich migrénní útok. Spiknutí také zahrnuje pacienty, kteří nehovořili žádnou reakci na počáteční dávku. |
Zdá se, že ani věk, ani sex neovlivňují reakci pacienta na nosní sprej dihydroergotaminu mesylátu. Rasové rozdělení pacientů nebylo dostatečné k určení účinku rasy na účinnost nosního spreje dihydroergotaminu mesylátu.
Informace o pacientovi pro Trudhesa
Trustla ™
(Trae - DEH - jeden)
(dihydroergotamin mesylát) nosní sprej
Jaké jsou nejdůležitější informace, které bych měl vědět o Trudhese?
Trudhesa může způsobit vážné vedlejší účinky včetně:
- Vážné problémy s krevním oběhem nohou a nohou (periferní ischemie). Trudhesa může způsobit periferní ischemii, když ji užíváte s určitými léky známými jako inhibitory CYP3A4. Periferní ischemie může vést k mrtvici a smrti. Pokud máte některý z následujících příznaků, přestaňte brát Trudhesa a okamžitě získejte pohotovostní lékařskou pomoc:
- křeče a bolest v nohou nebo bokech
- Pocit těžkosti nebo těsnosti ve svalech nohou
- pálení nebo bolavé bolesti na nohou nebo na nohou při odpočinku
- otupělost brnění nebo slabosti v nohou
- Změny studené nebo barvy v 1 nebo obou nohou nebo nohách
- Slurred řeč
- náhlá slabost
Nebere léky známé jako silné inhibitory CYP3A4, jako jsou:
-
- Ritonavir
- Erythromycin
- Ketokonazol
- Netfinavir
- Clarithromycin
- Itraconazole
Nejedná se o všechny léky, které by mohly ovlivnit to, jak Trudhesa funguje. Váš poskytovatel zdravotní péče vám může říct, zda je bezpečné brát Trudhesa s jinými léky.
Co je Trudhesa?
Trudhesa je lék na předpis používaný pro akutní léčbu migrény s aurou nebo bez aury u dospělých.
- Trudhesa se nepoužívá k prevenci migrény.
- Trudhesa se nepoužívá k léčbě jiných typů bolesti hlavy, jako je hemiplegická (díky nimž se nemůžete pohybovat na jedné straně těla) nebo bazilar (vzácná forma migrény s aurou) migrény.
Není známo, zda je Trudhesa u dětí bezpečná a efektivní.
Neberte si Trudhesa, pokud:
- užívají léky známé jako silné inhibitory CYP3A4.
- mít srdeční problémy nebo historii srdečních problémů.
- mají nekontrolovaný vysoký krevní tlak.
- Zúžení krevních cév v nohách ARMES AUGBEL nebo ledviny (periferní vaskulární onemocnění).
- mít sepsu.
- měli vaskulární chirurgii.
- mají závažné problémy s jatery.
- mají závažné problémy s ledvinami.
- jsou alergické na alkaloidy mesylátu dihydroergotaminu mesylátu nebo jakékoli složky v Trudhesa. Úplný seznam složek naleznete na konci této příručky k léku.
- vzali některou z následujících léků za posledních 24 hodin:
- Sumatriptan
- Almotriptan
- ELETRIPTAN
- frovatriptate
- Naratriptan
- Rizatriptan
- léky typu ergotaminu nebo ergotaminu
- vzali jakékoli léky, které omezují vaše krevní cévy nebo zvyšují krevní tlak.
Zeptejte se svého poskytovatele zdravotní péče, zda si nejste jisti, zda užíváte některý z těchto léků. Váš poskytovatel zdravotní péče vám může říct, zda je bezpečné brát Trudhesa s jinými léky.
Než vezmete Trudhesa, řekněte svému poskytovateli zdravotní péče o všech svých zdravotních stavech, včetně, pokud jste:
- mít vysoký krevní tlak.
- mít problémy s jatery.
- mít problémy s ledvinami.
- kouř.
- jsou těhotné nebo plánují otěhotnět. Trudhesa může způsobit předčasnou práci. Během těhotenství by se mělo zabránit Trudhesa. Pokud jste těhotná nebo chcete otěhotnět, promluvte si se svým poskytovatelem zdravotní péče.
- jsou kojení nebo plánují kojení. Trudhesa může snížit přísun mateřského mléka a přejít do mateřského mléka. Trudhesa může být pro vaše dítě škodlivá. Při užívání Trudhesa a po dobu 3 dnů po použití Trudhesa nekobejte své dítě. Promluvte si se svým poskytovatelem zdravotní péče o nejlepším způsobu, jak nakrmit své dítě, pokud si vezmete Trudhesa.
Řekněte svému poskytovateli zdravotní péče o všech lécích, které užíváte včetně předpisu a volně prodejných léků vitamínů a bylinných doplňků. Váš poskytovatel zdravotní péče se rozhodne, zda si můžete vzít Trudhesa s dalšími léky.
Zejména řekněte svému poskytovateli zdravotní péče, pokud vezmete:
-
- Sumatriptan
- flukonazol
- propranolol nebo jiné léky, které mohou snížit vaši srdeční frekvenci
- Lékař ergot typu O Grapefruitová šťáva o jakékoli léky, které mohou zvýšit váš krevní tlak
- Saquinavir o Zileuton o Selektivní serotonin zpětný vychytávání inhibitory
- nefazodon
- nikotin
Nejedná se o všechny léky, které by mohly ovlivnit to, jak Trudhesa funguje. Váš poskytovatel zdravotní péče vám může říct, zda je bezpečné brát Trudhesa s jinými léky.
Jak mám brát Trudhesa?
- Někteří lidé by měli vzít svou první dávku Trudhesa v kanceláři své lékaře nebo v jiném lékařském prostředí. Zeptejte se svého lékaře, zda byste měli vzít svou první dávku v lékařském prostředí.
- Použijte Trudhesa přesně tak, jak vám říká váš poskytovatel zdravotní péče, abyste ji používali. Přečtěte si a postupujte podle pokynů v Pokyny pro použití který má před použitím balíček Trudhesa.
- Trudhesa byste měli používat, jakmile se příznaky bolesti hlavy začnou, ale může být podána kdykoli během migrény.
- Po sestavení Trudhesa dohromady a nasazení zařízení na postřikování zařízení 1 do každé nosní dírky (kompletní dávka).
- Pokud se vaše bolest hlavy vrátí po první úplné dávce nebo získáte jen určitou úlevu od bolesti hlavy, můžete použít druhou dávku 1 hodinu po první úplné dávce. Pro druhou dávku použijte nové nosní stříkací zařízení Trudhesa.
- Nepoužívejte více než 2 dávky trudhesa během 24 hodin nebo 3 dávek během 7denního období.
- Trudhesa po dobu 10 a více dní za 1 měsíc může zhoršit bolesti hlavy. Měli byste si zapisovat, když máte bolesti hlavy a když si vezmete Trudhesa, abyste mohli mluvit se svým poskytovatelem zdravotní péče o tom, jak Trudhesa pro vás pracuje.
Jaké jsou možné vedlejší účinky Trudhesa?
Trudhesa může způsobit vážné vedlejší účinky včetně:
Vidět Jaké jsou nejdůležitější informace, které bych měl vědět o Trudhese?
- Srdeční infarkt a další srdeční problémy. Srdeční problémy mohou vést k smrti. Přestaňte brát Trudhesa a okamžitě získat pohotovostní lékařskou pomoc, pokud máte některý z následujících příznaků a infarkt :
- nepohodlí ve středu hrudníku, který trvá déle než několik minut nebo který zmizí a vrátí se zpět
- Těžká těsnost tlak bolesti nebo těžkosti v krku nebo čelisti na hrudi
- Bolest nebo nepohodlí v náručí zadní čelist nebo žaludek
- dušnost s nepohodlí na hrudi nebo bez něj
- vypuknutí studeného potu
- nevolnost or zvracení
- Cítit se smazeným
Trudhesa není pro lidi s rizikovými faktory pro srdeční choroby, pokud není provedena srdeční zkouška a nevykazuje žádný problém. Máte vyšší riziko pro srdeční choroby, pokud:
-
- mít vysoký krevní tlak
- mají vysokou hladinu cholesterolu
- kouř
- mají nadváhu
- mít cukrovku
- mít rodinnou anamnézu srdečních chorob
- Mrtvice. Přestaňte brát Trudhesa a okamžitě získejte pohotovostní lékařskou pomoc, pokud máte některý z následujících příznaků mrtvice:
- Trvá poklesená
- neobvyklá slabost nebo otupělost
- Slurred řeč
- Změny barvy nebo pocitu v prstech a nohou (Raynaudův syndrom).
- Problémy s žaludkem a střevem (Gastrointestinální a tlusté ischemické události). Mezi příznaky gastrointestinálních a tlustých ischemických událostí patří:
- náhlá nebo těžká bolest žaludku
- zácpa nebo průjem
- bolest žaludku po jídle
- Krvavý průjem
- hubnutí
- horečka
- nevolnost or zvracení
- Zvýšit krevní tlak.
- Nadměrná bolest hlavy. Někteří lidé, kteří používají příliš mnoho Trudhesa, mohou zhoršit bolesti hlavy (nadužívá bolest hlavy). Pokud se vaše bolesti hlavy zhorší, váš poskytovatel zdravotní péče se může rozhodnout zastavit léčbu Trudhesa.
- Předčasná práce.
- Změny tkáně (fibrotické komplikace). Kolem plic a žaludku se může vyskytnout nflamová a vlákninová tkáň, která není normální (fibróza).
- Spalování pocitů v ústech nosu a krku a abnormální chuti.
Mezi nejčastější vedlejší účinky Trudhesa patří:
- rýma nosu
- Reakce webu aplikací
- ospalost
- nevolnost
- závrať
- bolest v krku
- Abnormální chuť
- zvracení
- průjem
Nejedná se o všechny možné vedlejší účinky Trudhesa.
Zavolejte svého lékaře, kde najdete lékařskou radu ohledně vedlejších účinků. Můžete nahlásit vedlejší účinky FDA na 1-800-FDA-1088.
Jak mám ukládat Trudhesa?
Udržujte Trudhesa od tepla a světla.
- Ukládejte trudhesa při teplotě místnosti mezi 68 ° F až 77 ° F (20 ° C až 25 ° C).
- Neomeďte se ani zamrzněte.
- Po otevření lahvičky Trudhesa musí být vyhozena po 8 hodinách.
Udržujte Trudhesa a všechny léky mimo dosah dětí.
Nehodí Trudhesa do ohně nebo spaloven, protože kanystr uvnitř zařízení může explodovat.
Obecné informace o bezpečném a efektivním používání Trudhesa.
Léky jsou někdy předepisovány pro jiné účely než ty, které jsou uvedeny v průvodci s léky. Nepoužívejte Trudhesa pro podmínku, pro kterou nebyla předepsána. Nedávejte Trudhesu jiným lidem, i když mají stejné příznaky, jaké máte. Může jim to poškodit. Můžete požádat svého lékárníka nebo poskytovatele zdravotní péče o informace o Trudhesa, která je psána pro zdravotnické pracovníky.
Jaké jsou ingredience v Trudhesa?
Aktivní složka: Dihydroergotamin Mesylát
Neaktivní ingredience: Kofein oxid uhličitý dextróza a voda. Námořní nádoba na nosní rozprašovací zařízení obsahuje hnutí hydrofluoroalkane-134a (HFA). Začtení lahvičky není vyrobeno z latexu přírodního gumy. Trudhesa je ochranná známka společnosti Impel Neuropharma Inc.
Tento průvodce medikací byl schválen americkou správou potravin a léčiv.
Pokyny pro použití
Trustla ™
(roe-sa)
(Dihydroergotamin Mesylát)
nosní sprej
Pouze pro nosní použití
Zavedení
Přečtěte si tyto pokyny pro použití, než začnete používat Trudhesa a pokaždé, když získáte doplnění předpisu. Mohou existovat nové informace.
Tyto informace nezavazují místo rozhovoru se svým poskytovatelem zdravotní péče o vašem zdravotním stavu nebo léčbě. Vy a váš poskytovatel zdravotní péče byste měli mluvit o Trudhese, když ji začnete přijímat a při pravidelných kontrolách.
Je důležité tyto pokyny přesně postupovat podle toho, abyste získali správnou dávku. Kontaktujte svého poskytovatele zdravotní péče, pokud máte nějaké dotazy ohledně toho, jak tento produkt používat.
 |
Díly nosního stříkacího zařízení
 |
Díly skleněných lahviček
 |
Důležité informace, které potřebujete vědět před dávkováním s Trudhesa
- Pouze pro nosní použití.
- Před dávkováním vždy zařaďte nosní sprejové zařízení čerpaním prstů a skleněnou lahvičkou dohromady přesně čtyřikrát
- Účelem aktivace je přivést lék na špičku stříkací trysky. Můžete nebo nemusíte vidět, jak kapalina nebo sprej vychází z trysky během každé aktivační akce.
- Během primingmake se určitě zaměřte na stříkací trysku od tváře a všeho, co nechcete přijít do kontaktu se stříkáním medicíny.
- Kompletní dávka je 2 spreje; 1 sprej v každé nosní díře.
- Ne Vezměte více než 2 dávky během 24 hodin. Ne Vezměte více než 3 dávky za 7denní období.
- Při podpření a při podávání a při podání při podávání a při podávání.
- Tento produkt s nosním rozprašovacím zařízením je jednou dávkou (pouze pro jednu kompletní dávku) a po použití by měl být vyhozen (vyřazen). Pro každou dávku budete potřebovat novou soupravu.
- Udržujte produkt v případě, dokud není připraven k použití.
- Poté, co byla otevřená lahvička Trudhesa, musí být po 8 hodinách vyhozena.
- Ne Otevřete skleněnou lahvičku a vystavte vzduchu, dokud není připraven k použití.
- Uložte při pokojové teplotě v čistém suchém prostoru.
- Ne Použijte, pokud je produkt poškozen.
- Ne Použijte, pokud je produkt vypršen.
- Každá skleněná lahvička a nosní stříkací zařízení lze použít pouze 1krát. Po dávkování zahodí celé nosní stříkací zařízení bez odstranění skleněné lahvičky.
- Pokud přetrvávají vaše příznaky, můžete vzít další úplnou dávku alespoň 1 hodinu po první dávce.
Skladování Trudhesa
- Ukládejte trudhesa při teplotě místnosti mezi 68 ° F až 77 ° F (20 ° C až 25 ° C).
- Uložte Trudhesa v původním obalu v čisté oblasti od tepla a světla ( Obrázek a ).
- Udržujte Trudhesa v původním obalu, dokud nebudete připraveni k použití.
- Ne Chladit nebo zamrznout Trudhesa.
- Udržujte Trudhesa a všechny léky mimo dosah dětí.
 |
Příprava na dávku s Trudhesa
Krok 1: Shromažďujte a zkontrolujte zásoby
 |
 |
- Zkontrolujte, zda pro svou migrénu používáte správný lék (viz Obrázek b ).
- Zkontrolujte, zda se ujistěte, že Trudhesa nevyprší (EXP) (viz Obrázek c ).
- Pokud vyprší vypršen odhodit a získat novou skleněnou lahvičku.
- Zkontrolujte, zda skleněná lahvička a modrý plastový kryt nevypadají poškozeně.
Krok 2: Odstraňte modrou plastovou krycího fólie a šedou gumovou zátku ze skleněné lahvičky
 |
 |
 |
- Odstraňte (otočte) modrý plastový kryt ze skleněné lahvičky (viz Obrázek d ).
- Použijte modrý plastový kryt, abyste pomalu odlupovali kovovou fólii z šedé gumové zátky v kruhovém pohybu (viz viz Obrázek e ).

- Vytáhněte šedou gumovou zátku nahoru a ven ze skleněné lahvičky ( Obrázek f a Obrázek g ).
- Vyhoďte (zlikvidujte) zakryjte fólii a šedou gumovou zátku do koše.
Krok 3: Odstraňte čirý plastový kryt z nosního stříkacího zařízení
- Podržte vzpřímené zařízení pro nosální sppla.
- Vytáhněte na čirý plastový kryt a vyjměte jej z nosního stříkacího zařízení ( Obrázek h ).
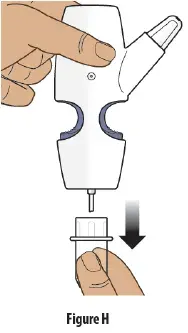
- Vyhoďte drahý plastový kryt.
Krok 4: Skleněné lahvičky zašroubujte do nosního stříkacího zařízení
 |
 |
- Držte vzpřímené přípravové zařízení.
- Jemně zatlačte skleněnou lahvičku do dna nosního sparayho zařízení (viz Obrázek i ) a zašroubujte to, dokud není zabezpečen, jak je znázorněno v Obrázek J. .
Krok 5: Prime the nosní sprejové zařízení čerpání čtyřikrát prsty a palcem
 |
- Držte nosní stříkací zařízení sloupek .
- Umístěte stříkací trysku pryč od obličeje.
- Umístěte palec na dno skleněné lahvičky a položte ukazatel (index) a střední prsty na úchopy prstů (viz Obrázek k ).
- Čerpejte nosní stříkací zařízení přesně čtyřikrát.
- Pro čerpání nosního stříkacího zařízení pevně stiskněte dowm prstů a zároveň stiskněte skleněnou lahvičku. Pak uvolněte (viz Obrázek k )
- Během aktivace můžete vidět nějaký lék. To je normální. Je to v pořádku, pokud nevidíte rozprašování léků na prvních několika čerpacích.
Důležitý tip: Účelem aktivace je přivést lék na špičku stříkací trysky. Pokud neomezujete nosní sprejové zařízení, nedostanete správnou dávku léku.
Před použitím vždy připravujte nosní stříkací zařízení přesně čtyřikrát.
Během aktivace nezapomeňte zamířit trysku od tváře a cokoli, co nechcete přijít do kontaktu se sprejem medicíny.
Pomocí Trudhesa
Krok 6: Umístěte nosní sprejové zařízení
 |
- Otočte nebo otočte nosní sprey zařízení tak, aby vám rozprašovací tryska směřovala.
- Ujistěte se, že je hlava rovná a nosní stříkací zařízení je vzpřímené.
- Vložte trysku Sparay do první nosní dírky, pokud jde o pohodlí (viz Obrázek l ).
Krok 7: Nastříkejte první sprej do 1 nosní dírky
- Pevně stiskněte prst uchopit dolů a zároveň stiskněte skleněnou lahvičku, abyste dodali první sprej (viz Obrázek m ).Then release.
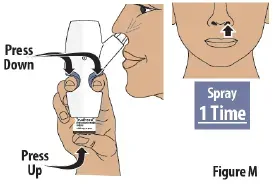
- Do této nosní dírky dodávejte pouze 1 sprej.
Krok 8: Nastříkejte druhý sprej do jiné nosní dírky
- Přesuňte stříkací trysku do druhé nosní dírky.
- Pevně stiskněte prst uchopení dolů a zároveň stiskněte skleněnou lahvičku, abyste dodali druhý sprej (viz viz Obrázek n ).Then release.
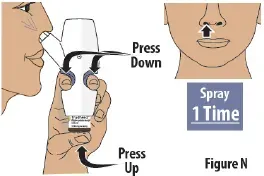
- Do této nosní dírky dodávejte pouze 1 sprej.
Důležitý tip: Kompletní dávka je 2 spreje; 1 sprej v každé nosní díře.
Výhody a vedlejší účinky černého pepře a vedlejší účinky
Ne Vezměte více než 2 dávky během 24 hodin. Ne Vezměte více než 3 dávky za 7denní období.Please refer to the prescribing information for more information.
Čichání během nebo po dávkování není nutné.
Důležité často kladené otázky (FAQ)
Otázka: Mohu uložit lék přeskakováním 4 čerpadel v „Kroku 5: Prime the Nove Spray Device“?
Odpověď: Žádné přeskakování 4 čerpadel, aby se upravilo, může mít přípravu nosního stříkaného zařízení k tomu, abyste nedostali správnou dávku medicíny.
Qestion: Když jsem poprvé načerpal nosní sprejové zařízení, abych připravil, zdálo se, že se nic nestane. Proč?
Odpověď: Účelem primingu je přivést lék na špičku trysky. I když na svém prvním čerpadlu nebo dvou nemusíte nic vidět ani neslyšíte, čerpací akce přesune lék ze skleněné lahvičky skrz vnitřek nosního stříkacího zařízení a do trysky. Měli byste vidět sprej svým čtvrtým pokusem z čerpadla.
Otázka: Mohu znovu použít nosní sprejové zařízení novou skleněnou lahvičkou?
Odpověď: Nic nosního stříkacího zařízení je pouze pro jednorázové použití a musí být odhozeno pryč po uzavření (1 sprej v každé nosní dírce). Je to proto, že zařízení může ucpat. Po dávkování skleněné lahvičky zašroubované na nosní stříkací zařízení a zahodí sestavené nosní stříkací zařízení do odpadku. Nepřekračujte žádnou část produktu.
Otázka: Mohu použít lék, který zůstává ve skleněné lahvičce pro pozdější dávku?
Odpověď: Neexistování, i když je nrmální, aby nějaký lék zůstal ve skleněné lahvičce, nelze použít pro pozdější dávkování. Který zbývající lék se stane neúčinným.
OTÁZKA: Co se stane, když Sparay více než jednou ve stejné nosní díře?
Odpověď: Kompletní a správná dávka je jeden sprej do každé nosní dírky. Není ve vás dávka jiná nosní dírka, pokud jste již dvakrát nastříkali v jedné nosní dírce.
Otázka: Jak brzy mohu vzít další dávku, pokud nedostávám úlevu od mé migrény?
Odpověď: Pokud vaše příznaky přetrvávají, můžete vzít další dávku nejméně 1 hodinu po první dávce. Ne Vezměte více než 2 dávky během 24 hodin. Ne Vezměte více než 3 dávky za 7denní období.Please refer to the prescribing information for more information.
Tyto pokyny pro použití byly schváleny společností U.S.Food a Drug Administration.




