Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
ProgestinsKyleena
Shrnutí drog
Co je Kyleena?
Kyleena (levonorgestrel -releasující intrauterinní systém) je intrauterinní systém obsahující progestin (IUS), který je označen pro prevenci těhotenství po dobu až 5 let.
Jaké jsou vedlejší účinky Kyleeny?
Kyleena může způsobit vážné vedlejší účinky včetně:
- Zvýšené vaginální krvácení
- Bolest břicha nebo bolest pánve
- Vyhoštění měny
- akné a
- Menstruační křeče
Získejte lékařskou pomoc okamžitě, pokud máte výše uvedené příznaky.
Mezi běžné vedlejší účinky Kyleeny patří:
- vaginální svědění a vypouštění
- ovariální cysty
- Bolest břicha
- pánevní bolest
- Bolest hlavy nebo migréna
- akné
- Abdominální křeče
- Bolest prsu nebo nepohodlí
- Zvýšené vaginální krvácení
- deprese a
- Vypadávání vlasů.
Pokud máte následující vážné vedlejší účinky, vyhledejte lékařskou péči nebo zavolejte na číslo 911:
- Vážné příznaky očí, jako je ztráta náhlého vidění rozmazané vidění vidění Vision Vision Eye Eye Eye Eye Eye Eye Eye Eye nebo vidět halos kolem světel;
- Vážné příznaky srdce, jako je rychlé nepravidelné nebo bušení srdečního rytmu; třepování v hrudi; dušnost; a náhlé závratě lightheadness nebo omdlení;
- Těžká zmatek bolesti hlavy zkroucený řečový rameno nebo slabost nohou Potíže se ztrátou chůze pocitu koordinace Pocit nestabilní velmi tuhé svaly vysoké horečky bohaté pocení nebo třes.
Tento dokument neobsahuje všechny možné vedlejší účinky a mohou dojít k jiným. Další informace o vedlejších účincích najdete u svého lékaře.
Dávkování pro Kyleenu
Kyleena je vložena vyškoleným poskytovatelem zdravotní péče. Míra uvolňování levonorgestrelu (LNG) v Kyleeně je 17,5 mcg/den po 24 dnech a klesá na 7,4 mcg/den po 5 letech; Kyleena musí být odstraněna nebo vyměněna po 5 letech.
IV tekutiny pro dehydratační vedlejší účinky
Jaké léčivé látky nebo doplňky interagují s Kyleenou?
Kyleena může interagovat s jinými drogami. Řekněte svému lékaři všechny léky a doplňky, které používáte.
Kyleena během těhotenství a kojení
Před použitím Kyleeny řekněte svému lékaři, pokud jste těhotná. Kyleena se nedoporučuje pro použití během těhotenství. Kyleena by měla být odstraněna, pokud dojde k těhotenství u Kyleeny na místě. Před kojením se poraďte se svým lékařem.
Další informace
Naše Kyleena (levonorgestrel uvolňující intrauterinní systém) vedlejší účinky léčivé centrum poskytuje komplexní pohled na dostupné informace o možných vedlejších účincích při užívání tohoto léku.
Informace o drogách FDA
Popis pro Kyleenu
Kyleena (levonorgestrel uvolňující intrauterinní systém) obsahuje 19,5 mg LNG A progestinu a má za cíl poskytnout počáteční rychlost uvolňování přibližně 17,5 mcg/den LNG po 24 dnech.
Levonorgestrel USP (-)-13-ethyl-17-hydroxy-1819-dinor-18a-pregn-4-20-y-y-3-one aktivní složka v Kyleeně má molekulovou hmotnost 312,4 A molekulární vzorec C C C 21 H 28 O 2 a následující strukturální vzorec:
 |
Kyleena
Kyleena consists of a T-shaped polyethylene frame (T-body) with a steroid reservoir (hormone elastomer core) around the vertical stem. The white T-body has a loop at one end of the vertical stem a two horizontal arms at the other end. The reservoir consists of a whitish or pale yellow cylinder made of a mixture of LNG a silicone (polydimethylsiloxane) containing a total of 19.5 mg LNG. The reservoir is covered by a semi-opaque silicone membrane composed of polydimethylsiloxane a colloidal silica. A ring composed of 99.95% pure silver is located at the top of the vertical stem close to the horizontal arms a is visible by ultrasound. The polyethylene of the T-body is compounded with barium sulfate which makes it radiopaque. A monofilament blue polypropylene removal thread is attached to a loop at the end of the vertical stem of the T-body. The polypropylene of the removal thread contains <0.5% phthalocyaninato(2-) copper as a colorant (see Figure 10).
Komponenty Kyleeny včetně jejího obalu nejsou vyráběny pomocí přírodního gumového latexu.
Obrázek 10: Kyleena
 |
Vložení
Kyleena is packaged sterile within an inserter. The inserter (Figure 11) which is used for insertion of Kyleena into the uterine cavity consists of a symmetric two-sided body a slider that are integrated with flange lock pre-bent insertion tube a plunger. The outer diameter of the insertion tube is 3.8 mm. The vertical stem of Kyleena is loaded in the insertion tube at the tip of the inserter. The arms are pre-aligned in the horizontal position. The removal threads are contained within the insertion tube a hale. Once Kyleena has been placed the inserter is discarded.
Obrázek 11: Schéma inserturu
 |
Použití pro Kyleenu
Kyleena is indicated to prevent pregnancy for up to 5 years. Replace the system after 5 years if continued use is desired.
Dávkování pro Kyleenu
Dávkování v průběhu času
Kyleena contains 19.5 mg of Levonorgestrel (LNG) released nadarmo po 24 dnech přibližně 17,5 mcg/den. Tato sazba se postupně snižuje na 9,8 mcg/den po 1 roce a na 7,4 mcg/den po 5 letech. Průměr nadarmo Míra uvolňování LNG je přibližně 12,6 mcg/den během prvního roku a 9,0 mcg/den po dobu 5 let. [Vidět Klinická farmakologie ]
Kyleena must be removed by the end of the fifth year a can be replaced at the time of removal with a new Kyleena if continued contraceptive protection is desired.
Kyleena can be physically distinguished from other intrauterine systems (IUSs) by the combination of the visibility of the silver ring on ultrasound a the blue color of the removal threads.
Kyleena is supplied in a sterile package within an inserter that enables single-haed loading (see Figure 1). Do not open the package until required for insertion [see POPIS ]. Nepoužívejte, pokud je těsnění sterilního balíčku narušeno nebo se zdá být ohroženo. V průběhu postupu vložení používejte přísné aseptické techniky [viz Varování a preventivní opatření ].
 |
Pokyny pro vložení
- Získejte úplnou lékařskou a sociální historii, abyste určili podmínky, které by mohly ovlivnit výběr intrauterinního systému uvolňujícího levonorgestrel (LNG IUS) pro antikoncepci. Pokud je uvedeno, proveďte fyzické vyšetření a vhodné testy pro jakékoli formy genitálií nebo jiných sexuálně přenosných infekcí. [Vidět Kontraindikace a Varování a preventivní opatření ] Protože nepravidelné krvácení/špinění je běžné během prvních měsíců Kyleeny používat endometriální patologii (polypy nebo rakovina) před vložením Kyleeny u žen s přetrvávajícím nebo netypickým krvácením [viz viz [viz Varování a preventivní opatření ].
- Postupujte podle pokynů pro vložení přesně tak, jak je popsáno, abyste zajistili správné umístění a vyhnuli se předčasnému uvolnění Kyleeny z inserturu. Po vydání Kyleeny nelze znovu načíst.
- Před zahájením vložení zkontrolujte datum vypršení platnosti Kyleeny.
- Kyleena should be inserted by a trained healthcare provider. Healthcare providers should become thoroughly familiar with the insertion instructions before attempting insertion of Kyleena.
- Vložení může být spojeno s určitou bolestí a/nebo krvácení nebo vazovagální reakce (například synkopa bradykardie) nebo se záchvaty zejména u pacientů s predispozicí k těmto podmínkám. Zvažte podávání analgetik před vložením.
Načasování inzerce
Tabulka 1: Kdy vložit Kyleenu
| Zahájení Kyleeny u žen v současné době nepoužívá hormonální nebo intrauterinní antikoncepci |
|
| Přechod na Kyleenu z ústní transdermální nebo vaginální hormonální antikoncepce |
|
| Přechod na Kyleenu z injekční antikoncepce progestinu |
|
| Přechod na Kyleenu z antikoncepčního implantátu nebo jiného IUS |
|
| Vložení Kyleeny po potratu nebo potratu prvního trimestru |
|
| Vložení Kyleeny po porodu nebo potrat nebo potratu ve druhém trimestru | |
|
|
| Inzerce intervalu po úplném invociuti dělohy |
|
Nástroje pro vložení
Poznámka
Vložení poskytnuté s Kyleenou (viz obrázek 1) a postup vložení popsaný v této části nelze použít pro okamžité vložení po porodu nebo potratu nebo potratu druhého trimestru. Pro okamžité vložení odstraňte Kyleenu z inserturu prvním zatížením (viz obrázek 2) a poté uvolnění (viz obrázek 7) Kyleena z inserturu a vložte podle akceptované praxe.
Příprava
- Rukavice
- Spekulum
- Sterilní zvuk dělohy
- Sterilní tenaculum
- Aplikátor antiseptického roztoku
Postup
- Sterilní rukavice
- Kyleena with inserter in sealed package
- Nástroje a anestezie pro paracervikální blok, pokud se očekávají
- Zvažte, zda máte k dispozici neotevřenou záložní Kyleenu
- Sterilní ostré zakřivené nůžky
Příprava for insertion
- Vyloučte těhotenství a potvrďte, že k použití Kyleeny neexistují žádné další kontraindikace.
- S pacientem pohodlně v litotomické poloze proveďte bimanuální zkoušku, aby vytvořili tvar velikosti a polohu dělohy.
- Jemně vložte spekulum pro vizualizaci děložního čípku.
- Důkladně očistěte děložník a vaginu vhodným antiseptickým roztokem.
- Připravte se na zvuk dutiny dělohy. Uchopte horní ret cervixu s tenakulu a jemně aplikujte trakci, aby stabilizoval a zarovnal děložní kanál s děložní dutinou. V případě potřeby proveďte paracervikální blok. Pokud je děloha retrovertována, může být vhodnější uchopit spodní ret děložního čípku. Tenaculum by mělo zůstat v poloze a jemná trakce na děložním čípku by měla být udržována během postupu vložení.
- Jemně vložte zvuk dělohy a zkontrolujte průchodnost děložního čípku měření hloubky dutiny dělohy v centimetrech potvrďte směr dutiny a detekujte přítomnost jakékoli anomálie dělohy. Pokud se setkáte s obtížemi nebo cervikální stenózou, použijte dilataci a nikoli nutí k překonání rezistence. Pokud je vyžadována dilatace děložního čípku, zvažte použití paracervikálního bloku.
Postup vložení
Pokračujte s vložením až po dokončení výše uvedených kroků a zjistěte, že pacient je vhodný pro Kyleenu.
Zajistěte použití aseptické techniky během celého postupu.
Krok 1 - otevření balíčku
Obrázek 1.. Otevření balíčku Kyleena
 |
- Otevřete balíček (obrázek 1). Obsah balíčku je sterilní.
- Pomocí sterilních rukavic zvedněte rukojeť sterilního vložení a vyjměte ze sterilního balíčku.
Krok 2 - založte Kyleenu do inzerční trubice
Obrázek 2. Přesuňte posuvník až do přední pozice a načte Kyleenu
 |
- Stiskněte posuvník vpřed Pokud je to možné ve směru šipky, čímž se pohybuje trubici vložení přes Kyleena T-těles, aby naložil Kyleenu do vložení trubice (obrázek 2). Špičky paží se setkávají a vytvoří zaoblený konec, který mírně přesahuje zavedení trubice.
- Na posuvníku udržujte tlak vpřed palcem nebo ukazováčkem. V tuto chvíli nepohybujte posuvník dolů, protože to může předčasně uvolnit vlákna Kyleeny. Jakmile je posuvník přesunut pod značkou Kyleena, nelze znovu načíst.
Krok 3 - Sestavení příruby
- Držení jezdce v této dopředné poloze Nastavte horní okraj příruby tak, aby odpovídala hloubce dělohy (v centimetrech) měřenou během zvuku (obrázek 3).
Obrázek 3. Nastavení příruby
 |
Krok 4 - Kyleena je nyní připravena k vložení
- Pokračujte v držení jezdce v této poloze vpřed. Pokročte inserter skrz děložník, dokud příruba není přibližně 1,5–2 cm od děložního čípku a poté pozastavení (obrázek 4).
Obrázek 4. Pokrok v inzerční trubici, dokud příruba není 1,5 až 2 cm od děložního čípku
 |
Nenuťte vložení. Pokud je to nutné, rozšířte cervikální kanál.
Krok 5 - Otevřete paže
- Zatímco držíte vložení Přesuňte posuvník dolů na značku pro uvolnění ramen Kyleeny (obrázek 5). Počkejte 10 sekund, než se vodorovná ramena úplně otevřou.
Obrázek 5. Přesuňte jezdec zpět na značku a otevřete paže
 |
Krok 6 - Příspěvek na pozici Fundal
Jemně postupovat vložení do fundusu dělohy Dokud se příruba nedotkne děložního čípku. Pokud narazíte na rezistenci na fundál, nepostupujte. Kyleena je nyní v poloze fundálu (obrázek 6). Pro zabránění vyhoštění je důležité umístění fundálu Kyleeny.
Obrázek 6. Přesuňte Kyleenu v pozici fundálu
 |
Krok 7 - Uvolněte Kyleenu a stáhněte vložení
Obrázek 7. Přesuňte jezdec celou cestu dolů a uvolní Kyleenu z inzerční trubice
 |
Obrázek 8. Řezání vláken
 |
- Držení celého vložení pevně na místě uvolňuje Kyleena pohybem posuvník celou cestu dolů (Obrázek 7).
- Pokračujte v držení jezdce po celou cestu dolů, zatímco pomalu a jemně stáhnete vložení z dělohy.
- Pomocí ostré zakřivené nůžky nařízne vlákna Kolmé ponechání asi 3 cm viditelné mimo děložníku [řezací vlákna v úhlu může zanechat ostré konce (obrázek 8)]. Při řezání nepoužívejte napětí ani netahujte na vlákny, abyste zabránili posunu Kyleeny.
Kyleena insertion is now complete. Prescribe analgesics if indicated. Record the Kyleena lot number in the patient records.
Důležité informace, které je třeba zvážit během inzerce nebo po něm
- Pokud máte podezření, že Kyleena není ve správném umístění kontroly polohy (například pomocí transvaginálního ultrazvuku). Odstraňte Kyleenu, pokud není umístěna zcela v děloze. Nepřejděte si odstraněnou Kyleenu.
- Pokud existuje klinický problém výjimečná bolest nebo krvácení během nebo po inzerci, provede vhodné kroky (jako je fyzické vyšetření a ultrazvuk) okamžitě k vyloučení perforace.
Sledování pacienta
- Reexaminujte a vyhodnoťte pacienty 4 až 6 týdnů po inzerci a jednou ročně poté nebo častěji, pokud jsou klinicky uvedeny.
Odstranění Kyleeny
Načasování odstranění
- Kyleena should not remain in the uterus after 5 years.
- Pokud není těhotenství požadováno, odstraňte Kyleenu během prvních 7 dnů menstruačního cyklu za předpokladu, že žena stále zažívá pravidelné menstruace. Pokud během cyklu dojde k odstranění jindy, nebo žena nezažije pravidelné menstruace, je ohrožena těhotenstvím; Spusťte novou antikoncepční metodu týden před odstraněním těchto žen. [Vidět Pokračování antikoncepce po odstranění ]
Nástroje pro odstranění
Příprava
- Rukavice
- Spekulum
Postup
- Sterilní kleště
Postup odstranění
Obrázek 9. Odstranění Kyleeny
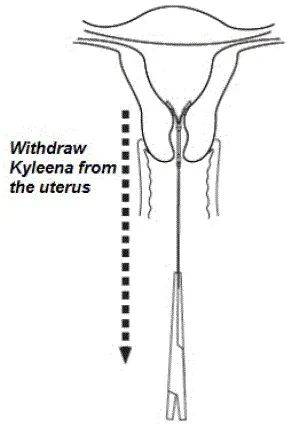
- Odstraňte Kyleenu použitím jemné trakce na vlákny pomocí kleští (obrázek 9).
- Pokud vlákna nejsou viditelná, určete umístění Kyleeny ultrazvukem [viz viz Varování a preventivní opatření ].
- Pokud je zjištěno, že Kyleena je v děložní dutině na ultrazvukové zkoušce, může být odstraněna pomocí úzkých kleští, jako jsou aligátorové kleště. To může vyžadovat dilataci cervikálního kanálu. Po odstranění Kyleeny prozkoumejte systém, aby se zajistilo, že je neporušený.
- Pokud není schopen odstranit jemnou trakci, určete umístění Kyleeny a vyloučte perforaci ultrazvukem nebo jiným zobrazením [viz Varování a preventivní opatření ].
- Odstranění může být spojeno s některými:
- bolest a/nebo krvácení nebo vazovagální reakce (například synkopa bradykardie) nebo záchvaty, zejména u pacientů s predispozicí k těmto podmínkám.
- rozbití nebo vložení Kyleeny v myometriu, které může ztěžovat odstranění [Viz Varování a preventivní opatření ]. Analgesia paracervical anesthesia cervical dilation alligator forceps or other grasping instrument or hysteroscopy may be used to assist in removal.
Pokračování antikoncepce po odstranění
- Pokud není těhotenství žádoucí a pokud si žena přeje pokračovat v používání Kyleeny, může být nový systém vložen okamžitě po odstranění kdykoli během cyklu.
- Pokud chce pacient s pravidelnými cykly zahájit odstranění času antikoncepční metody a zahájení nové metody k zajištění kontinuální antikoncepce. Buď odstraňte Kyleenu během prvních 7 dnů menstruačního cyklu a okamžitě spusťte novou metodu, nebo spusťte novou metodu nejméně 7 dní před odstraněním Kyleeny, pokud má k odstranění během cyklu dojít jindy.
- Pokud chce pacient s nepravidelnými cykly nebo amenoreou zahájit jinou antikoncepční metodu, spusťte novou metodu nejméně 7 dní před odstraněním.
Jak dodáno
Formy a silné stránky dávkování
Kyleena je IUS uvolňující LNG (typ intrauterinního zařízení nebo IUD) sestávajícího z polyethylenového rámu ve tvaru T s steroidní nádrží obsahující celkem 19,5 mg LNG.
Skladování a manipulace
Kyleena (Intrauterinní systém uvolňující levonorgestrel) obsahující celkem 19,5 mg LNG je k dispozici v kartonu jedné sterilní jednotky - NDC
Kyleena is supplied sterile. Kyleena is sterilized with ethylene oxide. Do not resterilize. For single use only. Do not use if the inner package is damaged or open. Insert before the end of the month shown on the label.
Skladovat při 25 ° C (77 ° F); s výlety povoleny mezi 15–30 ° C (59–86 ° F) [viz teplota místnosti s kontrolovanou USP].
Vyrobeno pro: Bayer Healthcare Pharmaceuticals Inc. Whippany NJ 07981. Revidováno: březen 2023
Vedlejší účinky pro Kyleenu
Následující vážné nebo jinak důležité nežádoucí účinky jsou diskutovány jinde při označování:
- Ektopické těhotenství [viz Varování a preventivní opatření ]
- Intrauterinní těhotenství [viz Varování a preventivní opatření ]
- Skupina A Streptococcal Sepsis (GAS) [Viz Varování a preventivní opatření ]
- Zánětlivé onemocnění pánve [viz Varování a preventivní opatření ]
- Perforace [viz Varování a preventivní opatření ]
- Vyhoštění [viz Varování a preventivní opatření ]
- Ovariální cysty [viz Varování a preventivní opatření ]
- Změny vzorů krvácení [viz Varování a preventivní opatření ]
Zkušenosti z klinických studií
Protože klinické studie se provádějí za široce proměnlivých podmínek, nežádoucí rychlosti nežádoucí reakce pozorované v klinických studiích léčiva nelze přímo porovnat s mírami v klinických studiích s jiným léčivem a nemusí odrážet míru pozorované v klinické praxi.
Níže popsané údaje odrážejí expozici 1697 zdravých 18 až 41letých žen (průměrný věk 27,8 ± 5,2 let) Kyleeně. Tato data pocházejí ze dvou multicentrových antikoncepčních studií: v Evropě byla provedena studie fáze 2 s tříletým dobou trváním, která se zapisovala obecně zdravé 21 až 41leté ženy; 217 subjektů bylo vystaveno Kyleeně po dobu jednoho roku a 174 dokončeno tři roky. Údaje v tomto pokusu pokrývají přibližně 8000 cyklů expozice. Ve Spojených státech (USA) Kanadě a Latinské Americe byla provedena studie fáze 3 s tříletým dobou trvání a volitelné prodloužení využití Kyleeny až 5 let. Populace byla obecně zdravá 18 až 35leté ženy. Kyleena bylo vystaveno celkem 1208 subjektů po dobu nejméně jednoho roku; 707 žen vstoupilo do volitelné fáze prodloužení po 3 letech a 550 dokončených pěti let. Data v tomto pokusu pokrývají přibližně 60000 cyklů.
Celkem pro obou studií bylo vystaveno 1425 subjektů po dobu nejméně 1 roku a 550 subjektů bylo dokončeno 5 let používání. Z celkového počtu 1697 subjektů vystavených Kyleeně 563 pocházelo z USA a 1134 pocházelo z Evropy Kanady a Latinské Ameriky; 623 (37%) bylo nulliparous (průměrný věk 24,6 ± 4,5 let) a 1074 (63%) bylo parous (průměrný věk 29,7 ± 4,7 let). Většina žen, které obdržely Kyleenu, byly kavkazské (83%) nebo černý/africký Američan (NULL,4%); 9,4% žen bylo hispánské etnicity. Klinické studie neměly žádný limit horní nebo nižší hmotnosti nebo indexu tělesné hmotnosti (BMI). Průměrná BMI předmětu Kyleena byla 25,2 kg/m 2 (Rozsah 15.2 - 57,6 kg/m 2 ); 16% mělo BMI ≥ 30 kg/m 2 a 2.0% had a BMI ≥ 40 kg/m 2 . Frekvence hlášených nepříznivých reakcí léčiva představují surový výskyt.
Nejběžnějšími nežádoucími účinky (vyskytující se u ≥ 5%uživatelů) byla vulvovaginitida (24%) ovariální cysta (22%) bolest břicha/bolest pánve (21%) bolest hlavy/migréna (15%) a zvýšená Bleea (10%) a zvýšená bledorhea (8%) (8%) a zvýšená Bleea (8%) (8%) (8%) a zvýšená Bleea (8%).
V kombinovaných studiích 22% předčasně přerušilo v důsledku nežádoucí reakce. Nejběžnější nežádoucí účinky (> 1%) vedoucí k přerušení byly zvýšené krvácení (NULL,5%) bolest břicha/bolest pánevní (NULL,2%) vypuštění zařízení (NULL,1%) akné/seboroje (NULL,3%) a spasm dysmenorrhea/dělohy (NULL,3%).
Běžné nežádoucí účinky (vyskytující se u ≥1% uživatelů) jsou shrnuty v tabulce 4 (prezentované jako surové incidence).
Tabulka 4: Nežádoucí účinky, ke kterým došlo u nejméně 1% uživatelů Kyleeny v klinických studiích podle třídy orgánů System (SOC)
| Systémová třída orgánů | Nežádoucí reakce | Incidence (%) (N = 1697) |
| Reprodukční systém a poruchy prsu | Vulvovaginitida | 24.3 |
| Ovariální cysta a | 22.2 | |
| Dysmenorrhea/děložní křeč | 8.0/2.4 | |
| Zvýšené krvácení b | 7.9 | |
| Bolest prsu/nepohodlí | 7.1/3.5 | |
| Vypouštění genitálií | 4.5 | |
| Vyhoštění zařízení (úplné a částečné) | 3.5 | |
| Infekce horního genitálního traktu | 1.5 | |
| Gastrointestinální poruchy | Bolest břicha/pánevní bolest | 13.3/8.2 |
| Nevolnost | 4.7 | |
| Poruchy kůže a podkožní tkáně | Akné/Seborrorea | 14.1/1.8 |
| Alopecie | 1.0 | |
| Poruchy nervového systému | Bolest hlavy/migréna | 12.9/3.3 |
| Psychiatrické poruchy | Deprese/depresivní nálada | 4,4/0,2 |
| a Ovariální cysty byly hlášeny jako nežádoucí účinky, pokud se jednalo o abnormální nefunkční cysty a/nebo měly průměr> 3 cm při ultrazvukovém vyšetření b Ne všechny změny krvácení byly zachyceny jako nežádoucí účinky [viz Varování a preventivní opatření ]. |
V klinických studiích vážné nežádoucí účinky, které se vyskytují u více než jediného subjektu, zahrnovaly: ektopické těhotenství/ruptované mimoděložní těhotenství (10 subjektů); zánětlivé onemocnění pánevní (6 subjektů); zmeškané potraty/neúplné spontánní potraty/spontánní potrat (4 subjekty); ovariální cysta (3 subjekty); Bolest břicha (4 subjekty); deprese/afektivní porucha (4 subjekty); a děložní perforace/zabudované zařízení (perforace myometria) (3 subjekty).
Zážitek z postmarketingu/
Nežádoucí reakces From Postmarketing Spontaneous Reports
Během po schválení používání Iuss uvolňující LNG byly identifikovány následující nežádoucí účinky. Protože tyto reakce jsou hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo vytvořit kauzální vztah k expozici léčiva.
- Arteriální trombotické a žilní tromboembolické události včetně případů plicní embolie hluboké žilní trombózy a mrtvice
- Zlomení zařízení
- Hypersenzitivita (včetně vyrážky a angioedému)
- Zvýšený krevní tlak
Hlášeny nežádoucí účinky z postmarketingových studií
Posouzení perforace a vyhoštění studie intrauterinního zařízení (Apex IUD)
Apex IUD byla velká americká retrospektivní kohortová studie k posouzení dopadu kojení a načasování poporodního vložení IUD na perforaci dělohy a vyhoštění IUD. Analýzy zahrnovaly celkem 326658 inzerce 30% (97824 inzerce), z nichž byly provedeny u žen s dodáním v předchozích 12 měsících. Pro inzerce prováděná u žen, které dodali ≤ 52 týdnů před vložením IUD, došlo k většině poporodní inzerce 57,3% (56047 inzercí) mezi 6 a 14 týdny po porodu. Údaje o kojení byly k dispozici v 94817 inzerci prováděných u žen 52 týdnů nebo méně po dodání.
Výsledky studie ukázaly, že riziko perforace dělohy bylo nejvyšší u žen s inzercí IUD ≤ 6 týdnů po porodu. Okamžité poporodní inzerce (0–3 dny) jsou nálezy omezeny kvůli relativně malému počtu inzercí, ke kterým dochází v tomto časovém intervalu. Ženy, které kojily v době inzerce, byly 33% vyšší riziko perforace (upravený poměr rizika [HR] = 1,33 95% interval spolehlivosti [CI]: 1,07–1,64) ve srovnání s ženami, které v době vložení nebyly kojení. Progresivně nižší riziko perforace dělohy bylo pozorováno v poporodních časových oknech po 6 týdnech u kojení i ne kojení. Tabulka 5 uvádí míru perforace dělohy pro LNG IUS stratifikovanou stavem kojení a poporodním intervalem.
Tabulka 5: Perforace dělohy 1 Sazby pro LNG IUS podle stavu kojení a poporodní interval
| Kojení v době zavedení | Ne kojení v době zavedení | |||
| Poporodní interval v době vložení | Počet událostí/ inzerce | Míra perforace dělohy na 1000 inzerce | Počet událostí/ inzerce | Míra perforace dělohy na 1000 inzerce |
| 0 až 3 dny | 8/1896 | 4.22 | 0/277 | 0.00 |
| 4 dny až ≤ 6 týdnů | 120/10735 | 11.18 | 28/2377 | 11.78 |
| > 6 až ≤ 14 týdnů | 268/29677 | 9.03 | 30/32011 | 6.66 |
| > 14 až ≤ 52 týdnů | 43/6139 | 7.00 | 22/9089 | 2.42 |
| > 52 týdnů nebo žádné doručení | K dispozici nejsou žádná data | 243/184733 | 1.32 | |
| 1 Perforace dělohy zahrnuje úplnou i částečnou perforaci |
Riziko vyloučení bylo variabilní během poporodních intervalů po 52 týdnech. Ženy, které kojily, měly na 28% nižší riziko vyhoštění IUD (upravené HR = 0,72 95% CI: 0,64-0,80) ve srovnání se ženami, které nebyly kojeno v době inzerce. Tabulka 6 uvádí míru vyhoštění IUD pro LNG IUS stratifikované stavem kojení a poporodním intervalem.
Tabulka 6: Vyhoštění 1 Sazby pro LNG IUS podle stavu kojení a poporodní interval
| Kojení v době zavedení | Ne kojení v době zavedení | |||
| Poporodní interval v době vložení | Počet událostí/ inzerce | Míra vyhoštění na 1000 inzerce | Počet událostí/ inzerce | Míra vyhoštění na 1000 inzerce |
| 0 až 3 dny | 187/1896 | 98.63 | 12/277 | 43.32 |
| 4 dny až ≤ 6 týdnů | 185/10735 | 17.23 | 52/2377 | 21.88 |
| > 6 až ≤ 14 týdnů | 421/29677 | 14.19 | 306/2011 | 25.48 |
| > 14 až ≤ 52 týdnů | 120/6139 | 19.55 | 273/9089 | 30.04 |
| > 52 týdnů nebo žádné doručení | K dispozici nejsou žádná data | 5481/184733 | 29.67 | |
| 1 Vyhoštění zahrnuje úplné i částečné vyhoštění |
Interakce drog pro Kyleenu
S Kyleenou nebyly provedeny žádné studie interakce léčiva léčiva.
Léky nebo bylinné produkty, které indukují nebo inhibují enzymy metabolizující LNG, včetně CYP3A4, se mohou během použití Kyleeny snížit nebo zvýšit sérové koncentrace LNG. Antikoncepční účinek Kyleeny je však zprostředkován přímým uvolňováním LNG do děložní dutiny a je nepravděpodobné, že by byl ovlivněn interakcemi léčiva indukcí nebo inhibicí enzymu.
Varování pro Kyleenu
Zahrnuto jako součást 'OPATŘENÍ' Sekce
Opatření pro Kyleenu
Riziko mimoděložního těhotenství
Vyhodnoťte ženy na ektopické těhotenství, pokud otěhotní s Kyleenou na místě, protože s Kyleenou se zvyšuje pravděpodobnost, že těhotenství bude ektopic. Přibližně polovina těhotenství, která se vyskytují u Kyleeny na místě, bude pravděpodobně ektopická. Zvažte také možnost mimoděložního těhotenství v případě nižší bolesti břicha, zejména ve spojení se zmeškanými menstruací, nebo pokud amenoreická žena začne krvácet.
Výskyt mimoděložního těhotenství v klinických studiích s Kyleenou, která vylučovala ženy s anamnézou mimoděložního těhotenství přibližně 0,2% ročně. Riziko mimoděložního těhotenství u žen, které mají v anamnéze mimoděložní těhotenství a používají Kyleenu, není známo. Ženy s předchozí anamnézou ektopické těhotenské tubální chirurgie nebo pánevní infekce mají vyšší riziko mimoděložního těhotenství. Ektopické těhotenství může vést ke ztrátě plodnosti.
Rizika s těhotenstvím intrauterinního
Pokud k těhotenství dojde při používání Kyleeny, odstraní Kyleenu, protože jeho ponechání na místě může zvýšit riziko spontánního potratů a předčasného porodu. Odstranění Kyleeny nebo sondování dělohy může také vést k spontánnímu potratům. V případě intrauterinního těhotenství s Kyleenou zvažte následující:
Septický potrat
U pacientů otěhotních s IUS na místě může dojít k septickému potratům - se septikémií septickým šokem a smrtí -.
Pokračování těhotenství
Pokud žena otěhotní s Kyleenou na místě a pokud Kyleena nelze odstranit nebo žena se rozhodne, že ji nebude odstranit, varuje ji, že neschopnost odstranit Kyleenu zvyšuje riziko předčasné porodu a předčasné porodu sepse. Poraďte jí o izolovaných zprávách o virilizaci ženského plodu po místní expozici LNG během těhotenství s LNG IUS na místě [viz Použití v konkrétních populacích ]. Follow her pregnancy closely a advise her to report immediately any symptom that suggests complications of the pregnancy.
Sepse
Po zavedení IUS uvolňující LNG byla hlášena závažná infekce nebo sepse včetně streptokokové sepse skupiny A (plyn). V některých případech došlo k závažné bolesti během několika hodin po zavedení následované sepsou během několika dnů. Protože smrt na plyn je pravděpodobnější, pokud je léčba zpožděna, je důležité si uvědomit tyto vzácné, ale závažné infekce. Aseptická technika během vložení Kyleeny je nezbytná pro minimalizaci závažných infekcí, jako je plyn.
Pánevní infekce
Okamžitě prozkoumejte uživatele se stížnostmi na dolní břišní nebo pánevnou bolest, která je nehořená vypouštění nevysvětlitelných krvácejících horečky pohlavní léze nebo vředy. Odstraňte Kyleenu v případech opakující se endometritidy nebo pánevního zánětlivého onemocnění nebo pokud je akutní pánevní infekce závažná nebo nereaguje na léčbu.
Zánětlivé onemocnění pánve (PID)
Kyleena is contraindicated in the presence of known or suspected PID or in women with a history of PID unless there has been a subsequent intrauterine pregnancy [see Kontraindikace ]. IUDs have been associated with an increased risk of PID most likely due to organisms being introduced into the uterus during insertion. In clinical trials PID was observed in 0.5% of women overall a occurred more frequently within the first year a most often within the first month after insertion of Kyleena.
Ženy se zvýšeným rizikem PID
PID je často spojena se sexuálně přenosnou infekcí (STI) a Kyleena chrání před STI. Riziko PID je větší u žen, které mají více sexuálních partnerů a také pro ženy, jejichž sexuální partnery mají více sexuálních partnerů. Ženy, které měly PID, jsou vystaveny zvýšenému riziku recidivy nebo opětovné infekce. Zejména zjistěte, zda je žena vystavena zvýšenému riziku infekce (například leukémie získala syndrom imunitního nedostatku [AIDS] intravenózní zneužívání drog).
Subklinický PID
PID může být asymptomatický, ale stále má za následek poškození tubálního a jeho následky.
Léčba PID
Po diagnóze PID nebo podezření na bakteriologické vzorky PID by měly být získány a by měla být okamžitě zahájena antibiotická terapie. Obvykle je vhodné odstranit Kyleenu po zahájení antibiotické terapie.1
Aktinomykóza
Aktinomykóza has been associated with IUDs. Remove Kyleena from symptomatic women a treat with antibiotics. The significance of actinomyces-like organisms on Pap smear in an asymptomatic IUD user is unknown a so this finding alone does not always require Kyleena removal a treatment. When possible confirm a Pap smear diagnosis with cultures.
Perforace
Perforace (total or partial including penetration/embedment of Kyleena in the uterine wall or cervix) may occur most often during insertion although the perforation may not be detected until sometime later. The incidence of perforation during clinical trials was <0.1%.
Riziko perforace dělohy se zvyšuje u žen, které nedávno porodily a u žen, které kojí v době inzerce. Ve velké studii bezpečnosti v postmarketingu provedené v USA bylo riziko perforace dělohy nejvyšší, když došlo k vložení během ≤ 6 týdnů po porodu a také vyšší s kojením v době vložení [viz viz Nežádoucí účinky ].
Riziko perforace může být zvýšeno, pokud je Kyleena vložena, když je děloha pevná retrovertovaná nebo zcela ne zcela zapsána.
Pokud dojde k perforaci, najděte a odstraňte Kyleenu. Může být vyžadována chirurgie. Zpožděná detekce nebo odstranění Kyleeny v případě perforace může vést k migraci mimo adhezí děložní dutiny peritonitida střevní perforace střevní obstrukce abscesů a erozi sousedního vnitřnosti. Kromě toho může perforace snížit antikoncepční účinnost a vést k těhotenství.
Vyhoštění
Částečné nebo úplné vyhoštění Kyleeny může dojít ke ztrátě účinnosti. Vyhoštění může být spojeno s příznaky krvácení nebo bolesti, nebo může být asymptomatické a bez povšimnutí. Kyleena obvykle snižuje menstruační krvácení v průběhu času; Zvýšení menstruačního krvácení proto může svědčit o vyhoštění. Zvažte další diagnostické zobrazování, jako je rentgen, pokud je vyloučení podezřelé na základě ultrazvuku [viz Klinické úvahy pro použití a odstranění ]. In clinical trials a 5-year expulsion rate of 3.5% (59 out of 1690 subjects) was reported.
Riziko vyhoštění se zvyšuje s inzercemi bezprostředně po porodu a zdá se, že se zvyšuje s inzercí po potratu druhého trimestru na základě omezených údajů. Ve velké studii bezpečnosti v postmarketingu provedené v USA bylo riziko vyhoštění nižší se stavem kojení [viz viz Nežádoucí účinky ].
Odstraňte částečně vyloučenou Kyleenu. Pokud došlo k vyhoštění, může být vložena nová Kyleena kdykoli, kdy si může poskytovatel přiměřeně jist, že žena není těhotná.
Ovariální cysty
Protože antikoncepční účinek Kyleeny je způsoben hlavně jeho lokálními účinky v ovulačních cyklech dělohy s prasknutím folikulárních ruptury, obvykle se vyskytuje u žen s úrodným věkem pomocí Kyleeny. Ovariální cysty (uváděné jako nežádoucí účinky, pokud se jednalo o abnormální nefunkční cysty a/nebo měly průměr> 3 cm při ultrazvukovém vyšetření) byly hlášeny alespoň jednou v průběhu klinických studií u 22% žen používajících Kyleenu a 0,6% subjektů přerušených kvůli ovární cyst. Většina ovariálních cyst je asymptomatická, i když některé mohou být doprovázeny pánevní bolestí nebo dyspareunií. Ve většině případů cysty vaječníků zmizí spontánně během pozorování dvou až tří měsíců. Vyhodnoťte perzistentní ovariální cysty. Chirurgický zásah není obvykle nutný.
Změny krvácení vzoru
Kyleena can alter the bleeding pattern a result in spotting irregular bleeding heavy bleeding oligomenorrhea a amenorrhea. During the first 3–6 months of Kyleena use the number of bleeding a spotting days may be higher a bleeding patterns may be irregular. Thereafter the number of bleeding a spotting days usually decreases but bleeding may remain irregular.
V klinických studiích Kyleena se amenorea vyvinula do konce prvního roku používání u přibližně 12% uživatelů Kyleeny. Celkem 81 subjektů z 1697 (NULL,8%) bylo přerušeno v důsledku stížností na krvácení dělohy. Tabulka 2 ukazuje vzorce krvácení, jak jsou dokumentovány v klinických studiích Kyleena založené na 90denních referenčních obdobích. Tabulka 3 ukazuje počet dnů krvácení a špinění na základě 28denních ekvivalentů cyklu.
Tabulka 2: Vzory krvácení hlášené s Kyleenou ve studiích antikoncepce (o 90denní referenční období)
| Kyleena | Prvních 90 dní N = 1566 | Druhý 90 dní N = 1511 | Konec roku 1 N = 1371 | Konec roku 3 N = 975 | Konec roku 5 N = 530 |
| Amenorea 1 | <1% | 5% | 12% | 20% | 23% |
| Opačné krvácení 2 | 10% | 20% | 26% | 26% | 26% |
| Časté krvácení 3 | 25% | 10% | 4% | 2% | 2% |
| Prodloužené krvácení 4 | 57% | 14% | 6% | 2% | 1% |
| Nepravidelné krvácení 5 | 43% | 25% | 17% | 10% | 9% |
| 1 Definované jako subjekty bez krvácení/špinění během 90denního referenčního období 2 Definované jako subjekty s 1 nebo 2 epizodami krvácení/špinění v 90denní referenční období 3 Definované jako subjekty s více než 5 epizodami krvácení/špinění v 90denní referenční období 4 Definované jako subjekty s epizodami krvácení/špinění trvající více než 14 dní v 90denní referenční období. Subjekty s prodlouženým krvácením mohou být také zahrnuty do jedné z dalších kategorií (s výjimkou amenorea) 5 Definováno jako subjekty s 3 až 5 epizodami krvácení/špinění a méně než 3 intervaly krvácení/bezpochyby 14 nebo více dní |
Tabulka 3: Průměrný počet dnů krvácení a špinění za 28denní ekvivalent cyklu
| 28denní cyklus Ekvivalent | Cyklus 1 N = 1619 | Cyklus 4 N = 1575 | Cyklus 7 N = 1518 | Cyklus 13 N = 1394 | Cyklus 39 N = 913 | Cyklus 65 N = 322 |
| Dny o léčbě | 1–28 | 85–112 | 169–196 | 337–364 | 1065-1092 | 1793-1820 |
| Střední (SD) | Střední (SD) | Střední (SD) | Střední (SD) | Střední (SD) | Střední (SD) | |
| Počet dnů krvácení | 7.2 (5.9) | 3.2 (3.6) | 2.2 (3.0) | 1.5 (2.4) | 1.0 (2.0) | 0.9 (1.8) |
| Počet dnů špinění | 8.6 (6.0) | 4.6 (4.4) | 3.5 (3.4) | 2.9 (3.0) | 2.2 (2.6) | 2.1 (2.4) |
Pokud se během delšího používání vyvíjí významná změna krvácení, přijme vhodná diagnostická opatření k vyloučení endometriální patologie. Zvažte možnost těhotenství, pokud k menstruaci nedochází do šesti týdnů od počátku předchozí menstruace. Jakmile je těhotenství vyloučeno, opakované těhotenské testy nejsou u amenorrheických žen obecně nezbytné, pokud není uvedeno například jinými známkami těhotenství nebo pánevní bolestí.
Rakovina prsu
Ženy, které v současné době mají nebo mají rakovinu prsu nebo mají podezření na rakovinu prsu Kontraindikace ].
Spontánní zprávy o rakovině prsu byly obdrženy během zážitku z postmarketingu s IU uvolňujícím LNG. Observační studie rizika rakoviny prsu s používáním IU uvolňujícího LNG neposkytují přesvědčivé důkazy o zvýšeném riziku.
Klinické úvahy pro použití a odstranění
Po pečlivém posouzení používejte Kyleenu s opatrností, pokud existuje některá z následujících podmínek, a zvažte odstranění systému, pokud některá z nich vznikne během použití:
- Koagulopatie nebo použití antikoagulantů
- Fokální migréna migrény s asymetrickou ztrátou zraku nebo jinými příznaky naznačujícími přechodnou mozkovou ischemii
- Výjimečně závažná bolest hlavy
- Výrazné zvýšení krevního tlaku
- Závažné arteriální onemocnění, jako je mrtvice nebo infarkt myokardu
Kromě toho zvažte odstranění Kyleeny, pokud během používání dojde k nějaké z následujících podmínek:
- Malignita dělohy nebo děložního čípku
- Žloutenka
Pokud vlákna nejsou viditelná nebo jsou výrazně zkrácena, mohly se rozbité nebo zasunout do cervikálního kanálu nebo dělohy. Zvažte možnost, že systém mohl být přemístěn (například vyloučený nebo perforován dělohou) [Viz Perforace Vyhoštění ]. Exclude pregnancy a verify the location of Kyleena for example by sonography X-ray or by gentle exploration of the cervical canal with a suitable instrument. If Kyleena is displaced remove it. A new Kyleena may be inserted at that time or during the next menses if it is certain that conception has not occurred. If Kyleena is in place with no evidence of perforation no intervention is indicated.
Bezpečnostní informace o magnetické rezonanci (MRI)
 |
Neklinické testování prokázalo, že Kyleena je MR podmínka. Pacient s Kyleenou může být v systému MR bezpečně naskenován v následujících podmínkách:
- Statické magnetické pole 3,0 t nebo méně
- Maximální gradient prostorového pole 36 000 Gauss/cm (360 T/m)
- Maximální MR systém hlásil, že celé tělo bylo průměrováno specifickou míru absorpce (SAR) 4W/kg (řízený provozní režim první úrovně)
Očekává se, že za podmínek skenování definovaných nad Kyleena IUS způsobí maximální nárůst teploty o menší než 2 ° C po 15 minutách nepřetržitého skenování.
Při neklinickém testování obrazového artefaktu způsobeného IUS se rozšířil až 5 mm od IUS, když byl zobrazen pomocí gradientního sekvence pulzní sekvence a 3,0 T MRI systému.
Informace o poradenství pro pacienta
Doporučujte pacientovi, aby si přečetl značení pacienta schváleného FDA ( Informace o pacientu ).
- Sexuálně přenosné infekce: Poraďte pacientovi, že tento produkt nechrání před infekcí HIV (AIDS) a dalšími sexuálně přenosnými infekcemi (STI).
- Riziko mimoděložního těhotenství: Poraďte pacientovi o rizicích mimoděložního těhotenství, včetně ztráty plodnosti. Naučte ji rozpoznat a podávat zprávy svému poskytovateli zdravotní péče okamžitě jakékoli příznaky mimoděložního těhotenství. [Vidět Varování a preventivní opatření ]
- Rizika intrauterinního těhotenství: Doporučte pacientovi, aby kontaktoval svého poskytovatele zdravotní péče, pokud si myslí, že by mohla být těhotná. Informujte pacienta o rizicích intrauterinního těhotenství při používání Kyleeny, včetně rizik ponechání Kyleeny na místě a rizika odstranění Kyleeny nebo sondování dělohy. Pokud Kyleena nelze u těhotné pacienta odstranit, aby jí poradila, aby okamžitě nahlásila jakýkoli příznak, který naznačuje komplikace těhotenství. Poraďte jí o izolovaných zprávách o virilizaci ženského plodu po místní expozici LNG během těhotenství s LNG IUS na místě. [Vidět Varování a preventivní opatření a Použití ve speciálních populacích ]
- Sepse: Doporučujte pacientovi, že během prvních několika dnů po vložení Kyleeny může dojít k závažné infekci nebo sepse, včetně streptokokové sepse skupiny A (plyn). Pokynujte jí, aby okamžitě kontaktovala poskytovatele zdravotní péče, pokud si krátce po vložení Kyleeny vyvine těžkou bolest nebo horečku. [Vidět Varování a preventivní opatření ]
- Pánevní infekce: Poraďte se pacientovi o možnosti pánevních infekcí, včetně PID a že tyto infekce mohou způsobit poškození tubálních látek vedoucí k mimoděložnímu těhotenství nebo neplodnosti nebo zřídka může vyžadovat hysterektomii nebo způsobit smrt. Naučte pacienty, aby rozpoznali a hlásili svému poskytovateli zdravotní péče, okamžitě jakékoli příznaky infekce pánve. Mezi tyto příznaky patří vývoj menstruačních poruch (prodloužené nebo silné krvácení) neobvyklý vaginální výbojový břišní nebo pánevní bolest nebo něha dyspareunia zimnice a horečka. [Vidět Varování a preventivní opatření .]
- Perforace a Vyhoštění: Doporučujte pacientovi, že IUS může být vyloučen z dělohy nebo perforizovat dělohu a poučit ji o tom, jak může zkontrolovat, zda vlákna stále vyčnívají z děložního čípku. Informujte ji, že při kyleeně může dojít k perforaci a vyhoštění Kyleeny nadměrné bolesti nebo vaginální krvácení během umístění Kyleeny zhoršující se bolest nebo krvácení po umístění nebo neschopnost cítit řetězce Kyleeny. Upozorněte ji, aby netahala na vlákna a vytlačila Kyleenu. Informujte ji, že neexistuje žádná antikoncepční ochrana, pokud je Kyleena vysídlena nebo vyloučena. Poskytněte pacientovi, aby kontaktoval svého poskytovatele zdravotní péče, pokud nemůže cítit vlákna a vyhnout se pohlavnímu styku nebo používat nehormonální záložní antikoncepci (jako jsou kondomy nebo spermicid), dokud nebude potvrzeno umístění Kyleeny. Radí jí, že pokud dojde k perforaci, bude muset být Kyleena umístěna a odstraněna; může být vyžadována chirurgie. [Vidět Varování a preventivní opatření ]
- Ovariální cysty: Poraďte pacientovi ohledně rizika ovariálních cyst a že cysty mohou způsobit klinické příznaky včetně bolesti břicha pánevní nebo dyspareunii. Doporučte pacientovi, aby kontaktoval svého poskytovatele zdravotní péče, pokud zažije tyto příznaky. [Vidět Varování a preventivní opatření ]
- Změny krvácení vzoru: Poraďte pacientovi, že během prvních několika týdnů po inzerci může dojít k nepravidelnému nebo prodlouženému krvácení a skvrnitě a/nebo křečkům. Informujte pacienta, že během prvních 6 měsíců Kyleeny používá počet krvácení a dnů špinění může být vyšší a vzorce krvácení může být nepravidelné. Pokud její příznaky pokračují nebo jsou závažné, měla by je nahlásit svému poskytovateli zdravotní péče. [Vidět Varování a preventivní opatření ]
- Klinické úvahy pro použití a odstranění: Doporučte pacientovi, aby kontaktoval svého poskytovatele zdravotní péče, pokud zažije některé z následujících:
- Mrtvice nebo infarkt
- Velmi závažné nebo migrénové bolesti hlavy
- Nevysvětlitelná horečka
- Žloutnutí kůže nebo bílých očí, protože to mohou být známky vážných problémů s jatery
- Těhotenství nebo podezření na těhotenství
- Během sexu bolest břišní bolesti pánevní břicha nebo bolest břicha
- HIV pozitivní sérokonverze v sobě nebo jejím partnerovi
- Možné vystavení STIS
- Neobvyklý vaginální výtok nebo vředy
- Těžké vaginální krvácení nebo krvácení, které trvá dlouho nebo pokud jí chybí menstruační období
- Neschopnost cítit Kyleenina vlákna
- Bezpečnostní informace o magnetické rezonanci (MRI): Informujte pacienta, že Kyleena může být bezpečně naskenována s MRI pouze za konkrétních podmínek [viz Varování a preventivní opatření ]. Instruct patients who will have an MRI to tell their doctor that they have Kyleena.
Neklinická toxikologie
Zhodnocení mutageneze karcinogeneze plodnosti
[Vidět Varování a preventivní opatření ]
Použití v konkrétních populacích
Těhotenství
Shrnutí rizika
Použití Kyleeny je kontraindikováno v těhotenství nebo s podezřením na těhotenství a Kyleena může způsobit nepříznivé výsledky těhotenství [viz Kontraindikace Varování a preventivní opatření ]. If a woman becomes pregnant with Kyleena in place the likelihood of ectopic pregnancy is increased a there is an increased risk of miscarriage sepsis premature labor a premature delivery. Remove Kyleena if possible if pregnancy occurs in a woman using Kyleena. If Kyleena cannot be removed follow the pregnancy closely [see Varování a preventivní opatření ].
Byly izolované případy virilizace vnějších genitálií ženského plodu po místní expozici LNG během těhotenství s LNG IU na místě. S Kyleenou nebyly provedeny studie reprodukce zvířat.
Laktace
Shrnutí rizika
Publikované studie uvádějí přítomnost LNG v lidském mléce. Malé množství progestinů (přibližně 0,1% z celkových dávek matek) byla detekována v mateřském mléce kojících matek, které používaly jiné Iuss uvolňující LNG, což vedlo k vystavení LNG kojeným kojencem. U kojených kojenců neexistují žádné zprávy o nepříznivých účincích s užíváním antikoncepcí pouze progestinu. Izolované případy snížené produkce mléka byly hlášeny u IU uvolňujícího LNG. Vývojové a zdravotní přínosy kojení by měly být zváženy spolu s klinickou potřebou matky k Kyleeně a jakýmikoli potenciálními nepříznivými účinky na kojené dítě z Kyleeny nebo ze základního stavu matek.
Ženy a muži reprodukčního potenciálu
Vraťte se k plodnosti po přerušení Kyleeny
Asi 71% ze 163 žen, které si přály těhotenství po přerušení studie a poskytly následné informace koncipované do 12 měsíců po odstranění Kyleeny.
Dětské použití
Bezpečnost a účinnost Kyleeny byla stanovena u žen v reprodukčním věku. Očekává se, že účinnost bude stejná u žen do postpubertálních žen mladších 18 let jako u uživatelů 18 let a starší. Použití tohoto produktu před menarche není indikováno.
Geriatrické použití
Kyleena has not been studied in women over age 65 a is not approved for use in this population.
Informace o předávkování Kyleeně
Žádné informace
Kontraindikace pro Kyleenu
Použití Kyleeny je kontraindikováno, když existuje jedna nebo více z následujících podmínek:
- Těhotenství or suspicion of pregnancy [see Varování a preventivní opatření Použití v konkrétních populacích ]
- Pro použití jako postkoitální antikoncepce (nouzová antikoncepce)
- Vrozená nebo získaná anomálie dělohy včetně fibroidů, které zkreslují děložní dutinu
- Akutní zánětlivé onemocnění pánevních pánev (PID) nebo anamnéza PID, pokud nedošlo k následnému intrauterinnímu těhotenství [viz Varování a preventivní opatření ]
- Poporodní endometritida nebo infikovaný potrat za poslední 3 měsíce
- Známá nebo podezřelá z dělohy nebo děložní malignity
- Známý nebo podezřelý rakovina prsu nebo jiná rakovina citlivá na progestin nyní nebo v minulosti
- Krvácení dělohy neznámé etiologie
- Neléčená akutní cervicitida nebo vaginitida včetně bakteriální vaginózy nebo jiných infekcí dolních genitálních traktů, dokud není infekce kontrolována
- Akutní onemocnění jater nebo nádor jater (benigní nebo maligní)
- Podmínky spojené se zvýšenou náchylností k infekcím pánve [viz Varování a preventivní opatření ]
- Dříve vložené intrauterinní zařízení (IUD), které nebylo odstraněno
- Přecitlivělost na jakoukoli součást tohoto produktu [viz Nežádoucí účinky a POPIS ]
Klinická farmakologie for Kyleena
Mechanismus působení
Místní mechanismus, kterým nepřetržitě uvolňovaný LNG přispívá k antikoncepční účinnosti Kyleeny, nebyl přesvědčivě prokázán. Studie Kyleeny a podobných prototypů LNG IUS navrhly několik mechanismů, které zabraňují těhotenství: zesílení cervikálního hlenu zabraňující průchodu spermií do inhibice spermatu nebo přežití spermií a změnou endometria.
Farmakodynamika
Kyleena has mainly local progestogenic effects in the uterine cavity. The local concentrations of LNG lead to morphological changes including stromal pseudodecidualization glaular atrophy a leukocytic infiltration a a decrease in glaular a stromal mitoses.
V klinických studiích s ovulací Kyleeny byly hodnoceny na základě hodnot progesteronu v séru> 2,5 ng/ml v jedné studii a hodnotách progesteronu v séru> 2,5 ng/ml spolu s hladinami estradiolu v séru spolu s hladinami estradiolu v séru <27.24 pg/mL in another study. Evidence of ovulation by these criteria was seen in 23 out of 26 women in the first year in 19 out of 20 women in the second year a in all 16 women in the third year. In the fourth year evidence of ovulation was observed in the one woman remaining in the subset a in the fifth year no women remained in this subset.
Farmakokinetika
Vstřebávání
Nízké dávky LNG se podávají do děložní dutiny pomocí intrauterinního systému Kyleena. The nadarmo Míra uvolňování je přibližně 17,5 mcg/den po 24 dnech a sníží se na přibližně 15,3 mcg/den po 60 dnech a na 9,8 mcg/den po 1 roce. Poté postupně klesá na přibližně 7,9 mcg/den po 3 letech a 7,4 mcg/den po 5 letech. Průměrný LNG nadarmo Míra uvolnění je přibližně 12,6 mcg/den během prvního roku a 9,0 mcg/den po dobu 5 let.
V podskupině 6 subjektů byla maximální pozorovaná koncentrace LNG v séru (průměr ± SD) 302 ± 170 pg/ml dosažena po 7,5 dnech (mediánu) inzerce Kyleeny. Poté koncentrace séra LNG (průměr ± SD) v roce 1 2 3 4 a 5 byly 199 ± 171 pg/ml (n = 6) 120 ± 57 pg/ml (n = 6) 122 ± 65 pg/ml (n = 6) 79 ± 12 pg/ml (n = 3) a 65 ± 15 pg/Ml (n = 3). Populační farmakokinetické hodnocení založené na širší databázi (> 1 000 pacientů) vykazovalo podobný klesající koncentrační profil s 175 ± 74 pg/ml 7 dní po umístění 125 ± 50 pg/ml při 1 roce 99 ± 41 pg/ml po 3 letech a 90 ± 35 pg/ml po 5 letech.
Symbicort 80-4,5 mcg inhalátor
Rozdělení
Zjevný objem distribuce LNG je uváděn jako přibližně 1,8 l/kg. LNG je nespecificky vázána na sérový albumin a konkrétně na globulin vázající pohlavní hormony (SHBG). V souladu s tím změny v koncentraci SHBG v séru vedou ke zvýšení (při vyšší koncentraci SHBG) nebo ke snížení (při nižší koncentraci SHBG) celkové koncentrace LNG v séru. U podskupiny 6 subjektů se koncentrace SHBG během prvních 3 měsíců po zavedení Kyleeny v průměru poklesla o asi 30% a zůstala relativně stabilní během 5 let používání. Méně než 2% cirkulujícího LNG je přítomno jako volný steroid.
Odstranění
Po intravenózním podání 0,09 mg LNG pro zdravé dobrovolníky je celková clearance LNG přibližně 1 ml/min/kg a poločas eliminace je přibližně 20 hodin. Míra metabolické clearance se může mezi jednotlivci několiknásobně lišit a to může částečně odpovídat za široké individuální změny koncentrací LNG pozorovaných u jedinců pomocí antikoncepčních produktů obsahujících LNG.
Metabolismus
Po absorpci je LNG rozsáhle metabolizována. Nejdůležitějšími metabolickými cestami jsou redukce skupiny A4-3-oxo a hydroxylace v polohách 2a 1p a 16p následované konjugací. Významná množství konjugovaného a nekonjugovaného 3α 5p- je také přítomna v séru spolu s mnohem menším množstvím 3a 5a-tetrahydrolevonorgestrelu a 16p-hydroxylevorgestrelu. CYP3A4 je hlavní enzym zapojený do oxidačního metabolismu LNG.
Vylučování
LNG a jeho metabolity fáze I jsou vylučovány především jako glukuronidové konjugáty. Asi 45% LNG a jeho metabolitů je vylučováno v moči a asi 32% je vylučováno ve stolicích většinou jako glukuronidové konjugáty.
Konkrétní populace
Dětský
Bezpečnost a účinnost Kyleeny byla stanovena u žen v reprodukčním věku. Použití tohoto produktu před menarche není indikováno.
Geriatric
Kyleena has not been studied in women over age 65 a is not approved for use in this population.
Rasa
Žádné studie nevyhodnotily účinek rasy na farmakokinetiku Kyleeny.
Poškození jater
Nebyly provedeny žádné studie za účelem vyhodnocení účinku jaterního onemocnění na dispozice Kyleeny.
Poškození ledvin
Nebyly provedeny žádné formální studie za účelem vyhodnocení účinku onemocnění ledvin na dispozice Kyleeny.
Interakce léčiva
S Kyleenou nebyly provedeny žádné studie interakce léčiva léčiva [viz Lékové interakce ].
Klinické studie
Antikoncepční účinnost Kyleeny byla hodnocena v klinické studii, která zapsala obecně zdravé ženy ve věku 18–35 let, z nichž 1452 obdrželo Kyleenu. Z těchto 40%(574) byly nulliparous ženy 870 (60%) žen dokončené 3 roky studie 707 (49%) zvolených do prodloužení fáze až do celkem 5 let a 550 (38%) dokončených 5 let používání. Soud byl multicentrickou více národní randomizovanou studií s otevřeným označením provedenou v 11 zemích v Evropě Latinské Americe v USA a Kanadě. Byly vyloučeny ženy méně než šest týdnů po porodu s anamnézou mimoděložního těhotenství s klinicky významnými cysty vaječníků nebo s HIV nebo jinak s vysokým rizikem sexuálně přenosných infekcí. Na amerických místech bylo léčeno celkem 563 (39%) a 889 (61%) bylo v místech mimo USA. Rasová demografie zapsaných žen, které obdržely Kyleenu, byla: Kavkazská (80%) černá/africký Američan (NULL,1%) ostatní (NULL,6%) a asijské (NULL,2%); 11% naznačilo hispánskou etnicitu. Klinická studie neměla horní nebo nižší hmotnost ani limit BMI. Rozsah hmotnosti byl 38 až 173 kg (průměrná hmotnost: 68,7 kg) a průměrná BMI byla 25,3 kg/m 2 (Rozsah 15.2–57,6 kg/m 2 ). Of Kyleena-treated women 22% discontinued the study treatment due to an adverse reaction 5.0% were lost to follow-up 2.3% withdrew for unspecified reasons 1.2% discontinued due to a protocol deviation 0.9% discontinued due to pregnancy a 20% discontinued due to other reasons.
Míra těhotenství vypočtená jako index Pearl (PI) u žen ve věku 18–35 let byl primárním koncovým bodem účinnosti používaný k posouzení antikoncepční spolehlivosti. PI byl vypočítán na základě 28denních ekvivalentních expozičních cyklů; Vyhodnocovatelné cykly vyloučily ty, ve kterých byla použita záložní antikoncepce, pokud v tomto cyklu nedošlo k těhotenství. Rok 1 PI byl založen na 2 těhotenstvích a kumulativní 5leté těhotenství bylo založeno na 13 těhotenstvích, ke které došlo po nástupu léčby a do 7 dnů po odstranění nebo vyhoštění Kyleeny. Tabulka 5 ukazuje vypočítanou roční a kumulativní míru těhotenství.
Tabulka 7: Indexy Pearl podle roku a 5letá kumulativní míra těhotenství
| Kyleena Clinical Trial | Index Pearl | Kumulativní 5letá sazba Kaplan Meier | ||||
| Rok 1 | 2 rok | 3. rok | 4 rok | Rok 5 | ||
| Počet hodnotících 28denních cyklů expozice16207 | 16207 | 13853 | 11610 | 8556 | 7087 | 57313 |
| Těhotenství Rate (95% Confidence Interval) | 0.16 (NULL,02 0,58) | 0.38 (NULL,10 0,96) | 0.45 (NULL,12 1,15) | 0.15 (NULL,00 0,85) | 0.37 (NULL,04 1,33) | 1.45 (NULL,82 2,53) |
Informace o pacientech pro Kyleenu
Kyleena
(Ki-Lee-nah)
(Intrauterinní systém uvolňující Levonorgestrel)
Než se rozhodnete, zda je pro vás Kyleena pravá, přečtěte si tyto informace o pacientech pečlivě. Tyto informace nezavazují místo rozhovoru s vaším gynekologem nebo jiným poskytovatelem zdravotní péče, který se specializuje na zdraví žen. Máte -li jakékoli dotazy ohledně Kyleeny, zeptejte se svého poskytovatele zdravotní péče. Měli byste se také dozvědět o dalších metodách kontroly antikoncepce, abyste si vybrali ten, který je pro vás nejlepší.
Kyleena does not protect against HIV infection (AIDS) a other sexually transmitted infections (STIs).
Co je Kyleena?
- Kyleena is a hormone-releasing system placed in your uterus by your healthcare provider to prevent pregnancy for up to 5 years.
- Kyleena can be removed by your healthcare provider at any time.
- Kyleena can be used whether or not you have given birth to a child.
Kyleena is a small flexible plastic T-shaped system that slowly releases a progestin hormone called Levonorgestrel (LNG) that is often used in birth control pills . Because Kyleena releases LNG into your uterus only small amounts of the hormone enter your blood. Kyleena does not contain estrogen .
K stonku (dolní konec) Kyleeny jsou připojena dvě tenká nití. Vlákna jsou jedinou částí Kyleeny, kterou můžete cítit, když je Kyleena ve vaší děloze; Na rozdíl od řetězce tamponu se však vlákna nepřesahují mimo vaše tělo.
 |
Kyleena is small
 |
a Flexible
Kyleena is small a Flexible
Co když potřebuji antikoncepci déle než 5 let?
Kyleena must be removed after 5 years. Your healthcare provider can place a new Kyleena during the same office visit if you choose to continue using Kyleena.
Co když chci přestat používat Kyleenu?
Kyleena is intended for use up to 5 years but you can stop using Kyleena at any time by asking your healthcare provider to remove it. You could become pregnant as soon as Kyleena is removed so you should use another method of birth control if you do not want to become pregnant. Talk to your healthcare provider about the best birth control methods for you because your new method may need to be started 7 days before Kyleena is removed to prevent pregnancy.
Co když změním názor na kontrolu porodnosti a chci otěhotnět za méně než 5 let?
Váš poskytovatel zdravotní péče může Kyleenu kdykoli odstranit. Jakmile je Kyleena odstraněna, můžete otěhotnět. Asi 7 z 10 žen, které chtějí otěhotnět, otěhotní někdy v prvním roce poté, co je Kyleena odstraněna.
Jak Kyleena funguje?
Kyleena may work in several ways including thickening cervical mucus inhibiting sperm movement reducing sperm survival a thinning the lining of your uterus. It is not known exactly how these actions work together to prevent pregnancy.
 |
Jak dobře pracuje Kyleena pro antikoncepci?
Následující graf ukazuje šanci na otěhotnění pro ženy, které používají různé metody kontroly antikoncepce. Každé pole v grafu obsahuje seznam metod kontroly antikoncepce, které mají podobnou účinnost. Nejúčinnější metody jsou na vrcholu grafu. Krabice na dně grafu ukazuje šanci na otěhotnění pro ženy, které nepoužívají antikoncepci a snaží se otěhotnět.
Kyleena an intrauterine device (IUD) also known as an intrauterine system (IUS) is in the box at the top of the chart.
Kdo by mohl použít Kyleenu?
Můžete si vybrat Kyleenu, pokud:
- Chcete dlouhodobou antikoncepci, která poskytuje nízkou šanci na otěhotnění (méně než 1 ze 100)
- Chcete kontrolu antikoncepce, která funguje nepřetržitě až 5 let
- Chcete kontrolu porodnosti, která je reverzibilní
- Chcete metodu kontroly antikoncepce, kterou nemusíte užívat denně
- jsou ochotni použít metodu antikoncepce, která je umístěna do dělohy
- chtějí kontrolu porodnosti, která neobsahuje estrogen
Nepoužívejte Kyleenu, pokud:
- jsou nebo mohou být těhotné; Kyleena nelze použít jako nouzová antikoncepce
- mít vážnou pánevní infekci zvanou zánětlivé onemocnění pánevní (PID) nebo jste v minulosti měli PID, pokud jste neměli normální těhotenství po odchodu
- mít nyní neošetřenou genitální infekci
- měli vážnou pánevní infekci za poslední 3 měsíce po těhotenství
- může snadno získat infekce. Například pokud:
- mít více sexuálních partnerů nebo váš partner má více sexuálních partnerů
- mít problémy s vaším imunitním systémem
- užívat nebo zneužívat intravenózní drogy
- mít nebo mít podezření, že byste mohli mít rakovinu dělohy nebo děložního čípku
- mají krvácení z vagíny, která nebyla vysvětlena
- mít onemocnění jater nebo nádor jater
- mít rakovinu prsu nebo jakoukoli jinou rakovinu, která je nyní nebo v minulosti citlivá na progestin (ženský hormon)
- mít již ve své děloze intrauterinní zařízení
- Mějte stav dělohy, která mění tvar dutiny dělohy, jako jsou velké nádory fibroidy
- jsou alergičtí na levonorgestrel silikonový polyethylenový stříbrný oxid křemičitý polypropylen nebo měď ftalocyanin
Předtím, než Kyleena umístila, řekněte svému poskytovateli zdravotní péče o všech vašich zdravotních stavech, včetně:
- mít výše uvedené podmínky
- měli infarkt
- měli mrtvici
- se narodili se srdečními chorobami nebo měli problémy s vašimi srdečními ventily
- mít problémy s srážením krve nebo užívat léky ke snížení srážení
- mít vysoký krevní tlak
- nedávno měl dítě nebo kojí
- mít vážné bolesti hlavy nebo migrény
- mít AIDS HIV nebo jinou sexuálně přenosnou infekci
Řekněte svému poskytovateli zdravotní péče o všech lécích, které užíváte, včetně vitamínů a bylinných doplňků léčivých přípravků na volně prodejné.
Jak je umístěna Kyleena?
Kyleena is placed by your healthcare provider during an in-office visit or immediately after giving birth.
Nejprve váš poskytovatel zdravotní péče prozkoumá vaši pánev a najde přesnou polohu dělohy. Váš poskytovatel zdravotní péče poté vyčistí vagínu a děložníku s antiseptickým roztokem a posune štíhlou plastovou trubici obsahující Kyleenu skrz děložku do dělohy.
Váš poskytovatel zdravotní péče poté odstraní plastovou trubici a nechá Kyleenu ve vaší děloze.
Váš poskytovatel zdravotní péče sníží vlákna na pravou délku.
Během umístění a po něm můžete zažít krvácení nebo závratě. Pokud vaše příznaky neproběhnou do 30 minut po umístění Kyleena, nemusí být umístěna správně.
Váš poskytovatel zdravotní péče vás prozkoumá, abyste zjistili, zda je Kyleena musí být odstraněna nebo nahrazena.
Mám zkontrolovat, zda je Kyleena na místě?
Ano, měli byste zkontrolovat, že Kyleena je ve správné poloze tím, že pocítí vlákna odstraňování. Je to dobrý zvyk to dělat 1krát za měsíc. Váš poskytovatel zdravotní péče by vás měl naučit, jak zkontrolovat, že Kyleena je na svém místě. Nejprve si umyjte ruce mýdlem a vodou. Můžete zkontrolovat dosažením až na horní část vagíny čistými prsty, abyste cítili vlákna odstraňování. Netahujte vlákna. Pokud se cítíte více než jen vlákna nebo pokud nemůžete cítit, že vlákna Kyleena nemusí být ve správné poloze a nemusí zabránit těhotenství. Vyvarujte se styku nebo používejte nehormonální záložní antikoncepci (jako jsou kondomy nebo spermicid) a požádejte svého poskytovatele zdravotní péče, aby zkontroloval, že Kyleena je stále na správném místě.
Jak brzy po umístění Kyleeny bych se měl vrátit ke svému poskytovateli zdravotní péče?
Pokud máte nějaké dotazy nebo obavy, zavolejte svému poskytovateli zdravotní péče (viz, kdy bych měl zavolat svému poskytovateli zdravotní péče?). Jinak byste se měli vrátit ke svému poskytovateli zdravotní péče na následnou návštěvu 4 až 6 týdnů poté, co je umístěna Kyleena, aby se ujistila, že Kyleena je ve správné poloze.
Mohu použít tampony nebo menstruační šálky s Kyleenou?
Ano, tampony nebo menstruační šálky mohou být použity s Kyleenou. S pečlivě měňte tampony nebo menstruační poháry, abyste se vyhnuli tahání vláken Kyleeny. Pokud si myslíte, že jste možná vytáhli Kyleenu na místě, vyhněte se pohlavnímu styku nebo použijte nehormonální záložní antikoncepci (jako jsou kondomy nebo spermicid) a kontaktujte svého poskytovatele zdravotní péče.
Co když při používání Kyleeny otěhotním?
Pokud si myslíte, že můžete být těhotná, zavolejte svému poskytovateli zdravotní péče. Pokud je to možné, také proveďte test těhotenství v moči. Pokud otěhotníte při používání Kyleeny, můžete mít mimoděložní těhotenství. To znamená, že těhotenství není v děloze. Neobvyklé vaginální krvácení nebo bolest břicha může být známkou mimoděložního těhotenství.
Ektopické těhotenství je lékařská pohotovost, která často vyžaduje chirurgický zákrok. Ektopické těhotenství může způsobit vnitřní krvácení neplodnost a dokonce i smrt.
Existují také rizika, pokud otěhotníte při používání Kyleeny a těhotenství je v děloze. U těhotenství, která pokračují u intrauterinního zařízení (IUD), může dojít k předčasnému porodu a dokonce smrti infekce. Z tohoto důvodu se váš poskytovatel zdravotní péče může pokusit odstranit Kyleenu, i když ji může způsobit potrat. Pokud Kyleena nelze odstranit, promluvte si s poskytovatelem zdravotní péče o výhodách a rizicích pokračování v těhotenství a možných účincích hormonu na vaše nenarozené dítě.
Pokud pokračujete v těhotenství, uvidíte svého poskytovatele zdravotní péče pravidelně. Okamžitě zavolejte svému poskytovateli zdravotní péče, pokud získáte příznaky podobné chřipce, horečka zimnice křeče, která krvácí bolest vaginálního výtoku nebo úniku tekutiny z vaší vagíny. To mohou být známky infekce.
Jak změní Kyleena moje období?
Během prvních 3 až 6 měsíců se vaše období může stát nepravidelnými a počet dnů krvácení se může zvýšit. Můžete také mít časté skvrny nebo krvácení světla. Některé ženy mají během této doby těžké krvácení. Během prvních několika týdnů můžete mít také křeče. Poté, co jste na chvíli použili Kyleenu, je pravděpodobné, že se počet krvácení a skvrnitých dnů zmenší. U některých obdobů žen se bude úplně zastavit. Když je Kyleena odstraněna, vaše menstruační období by se měla vrátit.
Je bezpečné kojit při používání Kyleeny?
Kyleenu můžete používat, když kojíte. Kyleena pravděpodobně neovlivní kvalitu nebo množství mateřského mléka nebo zdraví vašeho ošetřovatelského dítěte. Byly však hlášeny izolované případy snížené produkce mléka. Riziko, že Kyleena vstoupí do zdi dělohy (zabudovaná) nebo procházím stěnou dělohy, se zvýší, pokud je Kyleena vložena během kojení.
Bude Kyleena zasahovat do sexuálního styku?
Vy a váš partner byste neměli cítit Kyleenu během pohlavního styku. Kyleena je umístěna do dělohy, nikoli ve vagíně. Někdy může váš partner cítit vlákna. Pokud k tomu dojde, nebo pokud vy nebo váš partner zažijte bolest během sexuálního hovoru s poskytovatelem zdravotní péče.
Mohu mít MRI s Kyleenou na místě?
Kyleena can be safely scanned with MRI only under specific conditions. Before you have an MRI tell your healthcare provider that you have Kyleena an intrauterine device (IUD) in place.
Jaké jsou možné vedlejší účinky Kyleeny?
Kyleena can cause serious side effects including:
Okamžitě řekněte svému poskytovateli zdravotní péče, pokud máte některé z těchto známek PID: dlouhé nebo těžké krvácení neobvyklé vaginální výboj s nízkým břicho (žaludeční oblast) Bolestivá sexuální zimnice horečky Genitální léze nebo vředy.
- Ektopická těhotenství a intrauterinní těhotenské rizika. Existují rizika, pokud otěhotníte při používání Kyleeny (podívejte se, co když při používání Kyleeny otěhotním?).
- Životní infekce. Životní infekce může nastat během prvních několika dnů po umístění Kyleeny. Pokud si vyvinete těžkou bolest nebo horečku krátce po umístění Kyleena, okamžitě zavolejte svému poskytovateli zdravotní péče.
- Pánevní zánětlivé onemocnění (PID). Někteří uživatelé IUD dostávají vážnou pánevní infekci zvanou pánevní zánětlivé onemocnění. PID se obvykle sexuálně přenáší. Máte vyšší šanci získat PID, pokud máte vy nebo váš partner sex s jinými partnery. PID může způsobit vážné problémy, jako je neplodnost mimoděložní těhotenství nebo pánevní bolest, která nezmizí. PID se obvykle léčí antibiotiky. Vážnější případy PID mohou vyžadovat chirurgický zákrok, včetně odstranění dělohy (hysterektomie). Ve vzácných případech mohou infekce, které začínají jako PID, dokonce způsobit smrt.
- Perforace. Kyleena may go into the wall of the uterus (become embedded) or go through the wall of the uterus. This is called perforation. If this occurs Kyleena may no longer prevent pregnancy. If perforation occurs Kyleena may move outside the uterus a can cause internal scarring infection or damage to other organs a you may need surgery to have Kyleena removed. Excessive pain or vaginal bleeding during placement of Kyleena pain or bleeding that gets worse after placement or not being able to feel the threads may happen with perforation. The risk of perforation is increased if Kyleena is inserted while you are breastfeeding or if you have recently given birth.
- Vyhoštění. Kyleena may come out by itself. This is called expulsion. Vyhoštění occurs in about 4 out of 100 women. Excessive pain or vaginal bleeding during placement of Kyleena pain or bleeding that gets worse after placement or not being able to feel the threads may happen with expulsion. You may become pregnant if Kyleena comes out. If you think that Kyleena has come out avoid intercourse or use a non-hormonal back-up birth control (such as condoms or spermicide) a call your healthcare provider. The risk of expulsion is increased with insertion right after delivery or second-trimester abortion.
Mezi běžné vedlejší účinky Kyleeny patří:
- Krvácení bolesti nebo závratě během a po umístění. Pokud se tyto příznaky nezastaví 30 minut po umístění Kyleena, nemusí být umístěna správně. Váš poskytovatel zdravotní péče vás prozkoumá, abyste zjistili, zda je Kyleena musí být odstraněna nebo nahrazena.
- Změny v krvácení. Možná máte krvácení a špinění mezi menstruačními obdobími, zejména během prvních 3–6 měsíců. Někdy je krvácení zpočátku těžší než obvykle. Krvácení se však obvykle stává lehčí než obvykle a může být nepravidelné. Zavolejte svému poskytovateli zdravotní péče, pokud krvácení zůstává těžší než obvykle nebo se zvyšuje poté, co bude na chvíli světlo.
- Zmeškaná menstruační období. Asi 12 ze 100 žen přestane mít období po 1 roce používání Kyleeny. Máte -li nějaké obavy, že můžete být těhotná při používání Kyleeny proveďte test těhotenství v moči a zavolejte svému poskytovateli zdravotní péče. Pokud nemáte období po dobu 6 týdnů během Kyleena, volejte svého poskytovatele zdravotní péče. Když je Kyleena odstraněna, vaše menstruační období by se měla vrátit.
- Cysty na vaječníku. Asi 22 ze 100 žen pomocí Kyleeny se vyvíjí cystu na vaječníku. Tyto cysty obvykle zmizí sami za 2 až 3 měsíce. Avšak cysty mohou způsobit bolest a někdy cysty budou potřebovat chirurgický zákrok.
Mezi další běžné vedlejší účinky patří:
- Zánět nebo infekce vnější části vagíny (vulvovaginitida)
- Břicha nebo pánevní bolest
- Bolest hlavy nebo migréna
- akné or greasy skin
- Bolestivá období
- bolestivá nebo bolestivá prsa
Nejedná se o všechny možné vedlejší účinky s Kyleenou. Pro více informací se zeptejte svého poskytovatele zdravotní péče.
Zavolejte svého lékaře, kde najdete lékařskou radu ohledně vedlejších účinků. Můžete nahlásit vedlejší účinky FDA na 1-800-FDA-1088. Můžete také nahlásit vedlejší účinky společnosti Bayer Healthcare Pharmaceuticals na čísle 1-888-842-2937.
Poté, co byla Kyleena umístěna, kdy mám zavolat svému poskytovateli zdravotní péče?
Pokud je Kyleena náhodně odstraněna a během předchozího týdne jste měli vaginální styk, můžete být vystaveni riziku těhotenství a měli byste mluvit s poskytovatelem zdravotní péče.
Pokud máte nějaké obavy ohledně Kyleeny, zavolejte svému poskytovateli zdravotní péče. Nezapomeňte zavolat, pokud:
- Myslíš, že jsi těhotná
- mít pánevní bolest břicha nebo bolest během sexu
- mít neobvyklý vaginální výtok nebo vředy
- mají nevysvětlitelné příznaky nebo zimnice podobné horečce
- může být vystaven sexuálně přenosným infekcím (STIS)
- se obávají, že Kyleena možná byla vyloučena (vyšla)
- Nelze cítit vlákna Kyleeny
- rozvíjet velmi závažné nebo migrénové bolesti hlavy
- Ztělejatí kůže nebo bílých očí. To mohou být známky problémů jater.
- měli mrtvici or infarkt
- Staňte se HIV pozitivní nebo váš partner se stane pozitivním HIV
- mít závažné vaginální krvácení nebo krvácení, které vás trvá dlouho nebo se vás týká
Obecné rady ohledně bezpečného a efektivního používání Kyleeny.
Léky jsou někdy předepsány pro jiné podmínky než ty, které jsou uvedeny v letácích informací o pacientech. Pokud byste chtěli více informací, promluvte si se svým poskytovatelem zdravotní péče. Můžete požádat svého poskytovatele zdravotní péče o informace o Kyleeně, která je napsána pro zdravotnické pracovníky.
Jaké jsou ingredience v Kyleeně?
Aktivní složka: Levonorgestrel
Neaktivní ingredience: Silikonový polyethylenový stříbrný křemičitý síran s barvivem polypropylen měď ftalocyanin
Tyto informace o pacientech byly schváleny americkou správou potravin a léčiv.

