Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
Koagulační faktoryEspect
Shrnutí drog
Co je to Espect?
Esperoct [antihemofilní faktor (rekombinantní) glykopegylovaný-exei] je a koagulace Koncentrát faktoru VIII indikoval pro použití u dospělých a dětí s hemofilií A pro léčbu na vyžádání a kontrolu epizod krvácení Perioperační léčba krvácení a rutinní profylaxe ke snížení frekvence epizod krvácení. Espekt není indikován pro léčbu nemoci von Willebrand.
Jaké jsou vedlejší účinky Esperoctu?
Espect Topper
- kopřivka
- potíže s dýcháním
- Otok vašeho obličeje rty jazyk nebo krk
- svědění
- vyrážka
- necitlivost
- brnění
- horečka
- závrať
- nevolnost
- Rychlé srdeční rytmy
- těsnost hrudníku
- síť
- bledá kůže
- studený pot
- Lightheadedness
- mdloby
- Zvýšené epizody krvácení
- jakékoli krvácení, které se nezastaví a
- bolest na hrudi
Získejte lékařskou pomoc okamžitě, pokud máte výše uvedené příznaky.
Mezi běžné vedlejší účinky Espectu patří:
- vyrážka
- zarudnutí
- svědění a
- Reakce místa injekce
Pokud máte následující vážné vedlejší účinky, vyhledejte lékařskou péči nebo zavolejte na číslo 911:
- Vážné příznaky očí, jako je ztráta náhlého vidění rozmazané vidění vidění Vision Vision Eye Eye Eye Eye Eye Eye Eye Eye nebo vidět halos kolem světel;
- Vážné příznaky srdce, jako je rychlé nepravidelné nebo bušení srdečního rytmu; třepování v hrudi; dušnost; a náhlé závratě lightheadness nebo omdlení;
- Těžká zmatek bolesti hlavy zkroucený řečový rameno nebo slabost nohou Potíže se ztrátou chůze pocitu koordinace Pocit nestabilní velmi tuhé svaly vysoké horečky bohaté pocení nebo třes.
Tento dokument neobsahuje všechny možné vedlejší účinky a mohou dojít k jiným. Další informace o vedlejších účincích najdete u svého lékaře.
Dávkování pro Espect
Dávka ESPEROCT závisí na použití.
Jaké léčivé látky nebo doplňky interagují s Esperoctem?
Espekt může interagovat s jinými léky. Řekněte svému lékaři všechny léky a doplňky, které používáte.
Espekt během těhotenství nebo kojení
Řekněte svému lékaři, pokud jste těhotná nebo plánujete otěhotnět před použitím Esperoctu; Není známo, jak by to ovlivnilo plod. Není známo, zda Espect přechází do mateřského mléka nebo by to ovlivnilo kojící dítě. Před kojením se poraďte se svým lékařem.
Další informace
Náš esperort [antihemofilní faktor (rekombinantní) glykopegylovaný-exei] lyofilizovaný prášek pro roztok pro intravenózní použití vedlejších účinků Drug Center poskytuje komplexní pohled na dostupné informace o potenciálních vedlejších účincích při užívání tohoto léku.
Informace o drogách FDA
Popis pro Esperoct
ESPEROCT je sterilní ne-pygenní lyofilizovaný prášek bez sterilního konzervačního látek pro intravenózní injekci po rekonstituci s poskytnutým solným ředidlem. Aktivní složka v Esperoctu je rekombinantní analog lidského koagulačního faktoru VIII (FVIII) konjugovaného s molekulou polyethylenglykolu 40 kDa (PEG). ESPEROCT je formulován s následujícími pomocnými látkami: chlorid sodný l-histidin sacharóza polysorbát 80 l-methionin a chlorid vápenatý.
Aktivita FVIII v Esperoctu je stanovena pomocí chromogenního testu popsaného v evropské farmakopoeii. Přiřazení aktivity využívá referenční materiál FVIII, který je sledovatelný pro mezinárodní standard Světové zdravotnické organizace (WHO) pro FVIII koncentrát a vyhodnocuje vhodnými metodikami, aby zajistil přesnost výsledků. ESPEROCT je k dispozici v jednodávkách, které obsahují nominálně 500 1000 1500 2000 nebo 3000 IU FVIII. Každá lahvička Esperoctu je označena skutečnou činností FVIII. Po rekonstituci s dodávaným ředidlem (NULL,9% fyziologického roztoku) každý ML roztoku obsahuje přibližně 125 250 375 500 nebo 750 IU FVIII.
Protein FVIII v Esperoctu se produkuje v buňkách vaječníků čínského křečka (CHO) pomocí technologie rekombinantní DNA a obsahuje zkrácenou doménu B, která je O-glykosylovaná. Polypeptidová část molekuly má molekulární hmotnost 166 kDa (vypočteno bez posttranslačních modifikací) a představuje heterodimer těžkého řetězce a lehký řetězec, který je držen pohromadě nelalentními interakcemi. Rekombinantní protein FVIII je purifikován pomocí řady chromatografických kroků jedním z nich je afinitní chromatografie s použitím monoklonální protilátky k selektivně izolaci RFVIII z buněčného kultivačního média. Molekula PEG 40 kDa je konjugována s o-glykanovou skupinou domény B pomocí enzymatické reakce k vytvoření glykopegylovaného FVIII (FVIII-PEG). Proces čištění zahrnuje dva kroky virové clearance, jmenovitě detergentní (Triton X-100) léčba inaktivace obalených virů a filtrace 20 nm pro odstranění obávaných a nevyvinutých virů. Během výrobního procesu a formulace Esperoctu se nepoužívají žádné přísady lidského nebo zvířecího původu.
V krevním oběhu, když je FVIII-PEG aktivován trombinem, je část B-domény s připojenou pegem štěpena a výsledná aktivovaná FVIII (FVIIIA) má podobnou strukturu a funkci jako nativní FVIIIA.
Použití pro Espect
Espect ® [Antihemofilní faktor (rekombinantní) glykopegylated-exei] je rekombinantní koagulační koncentrát odvozený od DNA odvozeného od DNA, který je uveden pro použití u dospělých a dětí s hemofilií A pro:
- Léčba na vyžádání a kontrola epizod krvácení
- Perioperační řízení krvácení
- Rutinní profylaxe ke snížení frekvence epizod krvácení
Omezení použití
Espect ® není indikováno pro léčbu nemoci von Willebrand. (1)
Dávkování pro Espect
Pro intravenózní infuzi pouze po rekonstituci.
Dávka
- Dávka a trvání léčby závisí na závažnosti nedostatku faktoru VIII na místě a rozsahu krvácení a na klinickém stavu pacienta. Pečlivé sledování substituční terapie je nezbytné v případě hlavní chirurgického zákroku nebo epizody ohrožujících život.
- Každá lahvička Esperoctu ® Obsahuje označené množství rekombinantního faktoru VIII v mezinárodních jednotkách (IU). Jeden IU aktivity faktoru VIII odpovídá množství faktoru VIII v jednom mililitru normální lidské plazmy. Výpočet požadované dávky faktoru VIII je založen na empirickém zjištění, že jeden IU faktoru VIII na kg tělesné hmotnosti zvyšuje aktivitu plazmatického faktoru VIII o dva IU/DL.
On -Demand Léčba a kontrola epizod krvácení
Tabulka 1 lze použít k vedení dávkování Esperoctu ® Pro léčbu epizod krvácení.
Tabulka 1: Dávkování Esperoctu ® ovládat epizody krvácení
| Typ krvácení | Adolescenti/ dospělí ≥ 12 let Dávka (IU/kg) | Děti <12 years Dávka (IU/kg) | Další dávky |
| Menší | |||
| Časná hemartróza mírné krvácení nebo ústní krvácení | 40 | 65 | Jedna dávka by měla stačit |
| Mírný | |||
| Rozsáhlejší krvácení nebo hematom svalu hemartrózy | 40 | 65 | Další dávka může být podávána po 24 hodinách |
| Hlavní | |||
| Životní nebo končetiny ohrožující krvácení Gastrointestinální krvácení Intrakraniální intraabdominální nebo intrathorakální krvácení zlomeniny | 50 | 65 | Další dávka (y) může být podávána přibližně každých 24 hodin |
Perioperační řízení
Hladina dávky a intervaly dávky pro chirurgický zákrok závisí na postupu a místní praxi. Průvodce dávkováním s Esperoctem ® Během chirurgického zákroku (perioperační management) je uvedena v tabulce 2 níže.
Tabulka 2: Dávkování pro perioperační řízení s Esperoctem ®
| Typ chirurgie | Adolescenti/ dospělí ≥ 12 let Pre-operative Dávka (IU/kg) | Děti <12 years Pre-operative Dávka (IU/kg) | Další dávky |
| Menší | |||
| Včetně extrakce zubů | 50 | 65 | Další dávka (y) může být podávána po 24 hodinách v případě potřeby |
| Hlavní | |||
| Intrakraniální intraabdominální intrathorakální nebo náhradní chirurgie kloubů | 50 | 65 | Další dávky can be administered approximately every 24 hours for the first week a then approximately every 48 hours until wound healing has occurred |
Rutinní profylaxe
Dospělí a dospívající (≥ 12 let): Doporučená počáteční dávka je 50 IU Esperoctu ® na kg tělesné hmotnosti každé 4 dny.
Tento režim může být individuálně upraven na méně nebo častější dávkování na základě epizod krvácení.
Děti ( <12 years): A dose of 65 IU of Espect ® za kg tělesné hmotnosti dvakrát týdně. Tento režim může být individuálně upraven na méně nebo častější dávkování na základě epizod krvácení.
Dávkování (IU) = tělesná hmotnost (kg) × požadovaný faktor VIII zvyšuje (IU/DL nebo % normální) × 0,5
- Espect ® Může být také dávkováno, aby bylo dosaženo specifické úrovně cílového faktoru VIII, v závislosti na závažnosti hemofilie pro léčbu/kontrolu krvácení epizod nebo perioperační léčbu. Chcete -li dosáhnout konkrétní úrovně cílového faktoru VIII, použijte následující vzorec:
- Založte dávku a frekvenci Esperoctu ® o individuální klinické odpovědi. Pacienti se mohou lišit ve svých farmakokinetických a klinických reakcích.
- Pokud je provedeno monitorování aktivity faktoru VIII, použijte chromogenní nebo jednostupňový test srážení vhodný pro použití s Esperoctem ® [vidět Varování a preventivní opatření ].
Příprava a rekonstituce
- Před provedením rekonstitučních postupů vždy umyjte ruce a zajistěte, aby byla oblast čistá.
- Použijte aseptickou techniku během rekonstitučních postupů.
- Pokud dávka vyžaduje více než jednu lahvičku Esperoctu ® na infuzi rekonstiturujte každou lahvičku podle následujících pokynů.
Přehled ESPEROCT ® Balík
Přehled
Vial s Esperoctem ® prášek
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct.webp' > |
Rekonstituce
| ® vial and the pre-filled diluent syringe to room temperature. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-1.webp' > |
| ® vial. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-2.webp' > |
 |
| ® lahvička na plochém a pevném povrchu. Zatímco držíte ochrannou čepici, umístěte adaptér lahvičky na Esperoctu ® vial and press down firmly on the protective cap until the vial adapter spike penetrates the rubber stopper. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-4.webp' > |
 |
 |
 |
 |
 |
| ® vial until all of the powder is dissolved. Avoid shaking the vial and foaming the solution. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-10.webp' > |
- Přineste Espect ® Vial a předem naplněná stříkačka na teplotu pokojové teploty.
- Vyjměte plastovou uzávěrku z Esperoctu ® Vial.
- Gumová zátka na lahvičce otřete sterilním alkoholovým tamponem a nechte ji před použitím uschnout.
- Odstraňte ochranný papír z adaptéru lahvičky. Neodstraňujte adaptér lahvičky z ochranného uzávěru.
- Umístěte Espect ® lahvička na plochém a pevném povrchu. Zatímco držíte ochrannou čepici, umístěte adaptér lahvičky na Esperoctu ® Vial a pevně zatlačte na ochrannou čepici, dokud špička adaptéru lahvičky nepronikne gumovou zátkou.
- Ochranný uzávěr pečlivě vyjměte z adaptéru lahvičky.
- Uchopte prunžrovou tyč, jak je znázorněno na diagramu. Připevněte plunžrovou tyč k injekční stříkačce přidržením plunžrové tyče u širokého horního konce. Proměňte plunger tyč ve směru hodinových ručiček na gumový píst uvnitř předem naplněné stříkačky, dokud není pociťován odpor.
- Rozbijte kryt stříkačky z předem naplněné stříkačky na řeznutí prasknutím perforace uzávěru.
- Připojte předem naplněnou injekční stříkačku k adaptéru lahvičky otočením ve směru hodinových ručiček, dokud nebude zajištěna.
- Stisknutím tyče písem pomalu vstřikujte veškerý ředidlo do lahvičky.
- Bez odstranění injekční stříkačky jemně víří Espert ® lahvička, dokud se veškerý prášek nerozpustí. Vyvarujte se třesení lahvičky a pěny roztoku.
Správa
Pouze pro intravenózní infuzi
- Parenterální léčivé přípravky by měly být vizuálně kontrolovány na částice a zbarvení před podáním, kdykoli to roztok a nádoby povolí. Řešení by mělo být jasné a nemá žádné částice. Nepoužívejte, pokud jsou pozorovány částice nebo zbarvení.
- Nespravujte Esperocta ® ve stejné hadičce nebo nádobě s jinými léčivými přípravky.
- Spravovat Espect ® řešení okamžitě. Pokud ne uloží roztok do lahvičky s adaptérem lahvičky a stříkačkou připevněnou. Použijte Espect ® do 4 hodin při skladování při ≤ 86 ° F (30 ° C) nebo do 24 hodin při skladování v lednici při 36 ° F až 46 ° F (2 ° C až 8 ° C).
| ® vial and slowly draw the solution into the syringe. - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-11.webp' > |
- Invertujte Espect ® lahvička a pomalu nakreslete roztok do stříkačky.
- Odpojte stříkačku z adaptéru lahvičky otočením stříkačky proti směru hodinových ručiček.
- Připojte stříkačku k Luerově konci sady infuzní jehly.
- Naplňte rekonstituovaný espekt ® intravenózně pomalu během přibližně 2 minuty.
- Po infuzi bezpečně zlikvidujte stříkačku s infuzí, nastavte lahvičku s adaptérem lahvičky jakýkoli nepoužitý espekt ® a další odpadní materiály.
Pozor
Předem naplněná stříkačka je vyrobena ze skla s vnitřním průměrem špičky 0,037 palce a je kompatibilní se standardním konektorem Luer-block.
Některé bez potřebné konektory pro intravenózní katétry jsou nekompatibilní se skleněnými stříkačkami (například některé konektory s vnitřním hrotem, jako je Clave ® /Mikroklav ® Invision-plus ® Invision-plus CS ® Invision-plus junior ® Bietor ® ) a jejich použití může poškodit konektor a ovlivnit podávání. Pro správu Esperoctu ® Prostřednictvím nekompatibilních bez potřeb odstartujte rekonstituovaný produkt do standardní 10 ml sterilní plastové stříkačky Luer-Lock.
Jak dodáno
Formy a silné stránky dávkování
Espect ® je k dispozici jako sterilní bílá až bělavý lyofilizovaný prášek dodávaný v jednodávkových lahvičkách obsahujících nominálně 500 1000 1500 2000 nebo 3000 IU. Skutečná aktivita FVIII je vytištěna na každém Espeltu ® VIAL A KARTON.
Po rekonstituci se 4 ml ředidla fyziologického roztoku obsahuje rekonstituovaný roztok přibližně 125 250 375 500 nebo 750 IU na ml Esperoctu ® respektive.
- Espect ® je dodáván v balíčcích složených z jednodávkové lahvičky obsahující nominálně 500 1000 1500 2000 nebo 3000 IU faktoru VIII aktivity; mixpro ® Předem naplněná stříkačka na diluentu obsahující 0,9% solný roztok; a sterilní adaptér lahvičky s 25mikrometrovým filtrem, který slouží jako bezpodobní rekonstituční zařízení.
- Skutečná aktivita faktoru VIII v IU je uvedena na každém Esperoctu ® Karton a labera lahvičky.
Tabulka 9: Espect ® Prezentace
| Nominální pevnost v dávkování | Indikátor barev čepice | Lepenková krabice NDC Číslo | Komponenty |
| 500 IU | Červený | NDC 0169 8500 01 |
|
| 1000 IU | Zelený | NDC 0169 8100 01 |
|
| 1500 IU | Šedá | NDC 0169 8150 01 |
|
| 2000 IU | Žluť | NDC 0169 8200 01 |
|
| 3000 IU | Černý | NDC 0169 8300 01 |
|
| Iu = mezinárodní jednotky |
- Espekt ® Lahvičky jsou vyrobeny ze skla uzavřené chlobutylovou gumovou zátkou (ne vyrobenou z přírodního gumového latexu) a utěsněny hliníkovým uzávěrem.
- Předplněné ředidlové stříkačky jsou vyrobeny ze skla se silikonizovaným bromobutylovým gumovým písem (není vyrobeno s gumovým latexem).
- Uzavřené lahvičky a předem naplněné stříkačky jsou vybaveny manipulačním uzávěrem, který je vyroben z polypropylenu.
Skladování a manipulace
- Uložte Espect ® v původním balíčku pro ochranu Esperoctu ® lahvička ze světla.
- Uložte Espect ® ve formě prášku pod chlazením při 36 ° F až 46 ° F (2 ° C až 8 ° C) po dobu až 30 měsíců od data výroby až do data vypršení vypršení uvedeného na štítku. Během 30měsíční životnosti ® může být udržováno při teplotě místnosti:
- až 86 ° F (30 ° C) po dobu delší než 12 měsíců nebo
- až 104 ° F (40 ° C) po dobu ne déle než 3 měsíce
- Zaznamenejte datum na kartonu, když byl produkt odstraněn z chladničky. Nevracejte produkt do chladničky.
- Nezmrzněte esperokt ® .
- Použijte čekání ® do 4 hodin po rekonstituci, když se uloží při ≤ 86 ° F (30 ° C) nebo do 24 hodin, když je uložena v chladničce. Uložte rekonstituovaný produkt do lahvičky.
- Zlikvidujte jakýkoli nevyužitý rekonstituovaný produkt.
Vyrobeno: Novo Nordisk A/S DK-2880 Bagsvaerd Dánsko. Revidováno: září 2022
Vedlejší účinky lopid 600 mg
Vedlejší účinky pro Esperocta
Nejčastěji hlášená nežádoucí účinky (incidence ≥1%) v klinických studiích byla svědění vyrážky (Pruritus) a reakce na injekci.
Zkušenosti z klinických studií
Protože klinické studie se provádějí za široce proměnlivých podmínek, které nežádoucí reakce pozorované v klinických studiích léčiva nelze přímo porovnat s mírami v klinických studiích s jiným lékem a nemusí odrážet míru pozorované v klinické praxi.
Bezpečnost esperoctu ® byl hodnocen u 270 subjektů (202 adolescentů/dospělých a 68 dětí) v pěti prospektivních vícecentresových klinických studiích u dříve léčených pacientů (PTP) se závažnou hemofilií A ( <1% endogenous Facnar VIII activity) a no hisnary of inhibinars. All subjects received at least one dose of Espect ® . Dříve léčený pacient byl definován jako subjekt s anamnézou nejméně 150 expozičních dnů jinému faktoru VIII produkty (dospívající/dospělý subjekty) nebo 50 dnů expozice jinému faktoru VIII (pediatrické subjekty). Celková expozice Esperoctu ® bylo 80425 dnů expozice odpovídající 889 letům léčby pacientům.
Během klinických studií v nežádoucích účincích PTPS došlo rychlostí 0,10 událostí na pacientovou rok expozice. Nejčastěji hlášená nežádoucí účinky byla vyrážka (NULL,2%) injekční reakce (NULL,6%) zarudnutí (NULL,9%) a svědění (Pruritus) (NULL,5%).
Imunogenita
Subjekty byly monitorovány na neutralizační a neutralizační protilátky proti faktoru VIII polyethylenglykolu (PEG) a proteinu hostitelských buněk CHO. Jeden dříve ošetřený subjekt vyvinul potvrzené neutralizační protilátky proti faktoru VIII (NULL,5 jednotek Bethesda). Kromě toho měly dva subjekty přechodné nízké titr FVIII protilátky ( <5 Bethesda Units) test results at a single occasion. Anti-PEG antibodies of no clinical consequence were detected in 45 subjects 32 of whom had pre-existing anti-PEG antibodies. Nine subjects developed anti-CHO host cell protein antibodies of no clinical consequence.
Detekce protilátek je vysoce závislá na citlivosti a specificitě testu. Pozorovaný výskyt protilátky (včetně neutralizační protilátky) pozitivity v testu může být navíc ovlivněn několika faktory, včetně metodiky pro testovací metodiku, která manipuluje načasování vzorku doprovodných léků a základní onemocnění.
Zážitek z postmarketingu
Během schválení Esperoctu byly identifikovány následující nežádoucí účinky ® . Protože tyto reakce jsou hlášeny dobrovolně z populace nejisté velikosti, není vždy možné spolehlivě odhadnout jejich frekvenci nebo vytvořit kauzální vztah k expozici léčiva.
Snížená aktivita faktoru VIII: Zprávy o snížené aktivitě faktoru VIII v nepřítomnosti detekovatelných inhibitorů faktoru VIII u dříve léčených pacientů (PTP) ® Z jiných produktů faktoru VIII.
Lékové interakce pro Esperocta
Žádné informace
Varování pro Espect
Zahrnuto jako součást 'OPATŘENÍ' Sekce
Opatření pro Espect
Reakce přecitlivělosti
S esperotem jsou možné reakce hypersenzitivního alergického typu včetně anafylaxe ® . Produkt obsahuje stopy proteinů křečka, které mohou u některých pacientů způsobit alergické reakce [viz POPIS ]. Early signs of allergic reactions which can progress na anaphylaxis may include angioedema těsnost hrudníku potíže s dýcháním síť vyrážka kopřivka a svědění. Observe patients for signs a sympnams of acute hypersensitivity reactions particularly during the early phases of exposure na the product. Discontinue use of Espect ® Pokud se vyskytnou reakce alergického nebo anafylaktického typu a zahájí vhodnou léčbu.
Neutralizující protilátky
Po podání Esperoctu došlo k tvorbě neutralizačních protilátek (inhibitorů) na faktor VIII ® . Sledujte pacienty pro vývoj inhibitorů faktoru VIII vhodnými klinickými pozorováními a laboratorními testy. Pokud se očekává, že hladiny plazmy faktoru VIII nejsou dosaženy nebo pokud krvácení není kontrolováno po Esperově ® Podávání má podezření na přítomnost inhibitoru (neutralizační protilátka) [Viz Monitorování laboratorních testů ].
Monitorování laboratorních testů
Pokud je provedeno monitorování faktoru VIII ® [vidět Dávkování a podávání ].
Úrovně aktivity faktoru VIII mohou být ovlivněny typem aktivovaného částečného tromboplastinového času (APTT) použitého v testu. Některá APTT činidla na bázi oxidu křemičitého mohou podceňovat aktivitu Esperoctu ® až o 60%; Ostatní činidla mohou aktivita přeceňovat o 20%. Pokud není k dispozici odpovídající jednostupňové srážení nebo chromogenní test, použijte referenční laboratoř.
Pokud krvácení není ovládáno doporučenou dávkou Esperoctu ® nebo pokud se nedosáhne očekávané úrovně aktivity faktoru VIII v plazmě, proveďte test Bethesda k určení, zda jsou přítomny inhibitory faktoru VIII.
Informace o poradenství pro pacienta
Poradit pacienty:
- Přečíst značení pacienta schváleného FDA ( Informace o pacientu a Pokyny pro použití ).
- Že hypersenzitivní reakce nebo anafylaxe hypersenzitivity alergického typu jsou možné s použitím Esperoctu ® . Informujte pacienty o časných známkách reakcí přecitlivělosti, včetně vyrážkových úlů, které svědí těsnost obličeje otoku hrudníku a sípání. Doporučujte pacientům, aby ukončili použití Esperoctu ® okamžitě a kontaktujte svého poskytovatele zdravotní péče a/nebo okamžitě vyhledejte nouzovou péči, pokud k těmto příznakům dojde.
- Kontaktujte svého poskytovatele zdravotní péče nebo léčebné zařízení pro další léčbu a/nebo hodnocení, pokud zažijí nedostatek klinické reakce na substituční terapii faktoru VIII, protože se jedná o projev inhibitoru.
Neklinická toxikologie
Zhodnocení mutageneze karcinogeneze plodnosti
Mutageneze karcinogeneze a zhoršení studií plodnosti u zvířat nebyly provedeny.
Použití v konkrétních populacích
Těhotenství
Shrnutí rizika
S Esperoctem neexistují žádná data ® Použití u těhotných žen k určení, zda existuje riziko spojené s drogami. Studie reprodukce zvířat nebyly provedeny s Espeltem ® . Není známo, zda esperoct ® může způsobit poškození plodu při podávání těhotné ženě nebo může ovlivnit plodnost.
V americké obecné populaci odhadované riziko na pozadí major vrozená vada a miscarriage in clinically recognized pregnancies is 2–4% a 15–20% respektive.
Laktace
Shrnutí rizika
Neexistují žádné informace týkající se přítomnosti Esperoctu ® V lidském mléce účinek na kojené dítě a účinky na produkci mléka. Vývojové a zdravotní přínosy kojení by měly být zváženy spolu s klinickou potřebou espektu matky ® a any potential adverse effects on the breastfed infant from Espect ® nebo z podkladového stavu matky.
Dětské použití
Bezpečnost a účinnost byla hodnocena u 93 dříve léčených dětských pacientů <18 years of age who received at least one dose of Espect; all received routine prophylaxis [vidět Klinické studie ]. Thirty-four (34) of these subjects (36.6%) were 1 až <6 years of age; 34 subjects (36.6%) were 6 až <12 years of age; a 25 subjects (27%) were 12 až <18 years of age. Pharmacokinetic parameters were evaluated for 27 of these subjects who were treated with Espect ® [vidět Klinická farmakologie ].
Žádný rozdíl v bezpečnostním profilu Esperoctu ® byl pozorován mezi dříve léčenými pediatrickými subjekty a dospělými subjekty. Farmakokinetické studie u dětí <12 years of age demonstrated higher clearance a shorter half-life a lower incremental recovery of Facnar VIII compared na adults but the pharmacokinetic parameters are comparable between young children (1– <6 years) a older children (6- <12 years). Because clearance (per kg body weight) is higher in children ( <12 years) a higher dose a more frequent dosing may be needed in this population [vidět Klinická farmakologie ].
Geriatrické použití
Klinické studie espektu ® nezahrnovalo dostatečné množství subjektů ve věku 65 let a více, aby se určilo, zda reagují jinak než mladší předměty. Jiné hlášené klinické zkušenosti nezjistily rozdíly v odpovědích mezi staršími a mladšími pacienty. Obecně by měl být výběr dávky pro staršího pacienta opatrný, obvykle začínající na dolním konci rozsahu dávkování, což odráží větší frekvenci snížené funkce ledvin nebo srdeční jater a doprovodným onemocněním a jinou lékovou terapií.
Informace o předávkování Esperoctu
Žádné informace
Kontraindikace pro Espect
Espect ® je kontraindikován u pacientů, kteří mají přecitlivělost na Espelt ® nebo jeho komponenty (včetně proteinů křečka) [viz Varování a preventivní opatření a POPIS ].
Klinická farmakologie for Esperoct
Mechanismus působení
Espect ® Glykopegylovaná forma rekombinantního anti-hemofilního faktoru dočasně nahrazuje chybějící koagulační faktor VIII potřebný pro účinnou hemostázu u vrozené hemofilie A. Faktor VIII v Esperoctu ® je konjugován na 40 kDa polyethylenglykolovou molekulu, která zvyšuje poločas a snižuje clearance ve srovnání s nepegylovanou molekulou.
Farmakodynamika
Správa Esperoctu ® Zvyšuje plazmatické hladiny faktoru VIII a může dočasně opravit koagulační defekt u pacientů s hemofilií A, což se odráží snížením aktivovaného částečného tromboplastinového času (APTT).
Farmakokinetika
Všechny farmakokinetické studie s Esperoctem ® byly prováděny u dříve léčených subjektů s těžkou hemofilií A (faktor VIII <1%). In natal 129 single-dose pharmacokinetic profiles of Espect ® byly vyhodnoceny u 86 subjektů (včetně 24 pediatrických subjektů 1– <12 years).
Tabulka 3 ukazuje data pro subjekty, které každý obdrželo jednu dávku 50 IU/kg. Vzorky plazmy byly analyzovány pomocí jednostupňového srážení. Došlo k trendu rostoucího přírůstkového zotavení a AUC a snižování clearance s věkem.
Tabulka 3: Parametry PK s jednou dávkou ESPEROCT ® 50 IU/kg podle věku pomocí jednostupňového srážení (geometrický průměr (CV%))
| Parametr PK | 1 až <6 years | 6 až <12 years | 12 až <18 years | > 18 let |
| Počet předmětů | N = 12 | N = 10 | N = 3 | N = 42 |
| Počet profilů | 12 | 10 | 5 | 78 |
| IR (IU / D D D D DI) Per I / KG) a | 1,82 (32) | 1.67 (22) | 2.45 (16) | 2.53 (24) |
| FVIII Recovery (IU/DL) a | 103.2 (27) | 98.7 (18) | 117.7 (14) | 130.4 (26) |
| t 1/2 (hodiny) | 14.7 (27) | 13.8 (32) | 17.4 (39) | 21.7 (33) |
| Aucinf (iu*hodina/dl) | 2305 (42) | 2197 (38) | 3063 (40) | 4110 (38) |
| CL (ML/Hour/KG) | 2.4 (42) | 2.7 (42) | 1.6 (39) | 1.2 (34) |
| VSS (ML/KG) | 44.2 (25) | 47.3 (28) | 36.4 (12) | 37.3 (26) |
| MRT (hodiny) | 18.1 (27) | 17.8 (35) | 23.4 (43) | 27.4 (28) b |
| Parametry PK jsou uvedeny v geometrickém průměru. Zkratky: IR = přírůstkové zotavení; t 1/2 = terminál poločas; AUC = oblast pod časovým profilem aktivity FVIII; Cl = clearance; VSS = objem distribuce v ustáleném stavu; MRT = průměrná doba pobytu; CV% = variační koeficient a Obnova IR a FVIII byla hodnocena 30 minut po dávkování 50 IU/kg u pacientů ≥ 12 let a 60 minut po dávkování 50 IU/kg (první vzorek) pro děti <12 years. bCalculation based on 64 profiles. |
Při hodnocení PK s jednou dávkou u dospělých subjektů, jejichž index tělesné hmotnosti (BMI) se pohyboval od 17-35 kg/m 2 Rozdíly byly zaznamenány pro jednotlivce, kteří měli nadváhu (BMI 25 - <30 kg/m 2 ) a obézní (BMI 30 - <35 kg/m 2 ). Incremental recovery was increased by approximately 17% a 41% AUC was increased by approximately 10% a 27% a clearance was decreased by approximately 8% a 23% respectively all in comparison na those subjects with BMI <25 kg/m 2 . Neexistují dostatečné údaje, které by doporučily specifické úpravy dávky pro pacienty s nadváhou a obézní. Dávka může být podle potřeby upravena podle uvážení předepisujícího lékaře.
Pozorované předběžné dávky (koryta) a podávkování (vrchol) plazmatický faktor VIII aktivita v ustáleném stavu během profylaktického ošetření esperokt ® jsou uvedeny v tabulce 4 podle dávkového režimu a věkového rozmezí.
Tabulka 4: Koryto a maximální plazmatická aktivita FVIII v ustáleném stavu podle věkového a dávkového režimu chromogenního testu (geometrický průměr [95% CI])
Jaký druh léku je tramadol
| Dávka Regimen | 60 IU/KG dvakrát týdně ** (50–75 IU/kg) | 50 IU/KG Q4D* | 75 IU/KG Q7D* | |||
| Věkové rozmezí | <6 years | 6- <12 years | 12- <18 years | ≥ 18 let | 12- <18 years | ≥ 18 let |
| Ne. Pacienti | N = 31 | N = 34 | N = 23 | N = 143 | N = 6 | N = 29 |
| CORLUGH IU/DL | 1.2 (NULL,8; 1,6) | 2.0 (1.5; 2.7) | 2.7 (1.8; 4.0) | 3.0 (2.6; 3.5) | 0.6 (NULL,2; 1,6) | 1.3 (NULL,9; 2,0) |
| Vrchol IU/DL | 125.0 (NULL,7; 131,6) | 143.3 (NULL,8; 150.2) | 125.1 (NULL,0; 135,0) | 137.9 (133.9; 142.2) | 198.0 (NULL,8; 235,2) | 197.9 (NULL,9; 212.7) |
| *Data zahrnutá v analýze: Adolescents/Adults Hlavní fáze až do návštěvy 8 (konec hlavní fáze) 50 IU/KG Q4D a prodloužení 1 pro 75 IU/KG Q7D. Do analýz jsou zahrnuty pouze měření shromážděná v ustáleném stavu pro danou profylaxis léčbu. ** Data zahrnutá v analýze: Pediatrická hlavní fáze 60 IU/kg (50–75 IU/kg) dvakrát týdně. Do analýz jsou zahrnuty pouze měření shromážděná v ustáleném stavu pro danou profylaxis léčbu. |
Čas aktivity faktoru VIII nad 5%
Profily aktivity aktivity faktoru VIII v ustáleném stavu byly odhadnuty pomocí modelu s jedním kompartmentem s eliminací prvního řádu s parametry PK clearance (CL) a objemem distribuce (tabulka 5). Farmakokinetické předpovědi ukázaly, že ve všech věkových skupinách budou pacienti dávkováni dvakrát týdně (dávkový interval střídá se mezi 3 a 4 dny) nebo Q4D nad 5% aktivitou faktoru VIII (tj. V rozsahu mírné hemofilie) po většinu času (72–95% času). Pacienti dávkovaní s 50 IU/kg každé 4 dny budou nad 1% aktivitou faktoru VIII 100% dávkovacího intervalu. Předpokládá se, že pacienti s 75 IU/kg každých 7 dnů jsou nad 57% času a nad 1% po dobu 83% času.
Tabulka 5: Odhad špičkových a korytových aktivity FVIII v ustáleném stavu a čas na 5% činnost FVIII pro Esperoct ®
| Dávka regimen | 60 IU/KG (50–75 IU/kg) dvakrát týdně | 50 IU/KG dvakrát týdně | 50 IU/KG Q4d | 75 IU/KG Q7d |
| Věkové rozmezí | <12 years | ≥ 12 let | ≥ 12 let | ≥ 12 let |
| Peak FVIII Aktivita (%) | 110/112* | 133/138* | 132 | 194 |
| Aktivita koryta FVIII (%) | 2,8/0,8* | 8.6/3.6* | 3.5 | 0.3 |
| Čas do 5% aktivity FVIII (dny) | 2,5/2,5* | 3.6/3.6* | 3.6 | 4.0 |
| % času v dávkovacím intervalu nad 5% FVIII aktivita | 72 | 95 | 90 | 57 |
| *Hodnoty dvakrát týdně jsou zobrazeny jako 3 den/4 den. Pro analýzu se používá pouze 50 dat IU/kg. |
Toxikologie zvířat a/nebo farmakologie
U potkanů s nedostatkem s nedostatkem nebyly pozorovány žádné nepříznivé účinky intravenózně injikované Esperoctem ® (50-1200 IU/ kg/ injekce) jednou za 4. den po dobu 52 týdnů. Nebyl detekován žádný důkaz o akumulaci polyethylenglykolu imunohistochemickým zbarvením mozkové tkáně včetně choroidního plexu.
Klinické studie
Bezpečnost a účinnost Esperoctu ® byly vyhodnoceny v pěti nadnárodních studiích s otevřenými značkami u mužských subjektů s těžkou hemofilií A ( <1% endogenous Facnar VIII activity). One trial was subsequently partially raomized na evaluate two different prophylaxis regimens. All subjects were previously treated which was defined as having received other Facnar VIII products for ≥150 exposure days for adolescents a adults a ≥50 exposure days for pediatric subjects. The key exclusion criteria across trials included known or suspected hypersensitivity na trial or related products a known hisnary of Facnar VIII inhibinars or current inhibinar ≥0.6 Bethesda units (BU).
Hodnocení účinnosti zahrnovalo 254 subjektů, kteří obdrželi alespoň jednu dávku Esperoctu ® V následujících pokusech:
- Zkouška dospívajících/dospělých: Tato zkouška zahrnovala 186 subjektů 161 dospělých (18 až 65 let) a 25 adolescentů (12 <18 years old); it consisted of a Main Phase a optional Extension Phase. During the Main Phase 175 subjects received the prophylaxis regimen which consisted of 50 IU/KG every 4 days (Q4d) while 12 adults chose na be treated on-dema. (One subject changed from on-dema na prophylaxis a is counted in both groups.) Thirteen (7%) of 175 adults in the prophylaxis arm modified their dosing regimen na Q3-4D dosing for ease of use. All subjects received at least one dose of Espect ® a are evaluable for safety a efficacy. A natal of 165 subjects (91%) completed the Main Phase of this trial.
- Prodloužení: Toto prodloužení porovnávalo dvě dávkové režimy: 75 IU/kg každých 7 dní (Q7D) a 50 IU/kg Q4D. Randomizace byla otevřena subjektům, kteří zažili 2 nebo méně krvácení během posledních 6 měsíců v hlavní fázi.
- Pediatrická zkouška: Tato zkouška zahrnovala 68 subjektů, které byly rovnoměrně rozděleny 34 v každé věkové skupině 0– <6 a 6- <12 years of age. All subjects received the same prophylaxis regimen of approximately 65 IU/kg (50–75 IU/kg) dvakrát týdně. A natal of 63 subjects (93%) completed the Main Phase.
- Chirurgická studie: V chirurgické studii 33 Dříve léčených adolescentů/dospělých podstoupilo 45 hlavních operací. Hladina dávky esperoctu ® byla vybrána tak, aby byla zaměřena na aktivitu FVIII alespoň podle doporučení Světové federace hemofilie (WFH). Po dokončení chirurgického pokusu se všechny subjekty vrátily do adolescentního/dospělého pokusu.
Léčba na vyžádání a kontrola epizod krvácení
V 171 z 254 subjektů v rámci dokončených klinických hodnocení bylo hlášeno 1506 krvácení a nejběžnějšími typy krvácení byly kloubní (NULL,2%) svaly (NULL,5%) a subkutánní (NULL,9%). Tabulka 6 shrnuje účinnost při kontrole epizod krvácení podle věku.
Dávkas used for treatment of bleeding episodes depended on age treatment regimen a the severity of the bleed.
Z 1407 mírných a středních epizod krvácení u všech subjektů ve studii dospívajících/dospělých byla střední dávka 42 IU/kg. U subjektů, které byly na rameni na vyžádání, byla střední počáteční dávka 28 IU/kg a 88,4% krvácení bylo úspěšně léčeno jednou dávkou. U subjektů, které dostávaly rutinní profylaxi, byla střední počáteční dávka 52 IU/kg a 76,4% krvácení bylo úspěšně léčeno jednou dávkou. Z 15 závažných krvácení 12 (80%) vyžadovalo více než jednu dávku s celkovou střední dávkou 111 IU/kg.
V pediatrické studii 70 mírných/středních krvácení u dětí <12 years old receiving routine prophylaxis were treated with a median initial dose of 64 IU/kg per injection with 63% treated with a single injection. When needed additional median doses of 62 IU/kg were used at approximately 24 hour intervals. The median natal dose was 70 IU/kg per bleed.
Tabulka 6: Shrnutí účinnosti při kontrole epizod krvácení podle věku
| Věkové rozmezí | <6 years N = 34 | 6 - <12 years N = 34 | 12 - <18 years N = 25 | ≥ 18 let N = 161 | Celkový N = 254 | |
| 30 | 40 | 112 | 1324 | 1506 | ||
| 1-2 | 76,7% | 82,5% | 88,4% | 95,5% | 94,3% | |
| > 2 | 23,3% | 17,5% | 11,6% | 4,5% | 5,7% | |
| Reakce na první léčbu | Výborný/ dobrý | 80,0% | 77,5% | 75,0% | 88,7% | 87,3% |
| Mírný | 13,3% | 17,5% | 17,9% | 10,3% | 11,1 % | |
| Definice hemostatické odpovědi: Vynikající: Náhlé úlevy od bolesti a/nebo jednoznačné zlepšení objektivních příznaků krvácení do přibližně 8 hodin po jedné injekci. Dobré: definitivní úleva od bolesti a/nebo zlepšení příznaků krvácení do přibližně 8 hodin po jedné injekci, ale možná vyžaduje více než jednu injekci pro úplné rozlišení. Mírný: Probable or slight beneficial effect within approximately 8 hours after the first injection; usually requiring more than one injection. |
Perioperační řízení
Analýza účinnosti Esperoctu ® V perioperačním řízení zahrnovalo 45 hlavních chirurgických zákroků prováděných u 33 dospívajících a dospělých subjektů. Postupy zahrnovaly 15 kloubních náhrad 9 artroskopických ortopedických intervencí 17 dalších ortopedických intervencí a 4 neortopedické operace.
Klinické hodnocení hemostatické odpovědi během velké chirurgické zákroky bylo hodnoceno pomocí čtyřbodové stupnice vynikajícího dobrého mírného nebo žádného. Hemostatický účinek Esperoctu ® byl hodnocen jako vynikající nebo dobrý ve 43 ze 45 operací (NULL,6%), zatímco účinek byl hodnocen jako střední ve 2 operacích (NULL,4%). Žádná chirurgie neměla výsledek hodnoceno jako žádný nebo chybějící.
Střední předoperační dávka pro dospělé a adolescenty podstupující hlavní operace byla 52 IU/ kg a střední celková dávka byla 702 IU/ kg. Během pooperačních dnů 1-6 byla střední dávka 32 IU/kg v přibližně 24 hodinových intervalech. Během pooperačních dnů 7-14 byla střední dávka 36 IU/kg v přibližně 28 hodinových intervalech. Počet dávek a trvání léčby se lišil postupem.
Rutinní profylaxe In Adolescents/Adults
Účinnost Esperoctu ® U rutinní profylaxe s dávkováním Q4D byla prokázána pro populaci dospělých/ adolescentů (viz tabulka 7). V prodloužení části studijní léčby nebylo zavedeno úspěch Q7D ramene. Během hlavní fáze zkoušky dospívajících/dospělých mělo 186 subjektů celkem 159 let expozice. Střední roční anualizovaná míra krvácení (ABR) pro ošetřené krvácení u dospělých a dospívajících léčených každé 4 dny byla 1,2 (IQR: 0,0: 4,3) a průměrná ABR byla 3,0 (SD: 4,7). Při zahrnutí všech krvácení (ošetřených a neošetřených) byl střední ABR 1,2 (IQR: 0,0; 4,7) a průměrný ABR byl 3,3 (SD: 4,9).
Tabulka 7: Účinnost u dospívajícího/dospělého profylaxe středního a průměrného ABR podle věkového léčebného režimu a typu krvácení
| Věkové rozmezí | Profylaxe | Na vyžádání | ||
| 12-17 years | 18–70 let | 12-70 years | 18–70 let | |
| 25 | 150 | 175 | 12 | |
| Průměrná doba léčby (roky) | 0.85 | 0.81 | 0.82 | 1.33 |
| Ošetřené krvácení | ||||
| with bleeds (%) | 19 (76) | 86 (57) | 105 (60) | 12 (100) |
| without bleeds (%) | 6 (24) | 64 (43) | 70 (40) | 0 |
| 67 | 369 | 436 | 532 | |
| Medián ABR (IQR) | 2.2 (NULL,9; 4,7) | 1,2 (NULL,0; 3,7) | 1,2 (NULL,0; 4,3) | 30.9 (NULL,6; 38,5) |
| Střední ABR (SD) | 3.5 (3.9) | 2.9 (4.8) | 3.0 (4.7) | 31.9 (19.1) |
| Všechny krvácení (ošetřené a neléčené) | ||||
| with bleeds (%) | 19 (76) | 88 (59) | 107 (61) | 12 (100) |
| without bleeds (%) | 6 (24) | 62 (41) | 68 (39) | 0 |
| * | 72 | 386 | 458 | 536 |
| Medián ABR (IQR) | 2.2 (NULL,9; 6,0) | 1,2 (NULL,0; 4,3) | 1,2 (NULL,0; 4,7) | 31.3 (NULL,6; 38,9) |
| Střední ABR (SD) | 3.7 (4.1) | 3.2 (5.1) | 3.3 (4.9) | 32.2 (19.1) |
| Ošetřené spontánní krvácení | ||||
| with bleeds (%) | 11 (44) | 65 (43) | 76 (43) | 12 (100) |
| without bleeds (%) | 14 (56) | 85 (57) | 99 (57) | 0 |
| 30 | 221 | 251 | 415 | |
| Medián ASBR (IQR) | 0,0 (NULL,0; 1,5) | 0,0 (NULL,0; 1,9) | 0,0 (NULL,0; 1,8) | 19.4 (NULL,1; 31,0) |
| Střední ASBR (SD) | 1.4 (2.4) | 1.8 (3.7) | 1.7 (3.5) | 24.5 (17.3) |
| Ošetřené traumatické krvácení | ||||
| with bleeds (%) | 16 (64) | 57 (38) | 73 (42) | 10 (83) |
| without bleeds (%) | 9 (36) | 93 (62) | 102 (58) | 2 (17) |
| 37 | 146 | 183 | 110 | |
| Medián ATBR (IQR) | 1,3 (NULL,0; 2,6) | 0,0 (NULL,0; 1,4) | 0,0 (NULL,0; 1,7) | 4.3 (NULL,8; 9,9) |
| Střední ATBR (SD) | 2.1 (2.9) | 1.1 (2.2) | 1.2 (2.3) | 6.1 (6.2) |
| Ošetřené krvácení kloubů | ||||
| with bleeds (%) | 16 (64) | 74 (49) | 90 (51) | 12 (100) |
| without bleeds (%) | 9 (36) | 76 (51) | 85 (49) | 0 |
| 37 | 288 | 325 | 309 | |
| Medián AJBR (IQR) | 1,2 (NULL,0; 2,8) | 0,0 (NULL,0; 2,8) | 0,9 (NULL,0; 2,8) | 19.4 (4.5; 28,8) |
| Průměr AJBR (SD) | 1.8 (2.2) | 2.3 (4.3) | 2.2 (4.1) | 19.7 (15.1) |
| ABR = anualizovaná míra krvácení; IQR = mezikvartilní rozsah 25. percentil až 75. percentil; SD = standardní odchylka; ASBR = anualizovaná míra spontánního krvácení; ATBR = anualizovaná traumatická míra krvácení; AJBR = anualizovaná míra krvácení kloubů. *Odráží všechny krvácení hlášené pacienty, včetně pacientů, kde nebyl podáván žádný espekt |
Rutinní profylaxe In Děti <12 Years Of Age
Celkově 68 dětí pod 12 let dostávalo profylaktickou léčbu ESPEROCT v průměrné dávce přibližně 65 IU/kg dvakrát týdně. Profylaktický účinek ESPEROCT byl prokázán střední mírou ABR 2,0 (IQR: 0,0; 2,8) a 2,0 (IQR: 0,0; 4,2) pro ošetřené krvácení a všechny krvácení (viz tabulka 8). Průměrná ABR (SD) pro ošetřené krvácení a všechny krvácení byly 3,1 (NULL,1) a 4,4 (NULL,7). Ze 68 dětí 22 (32%) nezaznamenalo žádné epizody krvácení a 29 (43%) nezažilo žádné epizody krvácení, které vyžadovaly léčbu během hlavní fáze studie. Z 13 subjektů se 17 zdokumentovanými cílovými klouby na začátku 10 subjektů (77%) a 14 cílových kloubů (82%) neměly během hlavní fáze studie žádné krvácení.
Tabulka 8: Účinnost ve střední profylaxi a průměrného ABR podle věku a typu krvácení
| Věkové rozmezí | Medián ASBR (IQR)Profylaxe Regimen | ||
| <6 years** | 6 až <12 years | 0 až <12 years | |
| N = 34 | N = 34 | N = 68 | |
| Průměrná doba léčby (roky) | 0.46 | 0.51 | 0.48 |
| Ošetřené krvácení | |||
| with bleeds (%) | 19 (56) | 20 (59) | 39 (57) |
| without bleeds (%) | 15 (44) | 14 (41) | 29 (43) |
| 30 | 40 | 70 | |
| Medián ABR (IQR) | 1,9 (NULL,0; 2.1) | 2,0 (NULL,0; 3,9) | 2,0 (NULL,0; 2,8) |
| Střední ABR (SD) | 3.9 (9.7) | 2.3 (2.9) | 3.1 (7.1) |
| Všechny krvácení (ošetřené a neléčené) | |||
| with bleeds (%) | 20 (59) | 26 (77) | 46 (68) |
| without bleeds (%) | 14 (41) | 8 (24) | 22 (32) |
| * | 41 | 65 | 106 |
| Medián ABR (IQR) | 2,0 (NULL,0; 4,0) | 2.0 (1.9; 6.0) | 2,0 (NULL,0; 4,2) |
| Střední ABR (SD) | 5.0 (11.9) | 3.8 (3.6) | 4.4 (8.7) |
| Ošetřené spontánní krvácení | |||
| with bleeds (%) | 6 (18) | 7 (21) | 13 (19) |
| without bleeds (%) | 28 (82) | 27 (79) | 55 (81) |
| 9 | 10 | 19 | |
| Medián ASBR (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 0,0) |
| Střední ASBR (SD) | 2.1 (7.3) | 0,6 (NULL,5) | 1.3 (5.3) |
| Ošetřené traumatické krvácení | |||
| with bleeds (%) | 15 (44) | 17 (50) | 32 (47) |
| without bleeds (%) | 19 (56) | 17 (50) | 36 (53) |
| 20 | 30 | 50 | |
| Medián ATBR (IQR) | 0,0 (NULL,0; 2,0) | 0,9 (NULL,0; 2,0) | 0,0 (NULL,0; 2,0) |
| Střední ATBR (SD) | 1.7 (4.0) | 1.7 (2.5) | 1.7 (3.3) |
| Ošetřené krvácení kloubů | |||
| with bleeds (%) | 7 (21) | 12 (35) | 19 (28) |
| without bleeds (%) | 27 (79) | 22 (65) | 49 (72) |
| 10 | 24 | 34 | |
| Medián AJBR (IQR) | 0,0 (NULL,0; 0,0) | 0,0 (NULL,0; 2,0) | 0,0 (NULL,0; 2,0) |
| Průměr AJBR (SD) | 1.5 (6.3) | 1.4 (2.4) | 1.5 (4.7) |
| ABR = anualizovaná míra krvácení; IQR = mezikvartilní rozsah 25. percentil až 75. percentil; SD = standardní odchylka; ASBR = anualizovaná míra spontánního krvácení; ATBR = anualizovaná traumatická míra krvácení; AJBR = anualizovaná míra krvácení kloubů *Odráží všechny krvácení hlášené pacienty, včetně pacientů ® byl podáván ** Zvýšené průměrné ABR jsou způsobeny subjekty, které se stáhly ze studie, jejichž míra krvácení byla extrapolována na jeden rok |
Informace o pacientovi pro Esperocta
Espect ®
[Antihemofilní faktor (rekombinantní) glykopegylovaný-exei]
Přečtěte si informace o pacientovi a pokyny k použití, které přicházejí s Esperoctem ® Než začnete užívat tento lék a pokaždé, když dostanete doplnění. Mohou existovat nové informace.
Tyto informace o pacientech nezabírají místo rozhovoru se svým poskytovatelem zdravotní péče o vašem zdravotním stavu nebo léčbě. Pokud máte dotazy ohledně Esperoctu ® Po přečtení těchto informací se zeptejte svého poskytovatele zdravotní péče.
Jaké jsou nejdůležitější informace, které potřebuji vědět o Esperoctu ® ?
Nepokoušejte se udělat infúzi sami, pokud vás neučí, jak váš poskytovatel zdravotní péče nebo léčebné centrum hemofilie.
Musíte pečlivě dodržovat pokyny poskytovatele zdravotní péče týkající se dávky a harmonogramu pro infuzi espektu ® aby vaše ošetření pro vás bude fungovat nejlépe.
Co je Esperoct ® ?
Espect ® je injekční lék používaný k nahrazení srážení faktoru VIII, který chybí u pacientů s hemofilií A. Hemofilie A je zděděná porucha krvácení ve všech věkových skupinách, která zabraňuje normálnímu srážení krve.
Espect ® se používá k léčbě a prevenci nebo snížení počtu epizod krvácení u lidí s hemofilií A.
je pro vás koloidní stříbro dobré
Váš poskytovatel zdravotní péče vám může poskytnout espekt ® Když máte operaci.
Kdo by neměl používat Esperocta ® ?
Neměli byste používat Espect ® Pokud
- jsou alergičtí na faktor VIII nebo některá z jiných složek Espeltu ®
- Pokud are allergic na hamster proteins
Pokud si nejste si jisti, že se před použitím tohoto léku promluvte se svým poskytovatelem zdravotní péče.
Řekněte svému poskytovateli zdravotní péče, pokud jste těhotná nebo ošetřovatelství, protože espekt ® nemusí být pro vás to pravé.
Co bych měl říct svému poskytovateli zdravotní péče, než použiji Espect ® ?
Pokud jste: měli byste sdělit svému poskytovateli zdravotní péče:
- Mít nebo mít nějaké zdravotní stavy.
- Užívejte jakékoli léky, včetně léčivých přípravků bez předpisu a doplňků stravy.
- Jsou ošetřovatelství.
- Jsou těhotné nebo plánují otěhotnět.
- Bylo řečeno, že máte inhibitory na faktor VIII.
Jak mám použít esperoct ® ?
Léčba Esperoctem ® by měl být zahájen poskytovatelem zdravotní péče, který má zkušenosti s péčí o pacienty s hemofilií A.
Espect ® je dána jako infuze do žíly.
Můžete naplnit Esperocta ® v léčebném centru hemofilie v kanceláři poskytovatele zdravotní péče nebo ve vašem domě. Měli byste být vyškoleni o tom, jak provádět infuze svým centrem pro léčbu hemofilie nebo poskytovatele zdravotní péče. Mnoho lidí s hemofilií a naučí se infuzovat lék sám nebo pomocí člena rodiny.
Váš poskytovatel zdravotní péče vám řekne, kolik Esperoctu ® Chcete -li použít na základě vaší hmotnosti závažnost vaší hemofilie A a kde krvácíte. Vaše dávka bude vypočtena v mezinárodních jednotkách IU.
Pokud vaše krvácení nezastaví po užití Esperoctu, zavolejte svému poskytovateli zdravotní péče ® .
Pokud vaše krvácení není dostatečně kontrolováno, může to být způsobeno vývojem inhibitorů faktoru VIII. To by měl zkontrolovat váš poskytovatel zdravotní péče. Možná budete potřebovat vyšší dávku Esperoctu ® nebo dokonce jiný produkt pro kontrolu krvácení.
Nevytvářejte celkovou dávku Esperoctu ® ovládat své krvácení bez konzultace s poskytovatelem zdravotní péče.
Použití u dětí
Espect ® lze použít u dětí. Váš poskytovatel zdravotní péče rozhodne o dávce Espectu ® obdržíte.
Pokud zapomenete použít Esperocta ®
Pokud zapomenete na dávku, infrujte zmeškanou dávku, když objevíte chybu. Nepodstatněte dvojitou dávku, abyste nahradili zapomenutou dávku. Pokračujte s dalšími infuzemi podle plánu a pokračujte podle doporučení vašeho poskytovatele zdravotní péče.
Pokud přestanete používat Espect ®
Nepřestávejte používat Esperoct ® bez konzultace s poskytovatelem zdravotní péče.
Pokud máte nějaké další dotazy ohledně používání tohoto produktu, zeptejte se svého poskytovatele zdravotní péče.
Co když vezmu příliš mnoho ® ?
Vždy vezměte Espect ® Přesně tak, jak vám řekl váš poskytovatel zdravotní péče. Pokud si nejste jisti, měli byste se zkontrolovat u svého poskytovatele zdravotní péče. Pokud naplníte více Esperově ® než doporučeno, sdělení svého poskytovatele zdravotní péče co nejdříve.
Jaké jsou možné vedlejší účinky Esperoctu ® ?
Mezi běžné vedlejší účinky patří:
- vyrážka or svědění
- Otok bolesti nebo zarudnutí v místě infuze
Můžete mít alergickou reakci na koagulační faktor VIII. Okamžitě zavolejte svému poskytovateli zdravotní péče nebo okamžitě získejte nouzové ošetření, pokud dostanete nějaké známky alergické reakce, jako například: kopřivka těsnost hrudníku síť závrať potíže s dýcháním a/or swelling of the face.
Vaše tělo může také vyrábět protilátky nazývané inhibitory proti Esperoctu ® který může zastavit Espert ® z správné práce. Váš poskytovatel zdravotní péče může čas od času potřebovat testovat vaši krev na inhibitory.
Nejedná se o všechny možné vedlejší účinky Esperoctu ® . Požádejte svého poskytovatele zdravotní péče o další informace. Doporučujeme, abyste nahlásili vedlejší účinky FDA na 1-800-FDA-1088.
Řekněte svému poskytovateli zdravotní péče o jakémkoli vedlejším účinku, který vás vadí nebo který nezmizí.
Co je to Espect ® silné stránky dávkování?
Espect ® Dodává se v pěti různých dávkovacích silách. Skutečný počet mezinárodních jednotek (IU) faktoru VIII v lahvičce bude potištěn na etiketě a na krabici. Pět různých silných stránek je následující:
| Indikátor barev čepice | Nominální síla |
| Červený | 500 IU per vial |
| Zelený | 1000 IU per vial |
| Šedá | 1500 IU per vial |
| Žluť | 2000 IU per vial |
| Černý | 3000 IU per vial |
Vždy zkontrolujte skutečnou dávkovací sílu vytištěnou na štítku, abyste se ujistili, že používáte sílu předepsanou poskytovatelem zdravotní péče.
Jak bych měl ukládat espert ® ?
Před rekonstitucí (míchání suchého prášku v lahvičce s ředidlem):
Chránit před světlem. Nezmrzněte esperokt ® .
Espect ® Lze uložit v chlazení při 36 ° F až 46 ° F (2 ° C až 8 ° C) po dobu až 30 měsíců až do data vypršení platnosti na etiketě. Během 30měsíční životnosti ® může být udržováno při teplotě místnosti (nepřekročit 86 ° F/30 ° C) po dobu až 12 měsíců nebo až 104 ° F (40 ° C) po dobu ne více než 3 měsíců.
Pokud se rozhodnete uložit Espect ® při teplotě místnosti:
- Zaznamenejte datum, kdy byl produkt odstraněn z chladničky.
- Nevracejte produkt do chladničky.
- Nepoužívejte se po 12 měsících, pokud jsou skladovány až 86 ° F (30 ° C) nebo po 3 měsících, pokud jsou skladovány až do 104 ° F (40 ° C) nebo datum vypršení platnosti uvedené na lahvičce, podle toho, co je dříve.
Tento lék nepoužívejte po datu vypršení platnosti, který je na vnějším kartonu a lahvičce. Datum vypršení platnosti se týká posledního dne tohoto měsíce.
Po rekonstituci:
Rekonstituovaný (konečný produkt po smíchání s ředidlem) ® by se měly zdát čisté a bezbarvé bez viditelných částic.
Rekonstituovaný espekt ® by měl být použit okamžitě.
Pokud nemůžete použít rekonstituovaný espekt ® Okamžitě musí být použit do 4 hodin, když je uložen při nebo pod 86 ° C (30 ° C) nebo do 24 hodin, když je skladován v lednici při 36 ° F až 46 ° F (2 ° C až 8 ° C). Uložte rekonstituovaný produkt do lahvičky.
Udržujte tento lék mimo dohled a mimo dosah dětí.
Co jiného bych měl vědět o Esperoctu ® a hemophilia A?
Léky jsou někdy předepsány pro jiné účely, než jsou zde uvedeny. Nepoužívejte Esperoct ® pro podmínku, pro kterou není předepsán. Nesdílejte espekt ® s ostatními lidmi, i když mají stejné příznaky, jaké máte.
Pokyny pro použití
Espect ®
[Antihemofilní faktor (rekombinantní) glykopegylovaný-exei] MixPro ®
Před použitím Esperoctu si tyto pokyny pečlivě přečtěte ® .
Espect ® je dodáván jako prášek. Před infuzí (podáváním) musí být smíchán (rekonstituován) s kapalným ředidlem dodávaným v injekční stříkačce. Kapalný ředidlo je roztok chloridu sodného. Smíšený espekt ® Musí být vloženo do vaší žíly (intravenózní infuze). Zařízení v tomto balíčku je navrženo tak, aby mísilo a infuzilo ® .
Budete také potřebovat infuzní sadu (motýlí jehla s hadičkou) sterilní alkoholové tampony a obvazy.
Nepoužívejte zařízení bez řádného tréninku od svého lékaře nebo zdravotní sestry.
Vždy si umyjte ruce a ujistěte se, že oblast kolem vás bude čistá.
Když připravujete a naplníte léky přímo do žil, je důležité Použijte techniku čisté a aseptické) čisté a bakterie. Nesprávná technika může zavést zárodky, které mohou infikovat krev.
Neotevřete zařízení, dokud nebudete připraveni jej používat.
Nepoužívejte zařízení, pokud bylo zrušeno nebo je poškozeno. Místo toho použijte nový balíček.
Pokud vyprší, nepoužívejte zařízení. Místo toho použijte nový balíček. The expiration date is printed on the outer carnan a on the vial the vial adapter a the pre-filled syringe.
Pokud máte podezření, že je kontaminován, nepoužívejte zařízení. Místo toho použijte nový balíček.
Žádnou z položek se nepokračujte, dokud jste nesmíchali smíšené roztok.
Zařízení je pouze pro jedno použití.
Jednorázová kontejner. Vyhodit nevyužitou část.
Obsah
Balíček obsahuje:
Balík contents
| ® powder - Illustration' src='//pharmacie-hoffer.eu/img/coagulation-factors/92/esperoct-12.webp' > |
- Vial s Esperoctem ® prášek
- Adaptér lahvičky
- Předem naplněná stříkačka s ředidlem
- Prunger Rod (umístěný pod stříkačkou)
Přehled
co se valium používá k léčbě
Nedotýkejte se špičky stříkačky. Pokud se dotknete zárodků stříkaček z prstů.
Pozor: Předem naplněná stříkačka je vyrobena ze skla s vnitřním průměrem špičky 0,037 palce a je kompatibilní se standardním konektorem Luer-block.
Některé bez potřebné konektory pro intravenózní katétry jsou nekompatibilní se skleněnými stříkačkami (například některé konektory s vnitřním hrotem, jako je Clave ® /Mikroklav ® Invision-plus ® Invision- plus CS ® Invision-plus ® Juniorský ® Bietor ® ).
Pro správu Esperoctu ® Prostřednictvím nekompatibilních bezpokojových konektorů odebírá rekonstituovaný produkt do standardní 10 ml sterilní plastové stříkačky Luer-Lock.
Pokud jste se setkali s problémy s připojením předem naplněné stříkačky chloridu sodného k jakémukoli zařízení kompatibilnímu se Luerem-Lock, kontaktujte novo Nordisk na (800) 727-6500.
- Připravte lahvičku a stříkačku
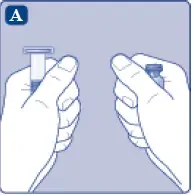
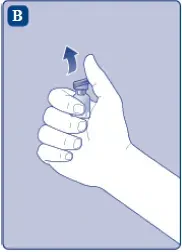
- Vyjměte počet esperotů ® balíčky, které potřebujete.
- Zkontrolujte datum vypršení platnosti.
- Zkontrolujte sílu a barvu názvu balíčku, aby se ujistil, že obsahuje správný produkt.
- Myjte si ruce a dry them properly using a clean nawel or air dry.
- Vyjměte lahvičku adaptér lahvičky a předem naplněnou stříkačku z kartonu. Nechte plunžrovou tyč nedotčenou v kartonu.
- Přineste lahvičku a předem naplněnou stříkačku na teplotu místnosti. Můžete to udělat tak, že je držíte ve svých rukou, dokud se necítí tak teplé jako vaše ruce.
- Odstraňte plastovou čepici z lahvičky. Pokud je plastová čepice volná nebo chybí, nepoužívejte lahvičku.
- Otřete gumovou zátku sterilním alkoholem a allow it na air dry for a few seconds before use na ensure that it is as germ free as possible.
- Nedotýkejte se gumového zátku prsty, protože to může přenášet bakterie.
- Připojte adaptér lahvičky
Nevybraněte adaptér lahvičky z ochranného víčka prsty. Pokud se dotknete špice na adaptérových zárodcích z vašich prstů.
Pokud ochranný papír není plně utěsněn nebo pokud je rozbitý, nepoužívejte adaptér lahvičky.

Jakmile je připojen, neodstraňte adaptér lahvičky z lahvičky.
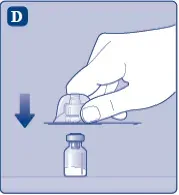
Nezvedněte adaptér lahvičky z lahvičky Při odstraňování ochranné čepice.

- Odstraňte ochranný papír z adaptéru lahvičky.
- Umístěte lahvičku na plochý a pevný povrch.
- Otočte ochrannou čepici a snap the vial adapter onna the Vial.
- Pečlivě odstraňte ochrannou čepici z adaptéru lahvičky.
- Připojte pístvič a stříkačku



- Uchopte plunžrovou tyč u širokého horního konce a vyjměte ji z kartonu. Nedotýkejte se stran nebo vlákna plunžrové tyče. Pokud se dotknete stran nebo zárodečných zárodků z prstů.
- Ihned Připojte plunžrovou tyč k injekční stříkačce tím, že přeměníte ji ve směru hodinových ručiček do gumového pístu uvnitř předem naplněné stříkačky, dokud nebude pociťován odpor.
- Odstraňte stříkačku Z předem naplněné stříkačky ohýbáním ji, dokud se perforace nerozbije. Nedotýkejte se špičky injekční stříkačky pod uzávěrem stříkačky. Pokud se dotknete zárodků stříkaček z prstů. Pokud je stříkačka volná nebo chybí, nepoužívejte předem naplněnou stříkačku.
- Bezpečně zašroubujte předem naplněnou stříkačku na adaptér lahvičky, dokud nebude pociťován odpor.
- Smíchejte prášek s ředidlem

Netřástejte lahvičku, protože to způsobí pěni.
Musí to být jasné a bezbarvé.
Pokud si všimnete viditelných částic nebo zabarvení, nepoužívejte je.
Místo toho použijte nový balíček.

Espect ® se doporučuje použít okamžitě po smíchání.
Pokud nemůžete použít smíšený espekt ® řešení okamžitě musí být použit do 4 hodin, když je skladován při ≤ 86 ° F (30 ° C) nebo do 24 hodin při skladování v lednici při 36 ° F až 46 ° F (2 ° C až 8 ° C). Uložte rekonstituovaný produkt do lahvičky.
Nezmrznejte smíšený espekt ® Řešení nebo jej uložte do stříkaček.
Udržujte rekonstituovaný Espect ® Řešení z přímého světla.
Pokud vaše dávka vyžaduje více než jednu opakovanou lahvičku A na J s dalšími lahvičkami a adaptéry a předem naplněné stříkačky, dokud nedosáhnete požadované dávky.
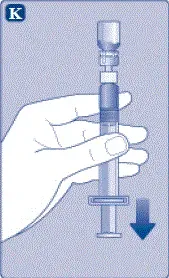
- Držte předem naplněnou stříkačku mírně nakloněnou s lahvičkou směřující dolů.
- Stiskněte tyč písem na inject all the diluent inna the Vial.
- Udržujte prunžrovou tyč stisknutou dolů a víří Lahvička jemně, dokud se veškerý prášek nerozpustí.
- Zkontrolujte smíšený roztok.
- Udržujte plunžrovou tyč úplně zatlačenou dovnitř.
- Otočte stříkačku s lahvičkou vzhůru nohama.
- Přestaňte tlačit plunžrovou tyč a nechte ji přesunout zpět samo o sobě, zatímco smíšený roztok vyplňuje stříkačku.
- Vytáhněte plunžrovou tyč mírně dolů na draw the mixed solution inna the syringe.
- V případě, že potřebujete pouze část celé lahvičky, použijte stupnici na stříkačce, abyste zjistili, kolik smíšeného řešení odstoupíte podle pokynů lékaře nebo zdravotní sestry.
- Zatímco drží lahvičku vzhůru nohama Jemně klepněte na stříkačku na let any air bubbles rise na the nap.
- Stiskněte tyč písem Pomalu, dokud všechny vzduchové bubliny nezmizí.
- Odšroubujte adaptér lahvičky s lahví.
- Naplňte smíšené řešení
Espect ® je nyní připraven vložit do své žíly.
Infuzí roztoku prostřednictvím centrálního přístupového zařízení (CVAD), jako je centrální žilní katétr nebo subkutánní port:
Štítky odlepeného nalezeného na Esperoctu ® Vial lze použít k záznamu čísla šarže.
Likvidace
Nevyhazujte to s obyčejným odpadkem domácnosti.
Před likvidací nerozložte adaptér lahvičky a lahvičky.
Nepoužívejte zařízení znovu.
Důležité informace
Pokud máte nějaké problémy, kontaktujte svého poskytovatele zdravotní péče nebo místní centrum pro léčbu hemofilie.
Úplné informace o předepisování přečtěte si druhou vložku zahrnutý do tohoto balíčku.
- Neměňte esperot ® s jakýmikoli jinými intravenózními infuzemi nebo léky.
- Naplňte smíšené řešení slowly over 1 až 3 minutes as instructed by your docnar or nurse.
- Použijte techniku čisté a aseptické) čisté a bakterie. Po konzultaci s lékařem nebo zdravotní sestrou postupujte podle pokynů pro správné použití pro svůj konektor a centrální přístupové zařízení.
- Infuze do CVAD může vyžadovat použití sterilní 10 ml plastové stříkačky pro stažení smíšeného roztoku a infuze.
- Pokud je to nutné, použijte 0,9% injekce chloridu sodného k propláchnutí linky CVAD před nebo po Esperoctu ® infuze.
- Po infuzi bezpečně zlikvidujte všech nevyužitých esperoktů ® Řešení stříkačky s infuzí Nastaví lahvičku s adaptérem lahvičky a dalšími odpadními materiály do vhodného kontejneru pro odhození lékařského odpadu.











