Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
AminoglykosidyArikayce
Shrnutí drog
Co je Arikayce?
Arikayce (inhalační suspenze liposomu amikacinu) je aminoglykosid Antibakteriální Ukázalo se u dospělých, kteří mají omezené nebo žádné alternativní možnosti léčby pro léčbu plicního onemocnění plic Mycobacterium avium (MAC) jako součást kombinovaného antibakteriálního lékového režimu u pacientů, kteří nedosáhnou negativních kultur sputa po minimálně 6 po sobě jdoucích měsících po dobu více měsíců léčby na pozadí režimu na pozadí. Tento lék je indikován pro použití u omezené a specifické populace pacientů.
Jaké jsou vedlejší účinky Arikayce?
Arikayce
- kopřivka
- potíže s dýcháním
- Otok vašeho obličeje rty jazyk nebo krk
- kašel (zejména během prvního měsíce používání léku)
- potíže s mluvením
- Zvoní v uších
- Změny ve sluchu
- závrať
- pocity točení
- Lightheadedness
- těsnost hrudníku
- síť
- dušnost
- kašel o krev
- malé nebo žádné močení
- otok nohou nebo kotníků a
- únava
Získejte lékařskou pomoc okamžitě, pokud máte výše uvedené příznaky.
Mezi běžné vedlejší účinky Arikayce patří:
- potíže s mluvením
- kašel
- Bronchospasmus
- kašel o krev
- poškození vnitřního ucha
- Podráždění horních cest dýchacích
- Muskuloskeletální bolest
- únava
- slabost
- Zhoršení základního onemocnění plic
- průjem a
- nevolnost
Pokud máte následující vážné vedlejší účinky, vyhledejte lékařskou péči nebo zavolejte na číslo 911:
- Vážné příznaky očí, jako je ztráta náhlého vidění rozmazané vidění vidění Vision Vision Eye Eye Eye Eye Eye Eye Eye Eye nebo vidět halos kolem světel;
- Vážné příznaky srdce, jako je rychlé nepravidelné nebo bušení srdečního rytmu; třepování v hrudi; dušnost; a náhlé závratě lightheadness nebo omdlení;
- Těžká zmatek bolesti hlavy zkažená paže řeči nebo slabost nohou Potíže se ztrátou chůze pocitu koordinace Nestabilní velmi tuhé svaly vysoké horečky bohaté pocení nebo třes.
Tento dokument neobsahuje všechny možné vedlejší účinky a mohou dojít k jiným. Další informace o vedlejších účincích najdete u svého lékaře.
Dávkování pro Arikayce
Doporučená dávka Arikayce u dospělých je kdysi denně orální inhalace obsahu jedné 590 mg/8,4 ml arikayce lahvičky. Používejte Arikayce Vials pouze se systémem Nebulizer Lamira.
Jaké léky nebo doplňky interagují s Arikayce?
Arikayce může interagovat s furosemidem kyseliny ethakrynové močovina Intravenózní mannitol nebo léky spojené s neurotoxicitou nefrotoxicitou a ototoxicitou. Řekněte svému lékaři všechny léky a doplňky, které používáte.
Arikayce během těhotenství nebo kojení
Řekněte svému lékaři, pokud jste těhotná nebo plánujete otěhotnět před použitím Arikayce; Může to poškodit plod. Není známo, zda Arikayce přejde do mateřského mléka. Před kojením se poraďte se svým lékařem.
Další informace
Naše Arikayce (inhalační suspenze liposomů amikacinu) pro orální inhalační účinky Vedlejší účinky drogové centrum poskytuje komplexní pohled na dostupné informace o možných vedlejších účincích při užívání tohoto léku.
Informace o drogách FDA
- Popis léku
- Indikace
- Dávkování
- Vedlejší účinky
- Varování
- Předávkovat
- Klinická farmakologie
- Průvodce léky
VAROVÁNÍ
Riziko zvýšených respiračních nežádoucích účinků
Arikayce byla spojena se zvýšeným rizikem respiračních nežádoucích účinků, včetně přecitlivělosti pneumonitis hemoptysis bronchospasm exacerbace základní plicní onemocnění, které v některých případech vedlo k hospitalizaci [viz viz hospitalizace VAROVÁNÍS AND OPATŘENÍ ].
Popis pro Arikayce
Účinnou složkou v Arikayce (inhalační suspenze liposomu amikacinu) je amikacin sulfát USP aminoglykosidové antibakteriální. Jeho chemický název je d-streptamin O -3-amino-3-deoxy-a-dglukopyranosyl- (1 → 6)- O -[6-amino-6-deoxy-a-d-glukopyranosyl- (1 → 4)]- N 1 -(4-amino-2-hydroxy-1oxobutyl) -2-deoxy- ( S )- síran (1: 2) Sůl s chemickým vzorcem C 22 H 43 N 5 O 13 • 2H 2 TAK 4 s molekulovou hmotností 781,76. Jeho strukturální vzorec je:
 |
Arikayce je bílá mléčná suspenze sestávající z amikacinu sulfátu zapouzdřeného v liposomech a je dodávána v jednotce 10 ml jasné skleněné lahvičky obsahující amikacin 590 mg/8,4 ml (ekvivalent amikacinu sulfátu 623 mg/8,4 ml) jako sterilní vodní liposomální suspenzion. Arikayce se skládá z amikacinu sulfátu zapouzdřeného v liposomech v cílené koncentraci 70 mg amikacinu/ml s rozmezí pH 6,1 až 7,1 a poměru hmotnosti lipidu k amikacinu v rozmezí 0,60 až 0,79. Neaktivní složky jsou cholesterol dipalmitoylfosfatidylcholin (DPPC) hydroxid sodný sodný sodný (pro nastavení pH) a vodu pro injekci.
Arikayce je spravován pouze pomocí systému Nebulizer Lamira [viz Dávkování a podávání ]. Like all other nebulized treatments the amount delivered to the lungs will depend upon patient factnebos. Under staardized in vitro Testování na USP <1601> Vzorec dechového dýchání (500 ml přílivového objemu 15 dechů za minutu a inhalaci: poměr vydechování 1: 1) Průměrná dodaná dávka z náustku byla přibližně 312 mg sulfátu amikacinu (53% nároku na štítky). Hmotný mediánský aerodynamický průměr (MMAD) nebulizovaných aerosolových kapiček je asi 4,7 μm (NULL,1 - 5,3 μm), jak bylo stanoveno pomocí metody Impactrow (NGI) příští generace. Procento amikacinu v liposomu je uvolněno procesem nebulizace, takže nebulizovaný Arikayce poskytuje kombinaci volného a liposomálního amikacinu.
Použití pro Arikayce
Omezená populace: Arikayce ® je indikováno u dospělých, kteří mají omezené nebo žádné alternativní možnosti léčby pro léčbu Mycobacterium avium Komplexní (MAC) plicní onemocnění jako součást kombinovaného antibakteriálního lékového režimu u pacientů, kteří nedosáhnou negativních kultur sputa po minimálně 6 po sobě jdoucích měsících léčby na podklady na pozadí více léků. Vzhledem k tomu, že pouze omezené údaje o klinické bezpečnosti a účinnosti pro Arikayce jsou v současné době k dispozici rezervní arikayce pro použití u dospělých, kteří mají omezené nebo žádné alternativní možnosti léčby. Tento lék je indikován pro použití u omezené a specifické populace pacientů.
Tato indikace je schválena na základě zrychleného schválení na základě dosažení přeměny kultury sputum (definované jako 3 po sobě jdoucí negativní měsíční kultury sputa) do 6. měsíce. Klinický přínos dosud nebyl stanoven [viz viz Klinické studie ]. Continued approval fnebo this indication may be contingent upon verification a description of clinical benefit in confirmatneboy trials.
Omezení použití
Arikayce byla studována pouze u pacientů s refrakterním onemocněním MAC plic definovaných jako pacienti, kteří nedosáhli negativních kultur sputa po minimálně 6 po sobě jdoucích měsících léčby na podklady na pozadí. Použití Arikayce se nedoporučuje u pacientů s nerefrakční onemocnění MAC plic.
Dávkování pro Arikayce
Důležité pokyny pro správu
Arikayce je pouze pro ústní inhalaci. Spravujte nebulizací pouze s Lamira ® Nebulizer System. Informace o použití Arikayce naleznete v pokynech pro použití v systému Arikayce se systémem Nebulizer Lamira.
Pokyn pacientům používajícím bronchodilatátor („reliever“), aby nejprve používali bronchodilatátor podle bronchodilatorového letáku pro použití informací před použitím Arikayce.
U pacientů se známým hyperreaktivním onemocněním dýchacích cest by mělo být zváženo předběžné ošetření s krátkodobými selektivními agonisty beta-2 chronické obstrukční plicní onemocnění nebo bronchospasmus [viz viz VAROVÁNÍS AND OPATŘENÍ ].
Doporučené dávkování
Doporučenou dávkování Arikayce u dospělých je kdysi denní inhalace obsahu jednoho 590 mg/8,4 ml arikayce lahvičky (590 mg Amikacinu) pomocí systému Nebulizer Lamira [viz viz [viz lamira. Klinické studie ].
Spravujte Arikayce pouze se systémem Nebulizer Lamira. Arikayce by měla být před použitím na teplotě místnosti. Před otevřením Shake Arikayce Vial Well po dobu nejméně 10 až 15 sekund, dokud se obsah neobjeví rovnoměrně a dobře smíšený. Vial Arikayce je otevřen převrácením plastové horní části lahvičky a poté, co se zvedl dolů, aby uvolnil kovový kroužek. Kovový kroužek a gumová zátka by měla být opatrně odstraněna. Obsah lahvičky Arikayce pak může být naliu do medikační rezervoáru sluchátka nebulizéru.
Pokud je denní dávka Arikayce vynechána, spravujte další dávku další den. Neozvete dávku, abyste nahradili promarněnou dávku.
Jak dodáno
Dávkování Fneboms And Strengths
Arikayce je dodáván jako sterilní bílá mléčná vodná suspenze liposomu pro perorální inhalaci ve skleněné lahvičce s jednotkou obsahující amikacin 590 mg/8,4 ml (ekvivalent amikacinu sulfátu 623 mg/8,4 ml).
Arikayce (Inhalační suspenze liposomu amikacinu) 590 mg/8,4 ml je dodávána ve sterilní 10 ml skleněné lahvičce. Produkt je vydán jako 28-viační sada.
Každý karton obsahuje 28denní zásobu léků (28 lahviček). Kromě lahviček Arikayce v kartonu jsou poskytnuty sluchátko Lamira Nebulizer a čtyři aerosolové hlavy Lamira.
NDC 71558-590-28
Systém Nebulizer Lamira obsahuje ovladač náhradní aerosol hlavu náhradního telefonu a příslušenství.
Skladování a manipulace
Uložte lahvičky Arikayce chlazené při 2 ° C až 8 ° C (36 ° F až 46 ° F) až do data vypršení platnosti na lahvičku. Ne zmrazení . Jakmile vypršela vypršela jakýkoli nevyužitý lék.
Arikayce can be stneboed at room temperature up to 25°C (77°F) fnebo up to 4 weeks. Once at room temperature any unused drug must be discarded at the end of 4 weeks.
Vyrobeno pro: InSmed Incorporated 700 US Highway 202/206 Bridgewater NJ 08807-1704. Revidováno: 2023
Vedlejší účinky pro Arikayce
Následující klinicky významné nežádoucí účinky jsou podrobněji popsány v jiných částech označování:
- Pneumonitida hypersenzitivity [viz Varování a VAROVÁNÍS AND OPATŘENÍ ]
- Hemoptysis [viz Varování a VAROVÁNÍS AND OPATŘENÍ ]
- Bronchospasm [viz Varování a VAROVÁNÍS AND OPATŘENÍ ]
- Exacerbace základní plicní onemocnění [viz Varování a VAROVÁNÍS AND OPATŘENÍ ]
- Anafylaxe a hypersenzitivní reakce [viz VAROVÁNÍS AND OPATŘENÍ ]
- Ototoxicita [viz VAROVÁNÍS AND OPATŘENÍ ]
- Nefrotoxicita [viz VAROVÁNÍS AND OPATŘENÍ ]
- Neuromuskulární blokáda [viz VAROVÁNÍS AND OPATŘENÍ ]
Zkušenosti z klinických studií
Protože klinické studie se provádějí za široce proměnlivých podmínek, nežádoucí rychlosti nežádoucí reakce pozorované v klinických studiích léčiva nelze přímo porovnat s mírami v klinických studiích s jiným lékem a nemusí odrážet míru pozorované v praxi.
Přehled klinických hodnocení pro hodnocení bezpečnosti
V rámci refrakterního klinického programu NTM 404 pacientů, kteří se účastnili tří klinických studií, byli léčeni Arikayce v dávce 590 mg/den (střední doba expozice Arikayce byla 236,5 dne).
Zkouška 1 (NCT Mycobacterium avium Komplexní (MAC) plicní onemocnění. Pacienti byli randomizováni buď na 8 měsíců Arikayce plus režim pozadí (n = 223) nebo samotný režim pozadí (n = 112).
Zkouška 2 (NCT
Zkouška 3 (NCT Mycobacterium . Pacienti byli randomizováni buď na režim Arikayce Plus na pozadí (n = 44), nebo na inhalované zředěné prázdné liposomové placebo plus režim pozadí (n = 45) po dobu 84 dnů.
Ve všech klinických studiích u pacientů s refrakterní NTM plicní infekcí a bez ní bylo vystaveno více dávkám Arikayce.
Nežádoucí účinky vedoucí k přerušení léčby
Ve třech studiích NTM došlo k vyššímu výskytu předčasného přerušení Arikayce. Ve studii 1 34,5% předčasně přerušilo Arikayce; Většina z nich byla způsobena nežádoucími reakcemi (NULL,8%) a stažením podle subjektu (NULL,9%). V rameni komparátoru 10,7% subjektů přerušilo svůj režim pozadí s 0,9% v důsledku nežádoucích účinků a 5,4% v důsledku stažení subjektem. Ve studii 2 (prodloužení pokusu 1) 37,8% pacientů začínajících na Arikayce předčasně přerušilo 24,4% přerušení v důsledku nežádoucích účinků. Ve studii 3 Všech 9 (NULL,5%) předčasných diskontinuace došlo u pacientů ošetřených režimem Arikayce Plus na pozadí a v rameni placeba plus neexistovaly žádné předčasné přerušení.
Vážné nežádoucí účinky v pokusech 1 a 3
Ve studii 1 19,7% pacientů léčených režimem Arikayce Plus uvedlo SAR ve srovnání se 16,1% pacientů léčených samotným režimem pozadí. Kromě toho ve studii 1 [2 až 1 randomizace Arikayce plus režim pozadí versus samotný režim pozadí] bylo u 41 pacientů (NULL,4%) léčeno 80 hospitalizací léčených samotným režimem pozadí. Nejběžnější SARS a důvody hospitalizace v rameni Arikayce Plus na pozadí byly spojeny s exacerbací základní plicní onemocnění a infekcí dolních dýchacích cest, jako je pneumonie. Ve studii 3 18,2% pacientů léčených režimem Arikayce Plus uvedlo SARS ve srovnání s 8,9% pacientů léčených režimem na pozadí plus inhalační placebem.
Běžné nežádoucí účinky
Incidence nežádoucích účinků ve studii 1 jsou zobrazeny v tabulce 1. Jsou zobrazeny pouze ty nežádoucí účinky s rychlostí alespoň 5% ve skupině Arikayce Plus a větší než skupina samotného režimu pozadí.
Tabulka 1: Nežádoucí účinky u ≥ 5% pacientů s MAC ošetřenými Arikayce a častější než režim pozadí v pokusu 1
| Nežádoucí reakce | Arikayce plus Background Regimen (N = 223) n (%) | Samotný režim pozadí (N = 112) n (%) |
| Dysfonie a | 106 (48) | 2 (2) |
| Kašel b | 88 (40) | 19 (17) |
| Bronchospasmus c | 64 (29) | 12 (11) |
| Hemoptysis | 41 (18) | 15 (13) |
| Muskuloskeletální bolest d | 40 (18) | 10 (9) |
| Podráždění horních cest dýchacích e | 39 (18) | 2 (2) |
| Elitudeicity f | 38 (17) | 11 (10) |
| Únava a astenia | 36 (16) | 11 (10) |
| Exacerbace základního plicního onemocnění g | 34 (15) | 11 (10) |
| Průjem | 28 (13) | 5 (5) |
| Nevolnost | 26 (12) | 4 (4) |
| Bolest hlavy | 22 (10) | 5 (5) |
| Zápal plic h | 20 (9) | 10 (9) |
| Pyrexia | 17 (8) | 5 (5) |
| Hmotnost se snížila | 16 (7) | 1 (1) |
| Zvracení i | 15 (7) | 4 (4) |
| Vyrážka j | 14 (6) | 1 (1) |
| Změna ve sputu k | 13 (6) | 1 (1) |
| Nepohodlí na hrudi | 12 (5) | 3 (3) |
| a Zahrnuje afonii a dysfonii b Zahrnuje produktivní kašel a syndrom kašle horních dýchacích cest c Zahrnuje astma bronchiální hyperreaktivita Bronchospasm Dyspnea Dyspnoea Zplňování prodlouženého expirace těsnosti krku a sípání d Zahrnuje bolest zad Artralgie Myalgia bolest/tělo bolesti svalu a bolesti muskuloskeletální e Zahrnuje orofaryngeální bolest orofaryngeální nepohodlí podráždění krku hltan erytém zánět dýchacích cest hltan edém zánět zánět hrtanů f Zahrnuje hluchotu hluchoty Neurosenzorická hluchota jednostranná závratě Hypoacusis Presyncope Tinnitus Vertigo Balance Poruchy g Zahrnuje CHOPN infekční exacerbaci CHOPN infekční exacerbace bronchiektasis h Zahrnuje atypickou infekci pneumonia empyém Pleural Effusion Dolní respirační cesty Infekce plicní infekce plicní infekce pseudomonas pneumonia pneumonia aspirace pneumonia pseudomonas infekce a respirační trakt infekce i Zahrnuje zvracení a post-tusivní zvracení j Zahrnuje vyrážku makulo-papulární erupce drog a kopce k Zahrnuje zvýšené hnisy sputum a sputum zbarvené |
Vybrané nepříznivé reakce léčiva, ve kterých došlo <5% of patients a at higher frequency in Arikayce-treated patients in Trial 1 are presented in Table 2.
Tabulka 2: Vybrané nežádoucí účinky <5% of Arikayce-treated MAC Patients a Mneboe Frequent than Samotný režim pozadí in Trial 1
| Nežádoucí reakce | Arikayce plus Background Regimen N = 223 n (%) | Samotný režim pozadí N = 112 n (%) |
| Úzkost a | 10 (5) | 0 (0) |
| Orální plísňová infekce b | 9 (4) | 2 (2) |
| Bronchitida | 8 (4) | 3 (3) |
| Dysgeusia | 7 (3) | 0 (0) |
| Hypersenzitivita pneumonitida c | 7 (3) | 0 (0) |
| Sucho v ústech | 6 (3) | 0 (0) |
| Epistaxis | 6 (3) | 1 (1) |
| Respirační selhání d | 6 (3) | 2 (2) |
| Pneumothorax e | 5 (2) | 1 (1) |
| Tolerance cvičení se snížila | 3 (1) | 0 (0) |
| Porucha rovnováhy | 3 (1) | 0 (0) |
| Neuromuskulární porucha f | 2 (1) | 0 (0) |
| a Zahrnuje úzkostnou a úzkostnou poruchu b Zahrnuje ústní kandidózu a infekci ústních plísňů c Zahrnuje alergickou alveolitidu Intersticiální onemocnění plic a pneumonitidu d Zahrnuje akutní respirační selhání a respirační selhání e Zahrnuje pneumotorax pneumotorax spontánní a pneumomediastinum f Zahrnuje svalovou slabost a periferní neuropatii |
Incidence hypersenzitivity pneumonitida bronchospasm Bronchospasm Dysfonia Dysfonia prohlubující základní onemocnění hemoptysis Ototoxicita Horní podráždění dýchacích a neuromuskulárních poruch viz tabulka 1 a tabulka 2. VAROVÁNÍS AND OPATŘENÍ ].
Zážitek z postmarketingu
Následující nežádoucí účinky byly identifikovány z postmarketingového dohledu. Protože tyto nežádoucí účinky jsou hlášeny dobrovolně z populace neznámé velikosti přesné odhady frekvence nelze provést a nelze provést kauzální vztah k expozici léčiva.
Poruchy imunitního systému: Anafylaxe hypersenzitivity [viz VAROVÁNÍS AND OPATŘENÍ ]
Interakce drog pro Arikayce
Léky s neurotoxickým nefrotoxickým nebo ototoxickým potenciálem
Vyvarujte se souběžného použití Arikayce s léky spojenými s neurotoxicitou nefrotoxicitou a ototoxicitou.
Ethyrynová kyselina furosemid močovina nebo mannitol
Některá diuretika mohou zvýšit toxicitu aminoglykosidu změnou koncentrací aminoglykosidu v séru a tkáni. Vyhněte se souběžnému použití arikayce s ethacrynovou kyselinou furosemid močovina nebo intravenózní mannitol.
Varování pro Arikayce
Zahrnuto jako součást 'OPATŘENÍ' Sekce
Opatření pro Arikayce
Hypersenzitivita pneumonitida
Hypersenzitivita pneumonitida has been repneboted with the use of Arikayce in the clinical trials. Hypersenzitivita pneumonitida (repneboted as allergic alveolitis pneumonitis interstitial lung disease allergic reaction to Arikayce) was repneboted at a higher frequency in patients treated with Arikayce plus a background regimen (3.1%) compared to patients treated with a background regimen alone (0%). Most patients with hypersensitivity pneumonitis discontinued treatment with Arikayce a received treatment with cneboticosteroids [see Nežádoucí účinky ]. If hypersensitivity pneumonitis occurs discontinue Arikayce a manage the patient as medically appropriate.
Hemoptysis
Hemoptysis has been repneboted with the use of Arikayce in the clinical trials. Hemoptysis was repneboted at a higher frequency in patients treated with Arikayce plus a background regimen (18.4%) compared to patients treated with a background regimen alone (13.4%) [see Nežádoucí účinky ]. If hemoptysis occurs manage the patients as medically appropriate.
Bronchospasmus
Bronchospasmus has been repneboted with the use of Arikayce in the clinical trials. Bronchospasmus (repneboted as asthma bronchial hyperreactivity Bronchospasmus dyspnea dyspnea exertional prolonged expiration throat tightness síť) was repneboted at a higher frequency in patients treated with Arikayce plus a background regimen (28.7%) compared to patients treated with a background regimen alone (10.7%) [see Nežádoucí účinky ]. If Bronchospasmus occurs during the use of Arikayce treat the patients as medically appropriate.
Exacerbace základního plicního onemocnění
Byly hlášeny exacerbace základního plicního onemocnění s použitím Arikayce v klinických studiích. Exacerbace základního plicního onemocnění (uváděná jako chronická obstrukční plicní onemocnění infekční exacerbace chronického obstrukčního plicního onemocnění infekční exacerbace bronchiektázy) byla hlášena při vyšší frekvenci u pacientů léčených Arikayce plus režimem na pozadí (15.2%) ve srovnání s pacienty (NULL,8%) [9,8%) [9,8%) [9,8%) Nežádoucí účinky ]. If exacerbations of underlying pulmonary disease occur during the use of Arikayce treat the patients as medically appropriate.
Anafylaxe a hypersenzitivní reakce
U pacientů užívajících Arikayce byly hlášeny závažné a potenciálně život ohrožující hypersenzitivní reakce včetně anafylaxe. Signs and symptoms include acute onset of skin and mucosal tissue hypersensitivity reactions (hives itching flushing swollen lips/tongue/uvula) respiratory difficulty (shortness of breath wheezing stridor cough) gastrointestinal symptoms (nausea vomiting diarrhea crampy abdominal pain) and cardiovascular signs and symptoms of anaphylaxis (tachycardia nízký krevní tlak Syncope inkontinence závratě). Před zavedením terapie Arikayce vyhodnotí předchozí hypersenzitivní reakce na aminoglykosidy. Pokud dojde k anafylaxi nebo reakce přecitlivělosti, ukončí Arikayce a zavede vhodná podpůrná opatření.
Elitudeicity
Elitudeicity With Use Of Arikayce
Elitudeicity has been repneboted with the use of Arikayce in the clinical trials. Elitudeicity (including deafness závrať presyncope tinnitus a vertigo) were repneboted with a higher frequency in patients treated with Arikayce plus a background regimen (17%) compared to patients treated with background regimen alone (9.8%). This was primarily driven by tinnitus (8.1% in Arikayce plus background regimen vs. 0.9% in the background regimen alone arm) a závrať (6.3% in Arikayce plus background regimen vs. 2.7% in the background regimen alone arm) [see Nežádoucí účinky ].
Během léčby Arikayce pečlivě monitorujte pacienty se známou nebo podezření na zvukovou nebo vestibulární dysfunkci. Pokud dojde k ototoxicitě, spravuje pacienta jako lékařsky vhodný, včetně potenciálně přerušení Arikayce.
Riziko ototoxicity v důsledku variant mitochondriálních DNA
U pacientů s určitými varianty v mitochondriálně kódovaném 12S rRNA genu (MT-RNR1) byly pozorovány případy ototoxicity s aminoglykosidy, zejména zejména variantou M.1555A> G. U některých pacientů došlo k ototoxicitě, i když jejich hladiny aminoglykosidového séra byly v doporučeném rozmezí. Varianty mitochondriálních DNA jsou přítomny u méně než 1% obecné populace v USA a podílu variantních nosičů, kteří mohou vyvinout ototoxicitu a závažnost ototoxicity, není známa. V případě známé mateřské anamnézy ototoxicity v důsledku užívání aminoglykosidů nebo známé varianty mitochondriální DNA u pacienta zvažte alternativní léčbu jinou než aminoglykosidy, ledaže by zvýšené riziko trvalé ztráty sluchu nevyváženo závažností infekce a nedostatkem bezpečných a účinných alternativních terapií.
Nefrotoxicita
Nefrotoxicita was observed during the clinical trials of Arikayce in patients with MAC lung disease but not at a higher frequency than the background regimen alone [see Nežádoucí účinky ]. Nefrotoxicita has been associated with the aminoglycosides. Close monitneboing of patients with known nebo suspected renal dysfunction may be needed when prescribing Arikayce.
Neuromuskulární blokáda
Pacienti s neuromuskulárními poruchami nebyli zapsáni do klinických studií Arikayce. Aminoglykosidy mohou zhoršit svalovou slabost blokováním uvolňování acetylcholinu při neuromuskulárních křižovatkách. Pečlivě sledujte pacienty se známými nebo podezřeními na neuromuskulární poruchy, jako je myasthenia gravis. Pokud dojde k neuromuskulární blokádě, může být zvrácena podáváním soli vápenatých, ale může být nutná mechanická respirační pomoc.
Toxicita embryo-fetální
Aminoglykosidy mohou při podávání těhotné ženy způsobit poškození plodu. Aminoglykosidy včetně Arikayce mohou být spojeny s celkovou nevratnou bilaterální vrozenou hluchotou u dětských pacientů v děloze . Pacienti, kteří používají Arikayce během těhotenství nebo otěhotní při užívání Arikayce Použití v konkrétních populacích ].
Informace o poradenství pro pacienta
Doporučujte pacientovi, aby si přečetl značení pacienta schváleného FDA ( Průvodce léky a Patient Instructions fnebo Use ).
Důležité pokyny pro správu Arikayce
Před zahájením Arikayce instrujte pacienty, aby si přečetli pokyny pro použití. Pokyn pacientům, aby používali pouze lamira ® Nebulizer System pro správu Arikayce. Doporučujte pacientovi nebo pečovateli, aby nepoužíval systém Nebulizer Lamira s žádným jiným lékem.
Hypersenzitivita pneumonitida And Bronchospasmus (Difficulty Breathing)
Poraďte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud po podání Arikayce zažijí dušnost nebo sípání. Poraďte pacientům s anamnézou reaktivního astmatu nebo bronchospasmu onemocnění dýchacích cest, aby podávali Arikayce po použití krátkodobého bronchodilatoru [viz viz VAROVÁNÍS AND OPATŘENÍ ].
Hemoptysis Or Kašel
Poraďte pacientům, aby informovali svého poskytovatele zdravotní péče, zda vykašlávají krev nebo zažijí epizodický kašel buď během nebo po Arikayce Administration, zejména v prvním měsíci po zahájení Arikayce [viz viz VAROVÁNÍS AND OPATŘENÍ a Nežádoucí účinky ].
Exacerbace základního plicního onemocnění
Poraďte pacientům, aby informovali o svém poskytovateli zdravotní péče, pokud po spuštění Arikayce zažijí zhoršení plicní choroby [viz VAROVÁNÍS AND OPATŘENÍ ].
Dysfonie Or Difficulty Speaking
Doporučujte pacientům, aby informovali svého poskytovatele zdravotní péče, pokud mají potíže s mluvením. S Arikayce byla hlášena potíže s mluvením nebo ztrátou schopnosti mluvit [viz Nežádoucí účinky ].
Anafylaxe a hypersenzitivní reakce
Poraďte pacientům a pečovatelům, že by mohly nastat vážné a potenciálně život ohrožující reakce hypersenzitivity, které vyžadují okamžitou léčbu. Doporučujte pacientovi, aby přerušil Arikayce a hledal okamžitou lékařskou pomoc, pokud dojde k nějakému příznakům nebo příznakům reakce přecitlivělosti [Viz [Viz VAROVÁNÍS AND OPATŘENÍ ].
Elitudeicity (Ringing In The Ears)
Poraďte pacientům, aby informovali o poskytovateli zdravotní péče, zda zažívají vyzvánění v uších závratě nebo jakékoli změny ve slyšení, protože Arikayce byla spojena se ztrátou sluchu [Viz VAROVÁNÍS AND OPATŘENÍ ].
Doporučujte pacientovi, aby neprovozoval těžké stroje nebo nečinil nebezpečné aktivity při vdechování Arikayce prostřednictvím systému Nebulizéra Lamira, protože Arikayce může způsobit příznaky, jako je závratě nebo respirační příznaky.
Nefrotoxicita Or Kidney Damage
Doporučujte pacientům informovat svého poskytovatele zdravotní péče, pokud mají problémy s ledvinami, protože bylo hlášeno poškození ledvin u aminoglykosidů [Viz VAROVÁNÍS AND OPATŘENÍ ]. Neuromuskulární blokáda Advise patients to infnebom their healthcare provider of known neuromuscular disease (e.g. myasthenia gravis) [see VAROVÁNÍS AND OPATŘENÍ ].
Toxicita embryo-fetální
Poraďte těhotné ženy, že aminoglykosidy včetně Arikayce mohou při podání během těhotenství způsobit nevratnou vrozenou hluchotu [viz viz VAROVÁNÍS AND OPATŘENÍ a Použití v konkrétních populacích ].
Neklinická toxikologie
Zhodnocení mutageneze karcinogeneze plodnosti
Ve dvouleté inhalační studii karcinogenity byly krysy vystaveny Arikayce po dobu 15-25-70 nebo 155170 minut denně po dobu 96-104 týdnů. Ty poskytly přibližné inhalační dávky 5 15 a 45 mg/kg/den. Karcinom skvamózních buněk byl pozorován v plicích 2 ze 120 potkanů podávaných nejvyšší testované dávce. Maximální hladiny AUC v séru amikacinu u potkanů v ustáleném stavu byly přibližně 1,3 2,8 a 7,6 mcg · h/ml při nízkých středních a vysokých dávkách ve srovnání s 23,5 mcg · h/ml (NULL,0 až 46,5 mcg/hr/ml) měřených u lidí. Karcinomy spinocelulárních buněk mohou být výsledkem vysoké plicní zátěže částic z Arikayce v plicích potkana. Relevance nálezů nádoru plic s ohledem na lidi, kteří přijímají Arikayce, není znám.
V baterii nebyly pozorovány žádné důkazy o mutagenicitě nebo genotoxicitě in vitro a nadarmo Studie genotoxicity s formulací amikacinu s liposomem podobnou Arikayce ( in vitro Test mikrobiální mutageneze in vitro Test mutace myšího lymfomu in vitro studie chromozomální aberace a nadarmo mikronukleusová studie u potkanů).
S Arikayce nebyly provedeny žádné studie plodnosti. Intraperitoneální podávání amikacinu na samce a samice potkanů v dávkách až 200 mg/kg/den před pářením 7. dne těhotenství nebylo spojeno s poškozením plodnosti nebo nežádoucích účinků na časný embryonální vývoj.
Použití v konkrétních populacích
Těhotenství
Shrnutí rizika
U těhotných žen neexistují žádné údaje o používání Arikayce k hodnocení jakéhokoli rizika asociovaného s drogami při potratu v narození nebo nepříznivých výsledků matek nebo plodu. Ačkoli se očekává, že systémová absorpce amikacinu po orální inhalaci bude nízká [viz Klinická farmakologie ] Systémová expozice aminoglykosidovým antibakteriálním lékům včetně Arikayce může být spojena s úplnou nevratnou bilaterální vrozenou hluchotou při podávání těhotným ženám [viz viz VAROVÁNÍS AND OPATŘENÍ ]. Advise pregnant women of the potential risk to a fetus.
Studie reprodukční toxikologie zvířat nebyly provedeny s inhalovaným amikacinem. Subkutánní podávání amikacinu na těhotné potkany (až 100 mg/kg/den) a myší (až 400 mg/kg/den) během organogeneze nebylo spojeno s malformacemi plodu. Ototoxicita nebyla ve studiích na zvířatech adekvátně hodnocena u potomků.
Odhadované riziko pozadí hlavních vrozených vad a potratu pro uvedené populace není známo. Všechna těhotenství mají na pozadí riziko ztráty vrozených vad nebo jiných nepříznivých výsledků. V americké obecné populaci je odhadované riziko na pozadí hlavních vrozených vad a potratu u klinicky uznávaných těhotenství 2-4% a 15–20%.
Data
Údaje o zvířatech
Nebyly provedeny žádné studie reprodukční toxikologie zvířat s Arikayce nebo neliposomálním amikacinem podávaným inhalací.
Amikacin byl subkutánně podáván těhotným potkanům (těhotenství 8-14) a myši (gestační dny 7-13) v dávkách 25 100 nebo 400 mg/kg pro posouzení vývojové toxicity. Tyto dávky nezpůsobily fetální viscerální nebo kosterní malformace u myší. Vysoká dávka byla příliš mateřská toxická u potkanů (byla pozorována nefrotoxicita a úmrtnost), která vylučovala hodnocení potomků v této dávce. Malformace plodu nebyly pozorovány při nízké nebo střední dávce u potkanů. Postnatální vývoj potkanů a myší vystavených těmto dávkám amikacinu v děloze se významně nelišil od kontroly.
Elitudeicity was not adequately evaluated in offspring in animal developmental toxicology studies.
Laktace
Shrnutí rizika
Neexistují žádné informace týkající se přítomnosti Arikayce v lidském mléce Účinky na kojené dítě nebo účinky na produkci mléka po podání Arikayce inhalací. Ačkoli omezené publikované údaje o jiných trasách podávání amikacinu naznačují, že amikacin je přítomen v systémové absorpci lidského mléka Arikayce po inhalačním podání se očekává, že bude nízká [viz viz Klinická farmakologie ]. The developmental a health benefits of breastfeeding should be considered along with the mother’s clinical need fnebo Arikayce a any potential adverse effects on the breastfed child from Arikayce nebo from the underlying maternal condition.
Dětské použití
Bezpečnost a účinnost Arikayce u pediatrických pacientů mladších 18 let nebyla stanovena.
Geriatrické použití
V klinických studiích NTM o celkovém počtu pacientů, kteří dostávali Arikayce 208 (NULL,5%), bylo ≥ 65 let a 59 (NULL,6%) bylo ≥ 75 let. Nebyly pozorovány žádné celkové rozdíly v bezpečnosti a účinnosti mezi staršími subjekty a mladšími subjekty. Protože starší pacienti mají větší pravděpodobnost snížení funkce ledvin, může být užitečné sledovat funkci ledvin [viz VAROVÁNÍS AND OPATŘENÍ ].
Poškození jater
Arikayce has not been studied in patients with hepatic impairment. No dose adjustments based on hepatic impairment are required since amikacin is not hepatically metabolized [see Klinická farmakologie ].
Dlouhodobé vedlejší účinky Percocet
Poškození ledvin
Arikayce has not been studied in patients with renal impairment. Given the low systemic exposure to amikacin following administration of Arikayce clinically relevant accumulation of amikacin is unlikely to occur in patients with renal impairment. However renal function should be monitneboed in patients with known nebo suspected renal impairment including elderly patients with potential age-related decreases in renal function [see VAROVÁNÍS AND OPATŘENÍ Geriatrické použití ].
Informace o předávkování Arikayce
Nepříznivé účinky specificky spojené s předávkováním Arikayce nebyly identifikovány. Akutní toxicita by měla být léčena okamžitým stažením Arikayce a měly by být provedeny základní testy funkce ledvin.
Hemodialýza může být užitečná při odstraňování amikacinu z těla.
Ve všech případech podezřelých lékařů o nadměrném věku by se měli kontaktovat regionální středisko pro kontrolu jedu ohledně efektivní léčby. V případě jakéhokoli předávání by se měla zvážit možnost lékových interakcí se změnami v dispozici léčiva.
Kontraindikace pro Arikayce
Arikayce is contraindicated in patients with a known hypersensitivity to any aminoglycoside.
Klinická farmakologie fnebo Arikayce
Mechanismus působení
Arikayce is an Antibakteriální drug [see Mikrobiologie ].
Farmakodynamika
Arikayce exposure-response relationships a the time course of pharmacodynamic response are unknown.
Farmakokinetika
Koncentrace sputa
Po jednou denně inhalaci 590 mg arikayce Mycobacterium avium Koncentrace komplexních (MAC) pacienti sputa po 1 až 4 hodinách po izolaci byly 1720 884 a 1300 mcg/g při 1 3 a 6 měsících. Byla pozorována vysoká variabilita koncentrací amikacinu (CV%> 100%). Po 48 až 72 hodinách se koncentrace amikacin sputum snížily na přibližně 5% koncentrací po 1 až 4 hodinách po izolaci.
Koncentrace v séru
Po 3 měsících kdysi denní inhalace 590 mg Arikayce u pacientů s MAC průměrný sérum AUC0-24 bylo 23,5 mcg*h/ml (rozmezí: 8,0 až 46,5 mcg*h/ml; n = 12) a průměrný sérum CMAX (NULL,8 mcg/ml (NULL,0 až 4,4 μg/ml; n = 12). Maximální CMAX a AUC0-24 byly pod průměrnou CMAX přibližně 76 mcg/ml a AUC0-24 154 mcg*h/ml pozorované pro intravenózní podání amikacinu sulfátu pro injekci při schváleném dávkování 15 mg/kg jednou denně u zdravých dospělých.
Vstřebávání
Očekává se, že biologická dostupnost Arikayce se bude lišit především od individuálních rozdílů v účinnosti rozprašovače a patologii dýchacích cest.
Rozdělení
Vazba proteinu amikacinu v séru je ≤ 10%.
Odstranění
Po inhalaci Arikayce u pacientů s MAC se zjevný poločas amikacinu v séru pohyboval od přibližně 5,9 do 19,5 hodin.
Metabolismus
Amikacin nepodléhá značnému metabolismu.
Vylučování
Systemicky absorbovaný amikacin po podávání Arikayce je eliminován hlavně pomocí glomerulární filtrace. V průměru 7,42% (v rozmezí od 0,72 do 22,60%; n = 14) z celkové dávky Arikayce bylo vylučováno v moči jako nezměněné léčivo ve srovnání s 94% po intravenózním podání sulfátu amikacinu pro injekci. Neabsorbovaný amikacin po inhalaci Arikayce je pravděpodobně eliminován především buněčným obratem a vykašláním.
Studie interakce léčiva
S Arikayce nebyly provedeny žádné studie interakce klinických léčiv [viz Lékové interakce ].
Mikrobiologie
Mechanismus působení
Amikacin je polykační semisyntetický baktericidní aminoglykosid. Amikacin vstupuje do bakteriální buňky vazbou na negativně nabité složky bakteriální buněčné stěny narušující celkovou architekturu buněčné stěny. Primárním mechanismem účinku je narušení a inhibice syntézy proteinů v cílových bakteriích vazbou na 30s ribozomální podjednotku.
Odpor
Mechanismus rezistence vůči amikacinu v mykobakteriích byl spojen s mutacemi v genu RRS 16S rRNA. V klinických studiích Izoláty MAC vyvíjející amikacin mikrofon> 64 mcg/ml po základní linii byly pozorovány ve vyšší podílu subjektů léčených Arikayce [viz viz Klinické studie ].
Interakce s jinými antimikrobiálními látkami
Nebyl tam ne in vitro signal for antagonism between amikacin and other antimicrobials against MAC based on fractional inhibitory concentration (FIC) and macrophage survival assays. In select instances some degree of synergy between amikacin and other agents has been observed as for example synergy between aminoglycosides including amikacin and the beta-lactam class has been documented.
Toxikologie zvířat Andor Pharmakologie
Pro poskytnutí informací o chronickém dávkování Arikayce jinému živočišnému druhu byla u psů provedena studie toxikologie 9měsíční inhalační toxikologie. Ploomy alveolární makrofágy spojené s clearancem inhalačního produktu byly přítomny při výskytu a závažnosti související s dávkou, ale nebyly spojeny s hyperplázií zánětlivé tkáně nebo přítomností preneoplastických nebo neoplastických změn. Psi byli vystaveni Arikayce po dobu až 90 minut denně a poskytovali inhalované dávky amikacinu přibližně 5 10 a 30 mg/kg/den.
Klinické studie
Zkouška 1 (NCT Mycobacterium avium Komplexní (MAC) plicní onemocnění, jak bylo potvrzeno nejméně 2 výsledky kultury sputa. Pacienti byli považováni za refrakterní onemocnění plic MAC, pokud nedosáhli negativních kultur sputa po minimální délce 6 po sobě jdoucích měsíců terapie režimem na pozadí, která probíhala nebo zastavila déle než 12 měsíců před screeningovou návštěvou. Pacienti byli randomizováni na Arikayce plus samotný režim pozadí nebo režimu pozadí. Koncový bod náhradního zájmu pro posouzení účinnosti byl založen na dosažení přeměny kultury (3 po sobě jdoucí měsíční negativní kultury sputa) do 6. měsíce. Datum přeměny bylo definováno jako datum první ze 3 negativních měsíčních kultur, které musely být dosaženy do 4 měsíce, aby bylo možné do 4 měsíce na základě na základě na základě rezidenta nebo na základě na základě na základě na základě na základě na základě na základě na základě na základě rezitifikaci nebo na základě na základě na základě na základě na základě na základě na základě na základě rezitifikace nebo na základě na základě rezimenu nebo na základě na základě na základě koncového bodu. Celkem 12 měsíců po první negativní kultuře sputa.
Celkem 336 pacientů bylo randomizováno (Arikayce plus režim pozadí n = 224; režim pozadí sám n = 112) (ITT populace) s průměrným věkem 64,7 let a ve studii bylo vyšší procento žen (NULL,3%) než muži (NULL,7%). V době zápisu 336 subjektů v populaci ITT byla 302 (NULL,9%) buď na režimu založeném na pokynech pro Mac, nebo mimo terapii pro Mac za méně než 3 měsíce, zatímco 34 (NULL,1%) bylo mimo léčbu po dobu 3 až 12 měsíců před registrací. Při screeningu byli pacienti stratifikováni podle stavu kouření (současný kuřák nebo ne) a tím, zda byli pacienti v léčbě nebo mimo léčbu po dobu nejméně 3 měsíců. Většina pacientů při screeningu nebyla současná kuřáci (NULL,3%) a měla základní bronchiektasis (NULL,5%). Na základní linii bylo 329 pacientů na podkladovém režimu s více léky, který zahrnoval makrolid (NULL,3%) rifamycin (NULL,3%) nebo ethambutol (NULL,4%). Celkově 55,6% subjektů dostávalo režim na pozadí trojitého léčiva sestávajícího z makrolidu rifamycinu a ethambutolu.
Podíl pacientů dosahujících přeměnu kultury (3 po sobě jdoucí měsíční negativní kultury sputa) do 6. měsíce byl významně (P <0.0001) greater fnebo Arikayce plus background regimen (65/224 29.0%) compared to background regimen alone (10/112 8.9%). Of those receiving Arikayce plus background regimen 18.3% (41/224) achieved culture conversion by Month 6 a sustained sputum culture conversion (defined as consecutive negative sputum cultures with no positive culture on solid media nebo no mneboe than 2 consecutive positive cultures on liquid media following culture conversion) fnebo up to 12 months of treatment after the first culture that defined culture conversion compared to 2.7% (3/112) of patients receiving background regimen alone (p <0.0001). At 3 months after the completion of treatment 16.1% (36/224) of patients who had received Arikayce plus background regimen maintained durable culture conversion compared to 0% of patients who had received background regimen alone (p <0.0001).
Kumulativní podíl subjektů dosahujících přeměnu kultury ukázaného prvním měsícem konverze záměru k léčbě (ITT) populace
 |
Ve studii 1 23/224 (NULL,3%) pacientů měl izoláty MAC, které se vyvinuly MIC> 64 mcg/ml při léčbě Arikayce. V samotném režimu na pozadí mělo rameno 4/112 (NULL,6%) pacientů izoláty MAC, které se vyvinuly amikacin MIC> 64 mcg/ml.
Další koncové body pro posouzení klinického přínosu Arikayce, například změny ze základní linie v šestiminutové vzdálenosti testování a respirační dotazník Saint George neprokázal klinický přínos do 6. měsíce.
Informace o pacientovi pro Arikayce
Arikayce
(Ar 'i Kase)
Omezená populace
(Amikacin Liposom Inhalation Suspension) Pro orální inhalační použití
Důležité: pouze pro orální inhalaci.
Jaké jsou nejdůležitější informace, které bych měl vědět o Arikayce?
Arikayce can cause serious side effects including:
- Alergický zánět plic: Tyto respirační problémy mohou být příznaky alergického zánětu plic a často přicházejí s:
- horečka
- síť
- kašeling
- dušnost
- Rychlé dýchání
- kašeling up of blood (hemoptysis): Kašeling up blood is a serious a common side effect of Arikayce.
- Těžké dýchací problémy: Těžké dýchací problémy mohou být příznaky bronchospasmu. Bronchospasmus je vážný a běžný vedlejší účinek Arikayce. Mezi příznaky bronchospasmu patří:
- dušnost
- obtížné nebo namáhavé dýchání
- síť
- kašeling nebo těsnost hrudníku
- Zhoršení chronického obstrukčního plicního onemocnění (COPD): Toto je vážný a běžný vedlejší účinek Arikayce.
- Vážné alergické reakce: Vážné alergické reakce, které mohou vést k smrti, se staly lidem, kteří berou Arikayce. Přestaňte okamžitě brát Arikayce a získejte pohotovostní lékařskou pomoc, pokud máte některý z následujících příznaků vážné alergické reakce:
- kopřivka
- hlučný vysoký
- Rychlé dýchání srdeční frekvence (Stridor)
- svědění
- kašel
- Cítíte světlo
- zarudnutí nebo červenání
- nevolnost
- cítit se slabý kůži (spláchnutí)
- oteklé rty jazyk nebo
- zvracení
- Ztráta kontroly střeva krku nebo močového měchýře (inkontinence)
- potíže s dýcháním nebo
- průjem
- závrať síť
- dušnost
- cítit křeče v oblasti žaludku
Při použití Arikayce se tyto vedlejší účinky mohou stát natolik závažným, že je zapotřebí léčby v nemocnici.
Zavolejte svému poskytovateli zdravotní péče nebo okamžitě získejte lékařskou pomoc Při užívání Arikayce máte některý z těchto vážných vedlejších účinků. Váš poskytovatel zdravotní péče vás může požádat, abyste přestali používat Arikayce na krátkou dobu nebo úplně přestat používat Arikayce.
Co je Arikayce?
Arikayce is a prescription medicine used to treat adults with refractneboy (difficult to treat) Mycobacterium avium Komplexní (MAC) plicní onemocnění v rámci kombinované antibakteriální léčby léčby (režim).
Není známo, zda je Arikayce bezpečný a účinný u dětí mladších 18 let. Tento produkt byl schválen FDA pomocí omezené populační dráhy.
To znamená, že FDA schválila tento lék pro omezenou a specifickou populaci pacientů a studie léku mohly odpovědět pouze na zaměřené otázky týkající se jeho bezpečnosti a účinnosti.
Nepoužívejte Arikayce, pokud:
- jsou alergické na jakýkoli aminoglykosid nebo některá ze složek v Arikayce. Vidět Jaké jsou ingredience v Arikayce? Na konci tohoto letáku pro úplný seznam složek v Arikayce.
Před použitím Arikayce řekněte svému poskytovateli zdravotní péče o všech vašich zdravotních stavech, včetně, pokud jste:
- Mají astma chronické obstrukční plicní onemocnění (COPD) dušnost nebo sípání (bronchospasmus).
- bylo řečeno, že máte špatnou funkci plic.
- mít nebo mít problémy s sluchem (včetně zvuků ve vašich uších, jako je vyzvánění nebo syčení) Ztráta sluchu nebo vaše matka měla problémy s sluchem po aminoglykosidu.
- bylo řečeno, že máte určité genové varianty (změna genu) související s abnormalitami slyšení zděděných od vaší matky.
- mít závratě nebo smysl pro točení místnosti.
- mít problémy s ledvinami.
- mají neuromuskulární onemocnění, jako je myasthenia gravis.
- are pregnant or plan to become pregnant. It is not known if ARIKAYCE can harm your unborn baby. ARIKAYCE is in a class of medicines that may be connected with complete deafness in babies at birth. The deafness affects both ears and cannot be changed.
- jsou kojení nebo plánují kojení. Není známo, zda lék v Arikayce prochází do mateřského mléka a pokud to může poškodit vaše dítě. Promluvte si se svým poskytovatelem zdravotní péče o nejlepším způsobu, jak nakrmit své dítě během léčby Arikayce.
Řekněte svému poskytovateli zdravotní péče o všech lécích, které užíváte Léky na předpis a overthelter Medicines Vitaminy a bylinné doplňky.
Jak mám použít Arikayce?
- Přečtěte si pokyny krok za krokem pro použití Arikayce na konci průvodce medikací a úplné pokyny pro použití ve vaší soupravě. Pokyny výrobce pro použití poskytují úplné informace o tom, jak sestavit (sestavit) Připravte použití čisté a dezinfikujte svou lamira ® Nebulizer System.
- Ne Používejte Arikayce, pokud nepochopíte poskytnuté pokyny. Pokud máte otázky, promluvte si se svým poskytovatelem zdravotní péče nebo zavolejte na podporu Arikares na čísle 1-833-Arikare (1-833-274-5273).
- Použijte Arikayce přesně tak, jak vám poskytuje váš poskytovatel zdravotní péče, abyste jej používali. Nepoužívejte Arikayce častěji, než je vám předepsáno.
- Používejte pouze Arikayce se systémem Nebulizer Lamira.
- Nadechněte každou denní dávku Arikayce 1krát každý den přes sluchátko Lamira Nebulizer. Nepoužívejte více než 1 lahvičku Arikayce za den.
- Ne use Arikayce after the expiration date on the vial. If you fneboget to take your daily dose of Arikayce take your next dose at your usual time the next day.
- Ne Dvojnásobte dávku, abyste nahradili promarněnou dávku.
- Ne Přestaňte používat Arikayce nebo jiné léky k léčbě vaší plicní choroby MAC, pokud k tomu bude váš poskytovatel zdravotní péče sdělen.
- Pokud používáte příliš mnoho Arikayce, zavolejte svému poskytovateli zdravotní péče nebo hned jděte do nejbližší pohotovostní místnosti.
Jaké jsou možné vedlejší účinky Arikayce?
Arikayce may cause serious side effects including:
- Vidíte, jaké nejdůležitější informace bych měl vědět o Arikayce?
- Ztráta sluchu nebo zvonění v uších (ototoxicita) . Ototoxicita je vážný a běžný vedlejší účinek Arikayce. Okamžitě řekněte svému poskytovateli zdravotní péče, pokud máte ztrátu sluchu nebo uslyšíte zvuky v uších, jako je vyzvánění nebo syčení. Sdělte svému poskytovateli zdravotní péče, pokud začnete mít problémy s rovnováhou nebo závratě (Vertigo).
- Zhoršení problémů s ledvinami (nefrotoxicita). Arikayce is in a class of medicines which may cause wnebosening kidney problems. Your healthcare provider may do a blood test to check how well your kidneys are wneboking during your treatment with Arikayce.
- Zhoršení svalové slabosti (neuromuskulární blokáda). Arikayce is in a class of medicines which can cause muscle slabost to get wnebose in people who already have problems with muscle slabost (myasthenia gravis).
Mezi nejčastější vedlejší účinky Arikayce patří:
- změny ve vašem hlase a
- bolest v krku
- chrapot bolesti svalů (dysfonie)
- průjem
- nevolnost
- únava (únava)
- horečka
- zvracení
- bolest hlavy
- snížená hmotnost
- zvýšené sputa
- vyrážka
- nepohodlí na hrudi
- kašel during nebo after a dose of Arikayce especially in the first month after starting treatment.
Nejedná se o všechny možné vedlejší účinky Arikayce.
co dělat v Havaně na Kubě
Zavolejte svého lékaře nebo lékárníka, kde najdete lékařskou radu ohledně vedlejších účinků. Můžete nahlásit vedlejší účinky FDA na 1-800-FDA-1088
Jak mám ukládat Arikayce?
- Uložte lahvičky Arikayce v chladu mezi 36 ° F až 46 ° F (2 ° C až 8 ° C) až do data vypršení platnosti na lahvičce. Ne zmrazení.
- Poté, co byla Arikayce uložena v lednici, musí být po datu vypršení platnosti na lahvičku po datu lahvičky nevyužíván nepoužitý lék.
- Uložte lahvičky Arikayce při teplotě místnosti mezi 68 ° F až 77 ° F (20 ° C až 25 ° C) po dobu až 4 týdnů
- Poté, co byla Arikayce uložena při pokojové teplotě, musí být na konci 4 týdnů vyhozen nevyužitý lék (zlikvidován).
- Okamžitě použijte otevřenou lahvičku Arikayce.
- Okamžitě zahoďte Arikayce Vial po použití.
Udržujte Arikayce a všechny léky mimo dosah dětí.
Obecné informace o bezpečném a efektivním používání Arikayce
Léky jsou někdy předepisovány pro jiné účely než ty, které jsou uvedeny v průvodci s léky. Nepoužívejte Arikayce pro podmínku, pro kterou nebyl předepsán. Nedávejte Arikayce jiným lidem, i když mají stejné příznaky, jaké máte. Může jim to poškodit. Můžete požádat svého lékárníka nebo poskytovatele zdravotní péče o informace o Arikayce, která je psána pro zdravotnické pracovníky.
Jaké jsou ingredience v Arikayce?
Aktivní složka: Amikacin sulfát
Neaktivní ingredience: Chlorid sodný sodný dipalmitoylfosfatidylcholin (DPPC) cholesterol sodný (pro nastavení pH) a vodu pro injekci
Tento průvodce medikací byl schválen americkou správou potravin a léčiv.
Pokyny pro použití
Arikayce ®
Omezená populace
(Amikacin Liposom Inhalation Suspension) Pro orální inhalační použití
Lamira ®
Nebulizer System
Před použitím systému Nebulizer Lamira se ujistěte, že jste si přečetli a porozuměli podrobným informacím v úplných pokynech pro použití, které přicházejí se systémem Nebulizer Lamira. To poskytne úplnější informace o tom, jak sestavit (sestavit) Připravte použití čisté a dezinfikujte svůj systém Nebulizer Lamira. Pokud nerozumíte žádné části pokynů kontaktujte Podpora Arikares na 1-833-Arikare (1-833-274-5273) Před použitím systému Nebulizer Lamira.
Shromážděte medicínu Arikayce. 28denní sada Arikayce obsahuje:
- 1 Průvodce Arikayce Quick Start
- 1 pokyny pro použití vložení
- 1 Úplné předepisování informací vložky
- 1 Nebulizer s lamira
- 4 hlavy lamira aerosolu (1 v každé týdenní krabici)
- 28 lahviček (1 lahvička každý den) Arikayce (7 v každé týdenní krabici)
Zkontrolujte, zda máte všechny potřebné díly pro svůj systém Nebulizer Lamira:
- Případ
- Připojovací šňůra
- Řadič
- A/C napájení
- AA baterie
 |
Stravová sluchátka Nebulizer Lamira:
- Lékařská uzávěr a těsnění
- Medikační rezervoár
- Modrý ventil
- Aerosolová komora
- Náustek
- Náhradní aerosolová hlava
 |
Budete také potřebovat následující zásoby, které nepřicházejí ve vaší 28denní sadě Arikayce, která vám pomůže pečovat o váš systém Nebulizer Lamira:
- Čisté tekuté mýdlo pro čištění sluchátka a aerosolové hlavy
- Destilovaná voda pro dezinfekci sluchátka a aerosolové hlavy
Vyberte si napájení a připravte jej.
A. 4 AA baterie
 |
b. A/C napájení
- Připojte napájení A/C do ovladače.
- Zapojte napájení A/C do výstupu zdi.
Ne insert the A/C Power into thefront of the Řadič.
 |
Čištění a dezinfekce
Než nejprve použijte opláchnutí čistě a dezinfikujte sluchátko a aerosolovou hlavu. Po každém použití se pohybujte vpřed Opláchněte a dezinfikujte sluchátko včetně aerosolové hlavy.
Když obdržíte sluchátko a aerosolovou hlavu, nebudou sterilní. Čištění a dezinfekce sluchátka a aerosolové hlavy je důležité pro snížení rizika onemocnění a kontaminace infekce.
- Čištění sluchátka a připomenutí hlavy aerosolu: Před prvním použitím opláchněte a vyčistěte sluchátko a aerosolovou hlavu. Pohybujte se dopředu a vyčistěte sluchátko včetně aerosolové hlavy hned po každém použití.
Používejte pouze obyčejné suché papežky nebo ubrousky. Ne use towels nebo wipes that have any chemicals added to them such as alcohol lotion nebo baby wipes.
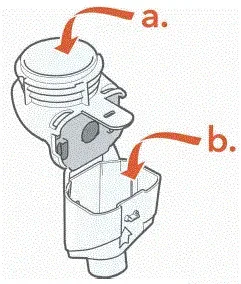
Dávejte pozor, abyste nepoškodili části. Neotřete aerosolovou hlavu.
Vyhoďte papírové ručníky likvidací do odpadu s pevným odpadem.

- Rozebrat (demontáž) sluchátko pro čištění
- Jemně otřete jakékoli kapky medicíny z medikační nádrže (a) aerosolové komory (B) a náustku (c) před oplachováním, aby se snížila antibiotika přidaná do vodních systémů.
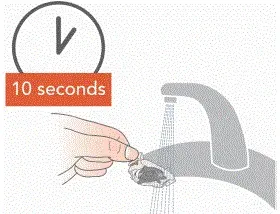
- Opláchněte každou z částí pod teplou běžící vodou z vodovodu pro 10 sekund. Opláchněte aerosolovou hlavu 10 sekund na každé straně.
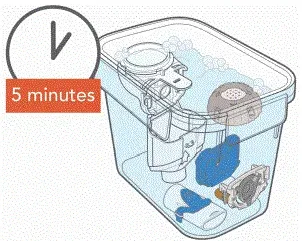
- Vyčistěte všechny díly sluchátka přidáním několika kapek čistého tekutého mýdla a teplé vodovodní vody do čisté vany nebo mísy. Zakryjte díly sluchátka v teplé mýdlové vodě a namočte pro 5 minut pravidelně je třese. Potom je důkladně opláchněte pod teplou běžeckou vodou z vodovodu.
- Před prvním použitím dezinfikuje sluchátko a aerosolovou hlavu před prvním použitím: dezinfikujte sluchátko a aerosol před prvním použitím.

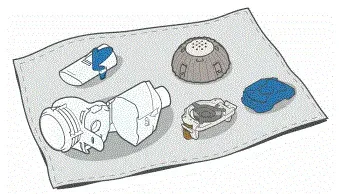
- Než dezinfikujete, ujistěte se, že vaše sluchátko a aerosolová hlava jsou čisté.
- Ujistěte se, že hrnec má dostatek destilované vody, aby zcela zakryl všechny části sluchátka včetně aerosolové hlavy.
- Zahřejte vodu do varu v čistém hrnci.
- Umístěte díly sluchátka včetně aerosolové hlavy do vroucí vody.
- Vařit na plný 5 minut . Poznámka: Může být užitečné použít časovač.
- Na vzduchu suchý na a bez vlády ručník. Při plně suchém zabalení dílů do ručníku bez vlákna pro skladování. Můžete je dát dohromady znovu těsně před dalším ošetřením.
Sestavení sluchátka
Krok 1: Umyjte si ruce mýdlo a voda a dry them well.
 |
Krok 2: Vložte modrý ventil.
Otevřete telefon jemným vytažením na kartě nádrže na léky.
Vložte modrý ventil tak, aby spočíval na vrcholu aerosolové komory s 2 chlopněmi ventilu směrem dolů (chlopně ventilů nejsou ohnuté).
 |
AER OSOL C HAMBER VAL V VE FALLALOVÁ KLAPU MODRA
Krok 3: Vložte aerosolovou hlavu.
Uchopte aerosolovou hlavu 2 flexibilními plastovými kartami na každé straně. Ujistěte se, že text Lamira ® směřuje k vám a je na vrcholu aerosolové hlavy.
Stisknutím 2 flexibilních plastových jazýčků dohromady vložte aerosolovou hlavu do nádrže na léky.
Po dokončení zavřete sluchátko (žádné mezery podél okraje modrého ventilu).
 |
Ne touch the silver part of theAerosol Head at any time.
Poté, co byla aerosolová hlava použita 7krát odhození (likvidace) a nahradí novou onidukací procesu čištění. Sluchátka Lamira se použije po dobu 28 dnů.
 |
Krok 4: Připojte náustek polykavový sluchátko s modrým klapkem nahoru.
 |
Krok 5: Nakonec připojte sluchátko k ovladači.
A. Připojte připojovací šňůru k sluchátku. A1. Spojte spodní část konektoru se spodkem sluchátka.
A2. Posuňte nahoru proti sluchátku, dokud neslyšíte, jak se kousky zachytí dohromady. b. Připojte připojovací šňůru k ovladači.
 |
Brát Arikayce
Váš Arikayce by měl být před použitím na pokojovou teplotu, aby se ujistil, že váš systém Nebulizer Lamira funguje správně. Ne use other medicines in your Haset.
Přiveďte Arikayce na pokojovou teplotu odstraněním z chladničky nejméně 45 minut před použitím. Ne use if your Arikayce has been frozen.
Krok 1: Připravte si Arikayce.
- Umístěte sluchátko na čistý plochý stabilní povrch.
- Protřepejte lahvičku Arikayce po dobu minimálně 10 až 15 sekund A dokud lék nevypadá stejně a dobře smíšený.
 |
Jak otevřít lahvičku Arikayce
 |
 |
 |
 |
- Zvedněte oranžovou čepici z lahvičky.
- Uchopit kovový prsten Na horní část lahvičky a jemně ji stáhněte, dokud se 1 boční se nerozbije od lahvičky, ale kartu nevytáhněte.
- Vytáhněte kovovou pásmo z kolem lahvičky vrcholem kruhovým pohybem, dokud se úplně nevypadne.
- Pečlivě vyjměte gumová zátka.
A. Otevřete lahvičku a nalijte Arikayce do nádrže na léky.
b. Připojte medikační čepici.
 |
Krok 2: Posaďte se ve uvolněné vzpřímené poloze.
- Stiskněte a podržte na tlačítku ON/OFF na několik sekund, abyste zapnuli Lamira.
- Mlha začne proudit.
 |
Krok 3: Vložte náustek (ale nezakrývejte modrou chlopni) a pomalu se zhluboka nadechněte.
- Poté normálně dýchejte dovnitř a ven skrz náustek, dokud nebude vaše ošetření dokončeno.
- Léčba by měla trvat asi 14 minut, ale může trvat až 20 minut.
Nezapomeňte udržet úroveň sluchátka během léčby.
 |
Krok 4: Zkontrolujte, zda vaše léčba skončila.
- Lamira pípne dvakrát.
- Na obrazovce se krátce objeví zaškrtnutí.
- Řadič se automaticky vypne.
- Odstraňte uzávěr léku a Zkontrolujte nádrž na léky, abyste se ujistili, že ne více než několik kapek Arikayce nezůstane. Pokud Arikayce zůstává nahrazením medikačního uzávěru stiskněte tlačítko ON/OFF a doplňte vaši dávku.
 |
Pro všechny problémy, které můžete mít s vaším systémem Nebulizer Lamira, viz část j -frequely kladena otázky a oddíl K -odstraňování úplných pokynů pro použití, které přicházejí s vaším lékem.
Po použití čištění sluchátka Lamira a aerosolu
- Opláchněte čisté a dezinfikujte sluchátko hned po každém použití ke snížení onemocnění a kontaminace infekce.
- Po každém použití dezinfikujte sluchátko a aerosolovou hlavu.
- Podívejte se na čištění a dezinfekci na začátku pokynů pro použití v tom, jak správně vyčistit a dezinfikovat sluchátko a aerosolovou hlavu.
Tyto pokyny pro použití byly schváleny americkou správou potravin a léčiv.






