Informace Na Stránce Nepředstavují Lékařskou Radu. Nic Neprodáváme. Přesnost Překladu Není Zaručena. Zřeknutí Se Odpovědnosti
Antibiotika, lincosamidCleocin IV
Shrnutí drog
Co je Cleocin?
Cleocin (clindamycin) je antibiotikum používané k léčbě vážných infekcí způsobených citlivými anaerobními bakteriemi. Cleocin je k dispozici v obecné podobě.
Jaké jsou vedlejší účinky cleocinu?
Cleocin IV
- kopřivka
- potíže s dýcháním
- Otok vašeho obličeje rty jazyk nebo krk
- Trvalá průjem
- Bolest břicha
- křeče
- krev nebo hlen ve své stolici
- bolest nebo otok v místě injekce
- Tmavá moč
- Žutání kůže nebo očí (žloutenka)
- trvalá nevolnost nebo zvracení
- Změna množství moči
- Snadné modřiny nebo modřiny
- bolest kloubů
- horečka
- Trvalé bolesti v krku
- Rychlý pomalý nebo nepravidelný srdeční rytmus
- mdloby a
- Těžká závratě
Získejte lékařskou pomoc okamžitě, pokud máte výše uvedené příznaky.
Mezi vedlejší účinky cleocinu patří:
k čemu se používá protamin sulfát
- Bolest břicha
- pseudomembranózní kolitida
- Ezofagitida
- nevolnost
- zvracení
- průjem
- nepříjemná nebo kovová chuť v ústech (pokud je cleocin injikován do žíly)
- bolest a otok v místě injekce (pokud je cleocin injikován do svalu)
- reakce přecitlivělosti (vyrážka a úly)
- svědění
- vaginální infekce a
- Žutání kůže a očí (žloutenka).
Řekněte svému lékaři, pokud máte vážné vedlejší účinky cleocinu, včetně:
- bolest nebo otok v místě injekce (pokud je tento lék vstřikován do žíly)
- Tmavá moč
- žloutnutí očí nebo kůže
- trvalá nevolnost nebo zvracení
- změna množství moči
- Snadné modřiny nebo krvácení
- bolest v několika kloubech
- Nové známky infekce (např. Horečka přetrvávající bolest v krku)
- Rychlý/pomalý/nepravidelný srdeční rytmus nebo
- mdloby.
Pokud máte následující vážné vedlejší účinky, vyhledejte lékařskou péči nebo zavolejte na číslo 911:
- Vážné příznaky očí, jako je ztráta náhlého vidění rozmazané vidění vidění Vision Vision Eye Eye Eye Eye Eye Eye Eye Eye nebo vidět halos kolem světel;
- Vážné příznaky srdce, jako je rychlé nepravidelné nebo bušení srdečního rytmu; třepování v hrudi; dušnost; a náhlé závratě lightheadness nebo omdlení;
- Těžká zmatek bolesti hlavy zkažená paže řeči nebo slabost nohou Potíže se ztrátou chůze pocitu koordinace Nestabilní velmi tuhé svaly vysoké horečky bohaté pocení nebo třes.
Tento dokument neobsahuje všechny možné vedlejší účinky a mohou dojít k jiným. Další informace o vedlejších účincích najdete u svého lékaře.
Dávkování pro cleocin
Doporučená dávka cleocinu pro dospělé je 150-450 mg perorálně každých 6 hodin nebo intravenózní dávky 600-2700 mg denně ve 2-4 rozdělených dávkách.
Jaké léčivé látky nebo doplňky interagují s cleocinem?
Cleocin může interagovat s jinými neuromuskulárními blokovacími látkami erytromycin a hormonální antikoncepcí. Řekněte svému lékaři všechny léky a doplňky, které používáte.
Cleocin během těhotenství a kojení
Cleocin nebyl u těhotných žen dostatečně hodnocen. Cleocin by měl být používán během těhotenství, pouze pokud je to jasně potřeba. Cleocin prochází do mateřského mléka a může mít nežádoucí účinky na kojící dítě. Před kojením se poraďte se svým lékařem.
Další informace
Naše drogové centrum pro vedlejší účinky Cleocinu poskytuje při užívání tohoto léku komplexní pohled na dostupné informace o možných vedlejších účincích.
Informace o drogách FDA
- Popis léku
- Indikace
- Dávkování
- Vedlejší účinky
- Lékové interakce
- Varování
- Opatření
- Předávkovat
- Klinická farmakologie
- Průvodce léky
VAROVÁNÍ
C LOSTRIDIUM HARD -Asociovaný průjem (CDAD) byl hlášen s použitím téměř všech antibakteriálních látek včetně cleocinového fosfátu a může se pohybovat závažností od mírné průjem po fatální kolitidu. Léčba antibakteriálními látkami mění normální flóru tlustého střeva vedoucí k přerůstání C. obtížné .
Protože terapie cleocinem fosfátem byla spojena se závažnou kolitidou, která může fatálně ukončit, měla by být vyhrazena pro vážné infekce, kde méně toxická antimikrobiální činidla jsou nevhodná, jak je popsáno v sekci indikací a využití. Neměl by se používat u pacientů s nebakteriálními infekcemi, jako je většina infekcí horních cest dýchacích. C. obtížné produkuje toxiny A a B, které přispívají k rozvoji CDAD. Kmeny produkující hypertoxin C. obtížné Způsobují zvýšenou morbiditu a úmrtnost, protože tyto infekce mohou být refrakterní vůči antimikrobiální terapii a mohou vyžadovat kolektomii. CDAD musí být zvažován u všech pacientů, kteří vyskytují průjem po použití antibiotik. Je nezbytná pečlivá anamnéza, protože bylo hlášeno, že CDAD dochází po dobu dvou měsíců po podání antibakteriálních látek.
Pokud je podezřelý nebo potvrzen probíhající užívání antibiotik, které není namířeno C. obtížné možná bude nutné ukončit. Vhodná ošetření antibiotik proteinu pro proteiny pro proteiny tekutin a elektrolytů C. obtížné a chirurgické hodnocení by mělo být zavedeno podle klinicky uvedeného.
Popis pro Cleocin I.V.
Cleocin fosfátový sterilní roztok v lahvičkách obsahuje clindamycin fosfát ve vodě rozpustný ester clindamycinu a kyseliny fosforečné. Každá ML obsahuje ekvivalent 150 mg clindamycinu 0,5 mg disodiového edetátu a 9,45 mg benzylalkoholu přidáno jako konzervační látku v každém ML. Clindamycin je semisyntetické antibiotikum produkované 7 (S)-chlor-substitucí 7 (R) -hydroxylové skupiny nadřazené sloučeniny lincomycinu.
Chemický název fosfátu clindamycin je L- směr -inzerát- Galacto -Ctopyranosid methyl-7-chlor-678-trideoxy-6-[[(1-methyl-4-propyl-2-pyrrolidinyl) karbonyl] amino] -1-thio- 2- (dihydrogen fosfát) (2S- trans )-.
Molekulární vzorec je C 18 H 34 Stravování 2 0 8 PS a molekulová hmotnost je 504,96.
Strukturální vzorec je reprezentován níže:
 |
Cleocin fosfát v lahvičce Add-Vantage je určen pro intravenózní použití až po dalším zředění s vhodným objemem přídavného roztoku přídavek (vidět Návod k použití ).
Roztok Cleocin fosfátu IV v plastové nádobě galaxie pro intravenózní použití se skládá z klindmycin fosfátu ekvivalentu 300 600 a 900 mg klindamycinu předběžně s 5% dextrózou jako sterilním roztokem. Edetát disodium byl přidán v koncentraci 0,04 mg/ml. PH bylo upraveno hydroxidem sodným a/nebo kyselinou chlorovodíkovou.
Plastová nádoba je vyrobena ze speciálně navrženého vícevrstvého plastového plastu PL 2501. Roztoky ve styku s plastovou nádobou mohou vyluhovat některé ze svých chemických složek ve velmi malých množstvích v období expirace. Vhodnost plastu byla potvrzena testy u zvířat podle biologických testů USP na plastové nádoby a také podle studií toxicity tkáňové kultury.
Použití pro cleocin i.v.
Produkty cleocin fosfátu jsou indikovány při léčbě vážných infekcí způsobených citlivými anaerobními bakteriemi.
Kleocin fosfátové produkty jsou také indikovány při léčbě vážných infekcí v důsledku citlivých kmenů pneumokoků streptokoků a stafylokoků. Jeho použití by mělo být vyhrazeno pro penicilin-alergické pacienty nebo jiné pacienty, u nichž je podle úsudku lékaře penicilin nevhodný. Kvůli riziku pseudomembranské kolitidy spojené s antibiotiky, jak je popsáno v Varování v krabici Před výběrem clindamycinu by měl lékař zvážit povahu infekce a vhodnost méně toxických alternativ (např. Erythromycin).
Měly by být provedeny bakteriologické studie za účelem stanovení příčinných organismů a jejich náchylnosti k clindamycinu.
Uvedené chirurgické zákroky by měly být prováděny ve spojení s antibiotickou terapií.
Cleocin fosfát je indikován při léčbě vážných infekcí způsobených citlivými kmeny určených organismů v níže uvedených podmínkách:
Infekce dolních dýchacích cest včetně empyému pneumonia a plicního abscesu způsobeného anaerobem Streptococcus pneumoniae jiné streptokoky (kromě E. Faecalis ) a Staphylococcus aureus.
Infekce struktury kůže a kůže způsobené Streptococcus pyogenes staphylococcus aureus a Anaerobes.
Gynekologické infekce včetně endometritidy nongonococccal tubo-ovarian absces pánevní celulitida a posturgické infekce vaginální manžety způsobené citlivými anaerobemi.
Intraabdominální infekce včetně peritonitidy a intraabdominálního abscesu způsobeného citlivými anaerobními organismy.
Septikémie způsobená Staphylococcus aureus Streptokoky (kromě Enterococcus faecalis ) a susceptible anaerobes.
Infekce kostí a kloubů včetně akutní hematogenní osteomyelitidy způsobené Staphylococcus aureus a jako doplňková terapie v chirurgické léčbě chronických infekcí kostí a kloubů v důsledku citlivých organismů.
Pro snížení vývoje bakterií rezistentních na léčivo a udržení účinnosti cleocinového fosfátu a jiných antibakteriálních léčiv by měl být Cleocin fosfát použit pouze k léčbě nebo prevenci infekcí, které jsou prokázány nebo silně podezřelé, že jsou způsobeny citlivými bakteriemi. Pokud jsou k dispozici informace o kultuře a citlivosti, měly by být zváženy při výběru nebo úpravě antibakteriální terapie. Při absenci takových dat může místní epidemiologie a vzorce citlivosti přispět k empirickému výběru terapie.
Dávkování pro cleocin I.V.
Pokud se během léčby objeví průjem, mělo by být toto antibiotikum přerušeno (viz viz Varování ).
Podávání clindamycin fosfátu IM by mělo být použity nezředěné.
Jaký je účel taurinu
Podávání fosfátu IV clindamycinu by mělo být zředěno (vidět Zředění pro IV a míru infuze IV níže).
Dospělí
Parenteral (IM nebo IV podávání): Vážné infekce způsobené aerobními gram-pozitivními koky a citlivějšími anaeroby (obecně ne včetně Bakteroides fragilis peptococcus druhy a Clostridium druhy jinými než Clostridium perfringens ):
600.1200 mg/den ve 2 3 nebo 4 stejných dávkách.
Závažnější infekce, zejména infekce, které mají prokázané nebo podezřelé Bakteroides fragilis peptococcus druhy nebo Clostridium species jiné než Clostridium perfringens:
1200,2700 mg/den ve 2 3 nebo 4 stejných dávkách.
Pro vážnější infekce může být nutné tyto dávky zvýšit. V situacích ohrožujících život v důsledku aerobů nebo anaerobů mohou být tyto dávky zvýšeny. Dávky až 4800 mg denně byly podávány intravenózně dospělým. Vidět Zředění pro IV a míru infuze IV sekce níže.
Jednotlivé intramuskulární injekce větších než 600 mg se nedoporučují.
Alternativně může být léčiva podávána ve formě jediné rychlé infuze první dávky následované kontinuální IV infuzí:
| Chcete -li udržovat hladinu klindamycinu v séru | Rychlá míra infuze | Míra údržby |
| Nad 4 mcg/ml | 10 mg/min po dobu 30 minut | 0,75 mg/min |
| Nad 5 mcg/ml | 15 mg/min po dobu 30 minut | 1,00 mg/min |
| Nad 6 mcg/ml | 20 mg/min po dobu 30 minut | 1,25 mg/min |
Novorozenci (méně než 1 měsíc)
15 až 20 mg/kg/den ve 3 až 4 stejných dávkách. Nižší dávka může být přiměřená pro malé předčasnosti.
Pediatričtí pacienti ve věku 1 měsíce do 16 let
Parenterální (IM nebo IV) podávání: 20 až 40 mg/kg/den ve 3 nebo 4 stejných dávkách. Vyšší dávky by byly použity pro závažnější infekce. Jako alternativu k dávkování na tělesné hmotnosti mohou být pediatričtí pacienti podávány na základě povrchu těla čtverečních metrů: 350 mg/m 2 /den pro vážné infekce a 450 mg/m 2 /den pro závažnější infekce.
Parenterální terapie může být změněna na perorální cleocin pediatricr ® Ochucené granule (clindamycin palmitát hydrochlorid) nebo cleocin HCLR ® Tobolky (clindamycin hydrochlorid), když stav zaručuje a podle uvážení lékaře.
V případech β-hemolytické streptokokové infekce by měla být léčba pokračována po dobu nejméně 10 dnů.
Zředění pro IV a míru infuze IV: The concentration of clindamycin in diluent for infusion should not exceed 18 mg per mL. Infusion rates should not exceed 30 mg per minute. Obvyklá ředění a rychlosti infuze jsou následující:
| Dávka | Ředící | Čas |
| 300 mg | 50 ml | 10 min |
| 600 mg | 50 ml | 20 min |
| 900 mg | 50-100 ml | 30 min |
| 1200 mg | 100 ml | 40 min |
Podávání více než 1200 mg v jedné 1hodinové infuzi se nedoporučuje.
Parenterální léčivé přípravky by měly být vizuálně kontrolovány na částice a zbarvení před podáním, kdykoli to roztok a nádoby povolí.
Ředění a kompatibilita
Studie fyzikální a biologické kompatibility monitorované po dobu 24 hodin při teplotě místnosti neprokázaly žádnou inaktivaci ani nekompatibilitu s použitím sterilního roztoku fosfátu v cleocinu (Clindamycin fosfát) v IV roztocích obsahujících chlorid sodný glukóza vápníku nebo draslíku a roztoky vitaminu B v koncentracích obvykle používaných klinicky. Nebyla prokázána žádná nekompatibilita s antibiotiky cefalothinem kanamycin gentamicin penicicilin nebo karbenicililin.
Následující léčiva jsou fyzicky nekompatibilní s Clindamycinem fosfát: ampicilin sodný fenytoin sodný sodný barbituruje aminofylin vápník glukonát a sulfát hořečnatého.
Kompatibilita a trvání stability příměsů léčiva se bude lišit v závislosti na koncentraci a jiných podmínkách. Aktuální informace týkající se kompatibility Clindamycin fosfátu za specifických podmínek prosím kontaktujte lékařskou a drogovou informační jednotku Pharmacia
Fyzikálně-chemická stabilita zředěných roztoků teploty pokojové teploty cleocinu fosfátu
6 9 a 12 mg/ml (ekvivalent k clindamycinové bázi) v injekci dextrózy 5% injekce chloridu sodného 0,9% nebo injekce vyzváněných vrstevníků do skleněných lahví nebo minibagů prokázala fyzikální a chemickou stabilitu po dobu nejméně 16 ° C. Také 18 mg/ml (ekvivalentní clindamycinové bázi) v injekci dextrózy 5% u minibagů prokázalo fyzikální a chemickou stabilitu po dobu nejméně 16 dnů při 25 ° C.
Chlazení
6 9 a 12 mg/ml (ekvivalent clindamycinové báze) v injekci dextrózy 5% injekce chloridu sodného 0,9% nebo laktatované injekční injekce do skleněných lahví nebo minibagů prokázala fyzikální a chemickou stabilitu po dobu nejméně 32 dnů při 4 ° C.
Důležité: Tato informace o chemické stabilitě v žádném případě naznačuje, že by bylo přijatelné používat tento produkt dobře po době přípravy. Dobrá odborná praxe naznačuje, že složené příměsné směsi by měly být podávány, jakmile po přípravě, jak je možné.
Zmrazený
6 9 a 12 mg/ml (ekvivalent k clindamycinové bázi) v injekci dextrózy 5% injekce chloridu sodného 0,9% nebo injekce vyzváněných vyzvánění do minibagů prokázala fyzikální a chemickou stabilitu po dobu nejméně osmi týdnů při -10 ° C.
Zmrazený solutions should be thawed at room temperature and not refrozen.
Pokyny pro vydávání
Hromadný balíček lékárny
Ne pro přímou infuzi
Obbalovací balíček Pharmacy je určen pro použití ve službě Pharmacy Admixture pouze pod kapotou laminárního průtoku. Vstup do lahvičky by měl být proveden s malým průměrem sterilní přenosové sady nebo jiným malým průměrem sterilním vydávacím zařízením a obsahem vydávaným v alikvotech pomocí aseptické techniky. Více položek s jehlou a stříkačkou se nedoporučuje. Po vstupu použijte celý obsah lahvičky rychle. Jakákoli nepoužitá část musí být vyřazena do 24 hodin po počátečním vstupu.
Návod k použití
Cleocin fosfát IV roztok v plastové nádobě galaxie
Předmíchaný roztok cleocin fosfátu IV je pro intravenózní podání pomocí sterilního vybavení. Před použitím pevně zkontrolujte minutové úniky. Pokud jsou nalezeny úniky zlikvidujte roztok, protože sterilita může být narušena. Nepřidávejte doplňkové léky. Parenterální léčivé přípravky by měly být vizuálně kontrolovány na částice a zbarvení před podáním, kdykoli to roztok a nádoby povolí. Nepoužívejte, pokud není řešení jasné a těsnění je neporušené.
Pozor
Nepoužívejte plastové kontejnery v sériových připojeních. Takové použití by mohlo vést k tomu, že vzduchová embolie kvůli zbytkovému vzduchu nakreslené z primárního kontejneru před podáním tekutiny ze sekundárního kontejneru je dokončeno.
Příprava na správu
- Pozastavte kontejner z podpory oční.
- Odstraňte ochránce z výstupního portu na dně kontejneru.
- Připojte administrativní sadu. Viz kompletní pokyny doprovázející sadu.
Příprava cleocinového fosfátu v systému Add-Vantage- . Pro IV pouze použití. Cleocin fosfát 300 mg 600 mg a 900 mg může být rekonstituován v 50 ml (pro 300 mg a 600 mg) nebo 100 ml (pro 900 mg) injekce dextrózy 5% nebo injekce chloridu sodíku 0,9% v přidané nádobě. Systém doplňků naleznete v samostatných pokynech.
Jak dodáno
Každý ml Cleocin fosfát Sterilní roztok obsahuje clindamycin fosfát ekvivalentní 150 mg clindamycinu 0,5 mg disodiuma edetátu 9,45 mg benzylalkoholu přidán jako konzervační látka. V případě potřeby je pH upraveno hydroxidem sodným a/nebo kyselinou chlorovodíkovou. Cleocin fosfát je k dispozici v následujících balíčcích:
25-2 ml lahviček NDC 0009-0870-26
25-4 ml lahviček NDC 0009-0775-26
25-6 ml lahviček NDC 0009-0902-18
5-60 ML Pharmacy Bulk Package NDC 0009-0728-09
Cleocin fosfát je dodáván v lahvičkách s doplňky:
| NDC | Velikost lahvičky | Celkový clindamycin fosfát/lahvička |
| 0009-6582-01 | 25-2 ml lahviček | 300 mg |
| 0009-3124-03 | 25-4 ml lahviček | 600 mg |
| 0009-3447-03 | 25-6 ml lahviček | 900 mg |
Uložte při kontrolované teplotě místnosti 20 ° až 25 ° C (68 ° až 77 ° F) [viz USP].
Cleocin fosfát IV Solution V galaxii jsou plastové nádoby sterilním roztokem clindamycinového fosfátu s 5% dextrózou. Plastové nádoby na dávku Galaxie jsou k dispozici následovně:
24-300 mg/50 ml kontejnerů NDC 0009-3381-02
24-600 mg/50 ml kontejnerů NDC 0009-3375-02
24-900 mg/50 ml kontejnerů NDC 0009-3382-02
Měla by být minimalizována expozice farmaceutických produktů na teplu. Doporučuje se, aby byly plastové nádoby galaxie skladovány při teplotě místnosti (25 ° C). Vyvarujte se teplot nad 30 ° C.
Distribuováno: Pfizer Pharmacia
Vedlejší účinky for Cleocin I.V.
Při použití clindamycinu byly hlášeny následující reakce.
Infekce a zamoření: Clostridium difficile kolitida
Gastrointestinal: Kolitida spojená s antibiotiky (viz VAROVÁNÍS ) pseudomembranózní kolitida břišní bolesti nevolnosti a zvracení. Počátek příznaků pseudomembranózní kolitidy se může objevit během nebo po antibakteriální léčbě (viz viz VAROVÁNÍS ). An unpleasant or metallic taste has been reported after intravenous administration of the higher doses of clindamycin phosphate.
Reakce přecitlivělosti: Během léčivé terapie byly pozorovány makulopapulární vyrážky a urticaria. Generalizované mírné až střední kožní vyrážky podobné morbilliformu jsou nejčastěji hlášeny ze všech nežádoucích účinků.
Byly hlášeny závažné reakce kůže, jako je toxická epidermální nekrolýza, některé s fatálním výsledkem (viz viz VAROVÁNÍS ). Cases of Acute Generálized Exanthematous Pustulosis (AGEP) erythema multiforme some resembling Stevens-Johnson syndrome have been associated with clindamycin. Anaphylactic shock anaphylactic reaction and hypersensitivity have also been reported (vidět VAROVÁNÍS ).
Membrány kůže a sliznic: Byly hlášeny pruritus vaginitis angioedém a vzácné případy exfoliativní dermatitidy (viz viz Reakce přecitlivělosti ).
Játra: Během terapie Clindamycinem byly pozorovány žloutenky a abnormality ve funkcích jaterních funkcí.
Renal: Ačkoli nebyl zaznamenán žádný přímý vztah clindamycinu k poškození ledvin, o čemž svědčí azotemie oligurie a/nebo proteinurie.
Hematopoetika: Byly hlášeny přechodné neutropenie (leukopenie) a eosinofilie. Byly provedeny zprávy o agranulocytóze a trombocytopenii. V žádném z výše uvedeného nemohl být vytvořen žádný přímý etiologický vztah ke souběžné terapii Clindamycin.
Imunitní systém: Byla hlášena reakce léčiva s eosinofilií a případy systémových symptomů (oblékání).
Místní reakce: Po intramuskulární injekci a tromboflebitidě po intravenózní infuzi byly hlášeny inderace bolesti injekce a sterilní absces. Reakce lze minimalizovat nebo zabránit tím, že poskytují hluboké intramuskulární injekce a zabrání dlouhodobému používání intravenózních katétrů.
Muskuloskeletální: Byly hlášeny případy polyartritidy.
Kardiovaskulární: Po příliš rychlém intravenózním podání byly hlášeny kardiopulmonální zatčení a hypotenze (viz viz Dávkování a podávání ).
Lékové interakce for Cleocin I.V.
Ukázalo se, že clindamycin má neuromuskulární blokovací vlastnosti, které mohou zvýšit působení jiných neuromuskulárních blokovacích látek. Proto by měla být používána s opatrností u pacientů, kteří takové látky dostávají.
cestovat znamená
Clindamycin je metabolizován převážně CYP3A4 a v menší míře CYP3A5 k hlavnímu metabolitovému clindamycinu sulfoxidu a menšímu metabolitu N-desmethylclindamycinu. Inhibitory CYP3A4 a CYP3A5 proto mohou zvýšit plazmatické koncentrace klindamycinu a induktory těchto isoenzymů mohou snížit plazmatické koncentrace klindamycinu. V přítomnosti silných inhibitorů CYP3A4 monitoruje nežádoucí účinky. V přítomnosti silných induktorů CYP3A4, jako je monitor rifampicinu pro ztrátu účinnosti.
In vitro Studie ukazují, že klindamycin neinhibuje CYP1A2 CYP2C9 CYP2C19 CYP2E1 nebo CYP2D6 a pouze středně inhibuje CYP3A4.
Antagonismus byl prokázán mezi clindamycinem a erytromycinem in vitro . Kvůli možné klinické významnosti by se dvě léky neměly podávat souběžně.
Varování for Cleocin I.V.
Vidět Varování .
Clostridium Difficile Associated Diarrhea
Clostridium difficile Byl hlášen přidružený průjem (CDAD) s použitím téměř všech antibakteriálních látek včetně cleocinového fosfátu a může se pohybovat v závažnosti od mírné průjem po fatální kolitidu. Léčba antibakteriálními látkami mění normální flóru tlustého střeva vedoucí k přerůstání C. obtížné .
C. obtížné produkuje toxiny A a B, které přispívají k rozvoji CDAD. Kmeny produkující hypertoxin C. obtížné Způsobují zvýšenou morbiditu a úmrtnost, protože tyto infekce mohou být refrakterní vůči antimikrobiální terapii a mohou vyžadovat kolektomii. CDAD musí být zvažován u všech pacientů, kteří vyskytují průjem po použití antibiotik. Je nezbytná pečlivá anamnéza, protože bylo hlášeno, že CDAD dochází po dobu dvou měsíců po podání antibakteriálních látek.
Pokud je podezřelý nebo potvrzen probíhající užívání antibiotik, které není namířeno C. obtížné možná bude nutné ukončit. Vhodná ošetření antibiotik proteinu pro proteiny pro proteiny tekutin a elektrolytů C. obtížné a chirurgické hodnocení by mělo být zavedeno podle klinicky uvedeného.
Anafylaktické a těžké hypersenzitivní reakce
Byly hlášeny anafylaktické šok a anafylaktické reakce (viz Nežádoucí účinky ).
Závažné reakce přecitlivělosti včetně závažných kožních reakcí, jako je toxická epidermální nekrolýza (deset) reakce léčiva s eosinofilií a systémovými příznaky (šaty) a Stevens-Johnson syndrom (SJS), byly hlášeny některé s fatálním výsledkem (viz viz (viz viz (viz viz (viz (viz viz (viz (viz viz (viz (viz (viz syndrom s fatálním výsledkem (viz (viz (viz syndrom SJS). Nežádoucí účinky ).
V případě takové anafylaktické nebo těžké hypersenzitivní reakce trvale přeruší léčbu a zavádí vhodnou terapii.
Mělo by být provedeno pečlivé vyšetřování týkající se předchozí citlivosti na drogy a jiné alergeny.
Toxicita benzylalkoholu u pediatrických pacientů (syndrom lapání)
Tento produkt obsahuje benzylalkohol jako konzervační látka. Konzervační benzylalkohol byl spojen s vážnými nežádoucími účinky, včetně syndromu GGASPING a smrt u pediatrických pacientů. Ačkoli normální terapeutické dávky tohoto produktu běžně dodávají množství benzylalkoholu, která jsou podstatně nižší než ty, které jsou uvedeny ve spojení se syndromem Aspingu, není známo minimální množství benzylalkoholu, u kterého může dojít k toxicitě.
Riziko toxicity benzylalkoholu závisí na podaném množství a kapacitě játra a ledvin detoxikovat chemikálii. Předčasně narozené a nízké porodní hmotnosti mohou s větší pravděpodobností vyvinout toxicitu.
Použití v meningitidě
Vzhledem k tomu, že klindamycin se při adekvátně nefunguje do mozkomíšního moku, by se léčivo nemělo používat při léčbě meningitidy.
Opatření for Cleocin I.V.
Generál
Přezkum zkušeností dosud naznačuje, že podskupina starších pacientů s přidruženým závažným onemocněním může méně dobře tolerovat průjem. Když je u těchto pacientů indikován klindamycin, měli by být pečlivě sledováni pro změnu frekvence střev.
Cleocin fosfát products should be prescribed with caution in individuals with a history of gastrointestinal disease particularly kolitida.
Cleocin fosfát should be prescribed with caution in atopic individuals.
Některé infekce mohou kromě antibiotické terapie vyžadovat řez a drenáž nebo jiné uvedené chirurgické zákroky.
Použití cleocinového fosfátu může mít za následek přerůstání nepoužitelných organismů--tód-kvasinků. Pokud by došlo k superinfekce, by měla být přijata odpovídající opatření, jak je uvedeno v klinické situaci.
Cleocin fosfát should not be injected intravenously undiluted as a bolus but should be infused over at least 10-60 minutes as directed in the Dávkování a podávání sekce.
U pacientů s onemocněním ledvin nemusí být nutná modifikace dávkování clindamycinu. U pacientů se středním až závažným onemocněním jater byla zjištěna prodloužení poločasu clindamycinu. Z Proto nemusí být nutná modifikace dávkování u pacientů s onemocněním jater. Při léčbě pacientů se závažným onemocněním jater by však mělo být provedeno periodické stanovení jaterního enzymu.
Předepisování fosfátu ctoocinu v nepřítomnosti prokázané nebo silně podezřelé bakteriální infekce nebo profylaktické indikace je nepravděpodobné, že by pacientovi poskytovalo přínos a zvyšuje riziko rozvoje bakterií rezistentních na léčivo.
Informace pro pacienty
Pacienti by měli být informováni, že antibakteriální léčiva včetně cleocinového fosfátu by se měla používat pouze k léčbě bakteriálních infekcí. Ne léčí virové infekce (např. Obecně nachlazení). Když je předepsán cleocin fosfát k léčbě pacientů s bakteriální infekcí, by měl být sdělen, že ačkoli je běžné cítit se lépe v průběhu terapie, lék by měl být považován za přesně podle pokynů. Přeskočení dávek nebo nedokončení úplného průběhu terapie může (1) snížit účinnost okamžité léčby a (2) zvýšit pravděpodobnost, že se bakterie v budoucnu vyvinou a v budoucnu nebudou léčitelné cleocinem fosfátem nebo jinými antibakteriálními léky.
Průjem je běžný problém způsobený antibiotiky, která obvykle končí, když je antibiotikum přerušeno. Někdy po zahájení léčby antibiotiky mohou pacienti vyvinout vodnatou a krvavou stolici (s křečemi a horečkou žaludku nebo bez něj), až dva nebo více měsíců po provedení poslední dávky antibiotiky. Pokud k tomu dojde, pacienti by se měli co nejdříve kontaktovat svého lékaře.
Laboratorní testy
Během dlouhodobé terapie periodické testy játra a ledvin a krevních testů a počtu krve.
Zhodnocení mutageneze karcinogeneze plodnosti
Dlouhodobé studie u zvířat nebyly provedeny s Clindamycinem pro vyhodnocení karcinogenního potenciálu. Provedené testy genotoxicity zahrnovaly test mikronukleusu potkana a test reverze Ames Salmonella. Obě testy byly negativní.
Studie plodnosti u potkanů se léčily orálně s až 300 mg/kg/den (přibližně 1,1krát nejvyšší doporučená dospělá lidská dávka založená na Mg/M 2 ) neodhalil žádné účinky na plodnost nebo schopnost páření.
Těhotenství
Teratogenní účinky
V klinických studiích s těhotnými ženami nebylo systémové podávání clindamycinu během druhého a třetího trimestru spojeno se zvýšenou frekvencí vrozených abnormalit.
Clindamycin by měl být použit během prvního trimestru těhotenství, pouze pokud je to jasně potřeba. Během prvního trimestru těhotenství neexistují žádné adekvátní a dobře kontrolované studie u těhotných žen. Protože studie reprodukce zvířat nejsou vždy prediktivní pro reakci člověka, který by měl být tento lék použit během těhotenství, pouze pokud je to jasně potřeba.
Reprodukční studie prováděné u potkanů a myší s použitím perorálních dávek klindamycinu až do 600 mg/kg/den (NULL,1 a 1,1krát nejvyšší doporučenou dospělou lidskou dávku na základě Mg/M Mg/M 2 respektive) nebo subkutánní dávky clindamycinu až do 250 mg/kg/den (NULL,9 a 0,5krát nejvyšší doporučené dospělé lidské dávky založené na Mg/m 2 respektive) neodhalil žádný důkaz teratogenity.
Cleocin fosfát Sterile Solution contains benzyl alcohol. Benzyl alcohol can cross the placenta. see VAROVÁNÍS .
Ošetřovatelské matky
Bylo hlášeno, že clindamycin se objevuje v mateřském mléce v rozmezí 0,7 až 3,8 mcg/ml v dávkách 150 mg orálně až 600 mg intravenózně. Clindamycin má potenciál způsobit nepříznivé účinky na kojení kojeného kojeneckého gastrointestinální flóry. Pokud je ošetřovatelská matka vyžadována ústní nebo intravenózní klindamycin, není to důvod k přerušení kojení, ale lze upřednostňovat alternativní lék. Sledujte dítěte na možné nepříznivé účinky na gastrointestinální flóru, jako je kandidóza průjmu (thrush plenková vyrážka) nebo zřídka krev ve stolici, což ukazuje na možnou kolitidu spojenou s antibiotiky.
Vývojové a zdravotní přínosy kojení by měly být zváženy spolu s klinickou potřebou matky klindmycinu a jakýmikoli potenciálními nepříznivými účinky na kojené dítě z klindamycinu nebo ze základního mateřského stavu.
nejlepší část nashvillu k pobytu
Dětské použití
Když je cleocin fosfátový sterilní roztok podáván pediatrické populaci (narození do 16 let) je žádoucí vhodné monitorování funkcí orgánových systémů.
Použití u novorozenců a kojenců
Tento produkt obsahuje benzylalkohol jako konzervační látka. Benzylalkohol byl u předčasně narozených dětí spojen s fatálním „syndromem zalapávání“. vidět VAROVÁNÍS .
Potenciál toxického účinku v pediatrické populaci z chemikálií, které mohou vyluhovat z jediné dávky předběžné IV přípravy v plastu, nebyl vyhodnocen. vidět VAROVÁNÍS .
Geriatrické použití
Klinické studie clindamycinu nezahrnovaly dostatečný počet pacientů ve věku 65 let a více, aby se určilo, zda reagují odlišně od mladších pacientů. Jiné hlášené klinické zkušenosti však naznačují, že kolitida a průjem spojená s antibiotiky (kvůli kvůli Clostridium difficile ), které se ve spojení s většinou antibiotik vyskytují častěji u starších osob (> 60 let) a mohou být závažnější. Tito pacienti by měli být pečlivě sledováni pro vývoj průjmu.
Farmakokinetické studie s klindamycinem neprokázaly žádné klinicky důležité rozdíly mezi mladými a staršími subjekty s normální funkcí jater a normální (věkově upravenou) renální funkcí po perorálním nebo intravenózním podání.
Informace o předávkování Cleocin I.V.
Významná úmrtnost byla pozorována u myší při intravenózní dávce 855 mg/kg a u potkanů při perorální nebo podkožní dávce přibližně 2618 mg/kg. U myší byla pozorována křeče a deprese.
Hemodialýza a peritoneální dialýza nejsou účinné při odstraňování klindamycinu ze séra.
Kontraindikace pro cleocin i.v.
Tento lék je kontraindikován u jedinců s anamnézou hypersenzitivity na přípravy obsahující clindamycin nebo lincomycin.
Klinická farmakologie for Cleocin I.V.
Rozdělení
Biologicky neaktivní clindamycin fosfát je přeměněn na aktivní clindamycin. Na konci krátkodobého intravenózního infuzního maximálního sérového séra jsou dosaženy aktivní clindamycin.
Po intramuskulární injekci hladin špičkového fosfátu clindamycinu je dosaženo do 3 hodin u dospělých a 1 hodinu u pediatrických pacientů. Křivky na úrovni séra mohou být konstruovány z hladin IV špičkového séra, jak je uvedeno v tabulce 1 aplikací poločasů eliminace (viz Vylučování ).
Sérové hladiny klindamycinu lze udržovat nad in vitro Minimální inhibiční koncentrace pro většinu indikovaných organismů podáváním clindamycin fosfátu každých 8 až 12 hodin u dospělých a každých 6 až 8 hodin u pediatrických pacientů nebo nepřetržitá intravenózní infuze. Rovnováha je dosažena třetí dávkou.
V mozkomíšní tekutině nejsou dosaženy žádné významné hladiny klindamycinu ani v přítomnosti zanícených meningů.
Metabolismus
In vitro Studie v mikrozomech lidských jater a střeva naznačily, že klindamycin je převážně metabolizován cytochromem P450 3A4 (CYP3A4) s menším příspěvkem z CYP3A5 za vytvoření clindamycinu sulfoxidu a menším metabolitem N-desmetylklindamycinem.
Vylučování
Biologicky neaktivní clindamycin fosfát rychle zmizí ze séra; Průměrná poločas eliminace je 6 minut; U dospělých a 2 hodin u pediatrických pacientů je však poločas eliminace séra eliminace aktivního clindamycinu.
Speciální populace
Poškození ledvin/jater
Eliminační poločas clindamycinu se mírně zvyšuje u pacientů s výrazně sníženou funkcí ledvin nebo jater. Hemodialýza a peritoneální dialýza nejsou účinné při odstraňování klindamycinu ze séra. Rozvrhy dávkování nemusí být modifikovány v přítomnosti mírného nebo středního ledvinového nebo jaterního onemocnění.
Použití u starších
Farmakokinetické studie u starších dobrovolníků (61-79 let) a mladší dospělí (18-39 let) naznačují, že samotný věk neměňuje farmakokinetiku Clindamycinu (clearance eliminace poločasu distribuce a plocha pod křivkou sérového koncentrace)) po podání fosfátu clindamycinu. Po perorálním podávání clindamycin hydrochloridu eliminace poločas se zvyšuje na přibližně 4,0 hodiny (rozmezí 3,4-5,1 h) u starších osob ve srovnání s 3,2 hodiny (rozmezí 2,1-4,2 h) u mladších dospělých. Rozsah absorpce se však neliší mezi věkovými skupinami a pro seniory není nutná žádná změna dávkování s normální funkcí jater a normální (věkově přizpůsobené) renální funkce ledvin 1 .
Sérové testy pro aktivní clindamycin vyžadují inhibitor, aby zabránil in vitro Hydrolýza clindamycin fosfát.
Tabulka 1. Průměrné vrcholy a koryto sérové koncentrace aktivního klindamycinu po dávkování clindamycinem fosfátem
| Dávkování Regimen | Vrchol MCG/ML | Koryto MCG/ML |
| Zdraví dospělí muži (po rovnováze) | ||
| 10.9 | 2.0 | |
| 10.8 | 1.1 | |
| 14.1 | 1.7 | |
| 9 | ||
| Pediatričtí pacienti (první dávka)* | ||
| 5-7 mg/kg IV in 1 hour | 10 | |
| 5-7 mg/kg IM | 8 | |
| 3-5 mg/kg IM | 4 | |
| *Údaje v této skupině od pacientů léčených pro infekci. |
Mikrobiologie
Mechanismus působení
Clindamycin inhibuje syntézu bakteriálního proteinu vazbou na 23S RNA podjednotky ribozomu. Clindamycin je bakteriostatický.
Odolnost proti rezistenci vůči klindamycinu je nejčastěji způsobena modifikací specifických bází 23S ribozomální RNA. Křížová rezistence mezi clindamycinem a lincomycinem je kompletní. Protože vazebná místa pro tato antibakteriální léčiva se překrývají zkříženou rezistencí u lincosamidů makrolidů a streptogramin b.macrolid-indukovatelné rezistence vůči clindamycinu na některých izolátech bakterií rezistentních na makrolid. Izoláty stafylokoků a beta-hemolytických streptokoků rezistentních na makrolid by měly být prověřeny pro indukci rezistence na klindamycin pomocí testu D-zóny.
Antimikrobiální aktivita
Ukázalo se, že clindamycin je aktivní proti většině izolátů následujících mikroorganismů in vitro a v klinických infekcích, jak je popsáno v Indikace a použití sekce.
Gram-pozitivní bakterie
Staphylococcus aureus (kmeny citlivé na methicilin)
Streptococcus pneumoniae (kmeny citlivé na penicilin)
Streptococcus pyogenes
Anaerobní bakterie
Clostridium perfringens
Fusobacterium necrophorum
Fusobacterium nucleatum
PeptoStreptococcus Anaerobius
Prevotella melaninogenica
Nejméně 90% níže uvedených mikroorganismů in vitro Minimální inhibiční koncentrace (MICS) menší nebo rovné jako clindamycin citlivý bod mikropočtu pro organismy podobného typu jako koncentrace uvedené v tabulce 2. Účinnost clindamycinu při léčbě klinických infekcí způsobených těmito mikroorganismy však nebyla stanovena v přiměřených a dobře kontrolovaných klinických studiích.
Gram-pozitivní bakterie
Staphylococcus epidermidis (kmeny citlivé na methicilin)
Streptococcus agalactiae
Streptococcus kape
Streptococcus mírný
Orální streptococcus
Anaerobní bakterie
Actinomyces Israel
Clostridium clostridioforme
Eggerthella lentta
Finegoldia (peptostreptococcus) Skvělé
Mikromonas (peptoStreptococcus) micros
Prevotella Bivia
Prevetella Intermedia
Propionibacterium acnes
Metody testování citlivosti
Pokud je k dispozici, měla by klinická mikrobiologická laboratoř poskytnout kumulativní in vitro Výsledky testu citlivosti na antimikrobiální léky používané v místních nemocnicích a oblastech praxe pro lékaře jako periodické zprávy, které popisují profil citlivosti nozokomiálních a komunitě získaných patogenů. Tyto zprávy by měly pomoci lékaři při výběru antibakteriálního léčiva pro léčbu.
Techniky ředění
Kvantitativní metody se používají ke stanovení antimikrobiálních minimálních inhibičních koncentrací (MIC). Tyto MICS poskytují odhady citlivosti bakterií na antimikrobiální sloučeniny. MIC by měly být stanoveny pomocí standardizované testovací metody 23 (Vývar a/nebo agar). Hodnoty MIC by měly být interpretovány podle kritérií uvedených v tabulce 2.
Technické šíření
Kvantitativní metody, které vyžadují měření průměrů zóny, mohou také poskytnout reprodukovatelné odhady citlivosti bakterií na antimikrobiální sloučeniny. Velikost zóny by měla být stanovena pomocí standardizované metody 25 . Tento postup používá papírové disky impregnované 2 mcg clindamycinu k testování citlivosti bakterií na clindamycin. Body přerušení disků jsou uvedeny v tabulce 2.
Anaerobní techniky
U anaerobních bakterií může být citlivost na klindamycin určena standardizovanou testovací metodou 24 . Získané hodnoty MIC by měly být interpretovány podle kritérií uvedených v tabulce 2.
Tabulka 2. Interpretační kritéria testu citlivosti pro klindamycin
| Patogen | Interpretační kritéria citlivosti | |||||
| Minimální inhibiční koncentrace (MIC v MCG/ML) | Disková šířka (Průměry zóny v mm) | |||||
| S | I | R | S | I | R | |
| Staphylococcus spp. | ≤0,5 | 1-2 | ≥ 4 | ≥21 | 15–20 | ≤14 |
| Streptococcus pneumoniae a další Streptococcus spp. | ≤0,25 | 0.5 | ≥1 | ≥19 | 16–18 | ≤15 |
| Anaerobní bakterie | ≤2 | 4 | ≥ 8 | Na | Na | Na |
| Na=not applicable |
Zpráva o Citlivé (s) ukazuje, že antimikrobiální léčivo pravděpodobně inhibuje růst patogenu, pokud antimikrobiální léčivo dosáhne koncentrace obvykle dosažitelné v místě infekce. Zpráva o Střední (i) ukazuje, že výsledek by měl být považován za nejednoznačný a pokud mikroorganismus není plně citlivý na alternativní klinicky proveditelné léky, měl by být test opakován. Tato kategorie znamená možnou klinickou použitelnost v místech těla, kde je lék fyziologicky koncentrovaný nebo v situacích, kdy lze použít vysokou dávkování léčiva. Tato kategorie také poskytuje vyrovnávací zónu, která zabraňuje malým nekontrolovaným technickým faktorům způsobovat hlavní nesrovnalosti při interpretaci. Zpráva o Odolný (R) ukazuje, že antimikrobiální léčivo pravděpodobně inhibuje růst patogenu, pokud antimikrobiální léčivo dosáhne koncentrace obvykle dosažitelné v místě infekce; Měla by být vybrána jiná terapie.
Kontrola kvality
Postupy testu standardizovaného náchylnosti vyžadují použití laboratorních ovládacích prvků ke sledování a zajištění přesnosti a přesnosti zásob a činidel použitých v testu a techniky jednotlivců provádějících test 2345 . Standardní clindamycinový prášek by měl poskytnout rozsahy MIC v tabulce 3. Pro techniku diskované diskové diskové diskové diskové disky pomocí 2 mcg clindamycinového disku je měla být dosažena kritéria uvedená v tabulce 2.
Tabulka 3. Přijatelné rozsahy kontroly kvality pro clindamycin
| Kmen QC | Přijatelné rozsahy kontroly kvality | |
| Minimální rozsah inhibiční koncentrace (MCG/ML) | Disková šířka Range (Průměry zóny v mm) | |
| Enterococcus faecalis 1 ATCC 29212 | 4-16 | Na |
| Staphylococcus aureus ATCC 29213 | 06-0,25 | Na |
| Staphylococcus aureus ATCC 25923 | Na | 24-30 |
| Streptococcus pneumoniae ATCC 49619 | 0,03-0,12 | 19-25 |
| Bakteroides fragilis ATCC 25285 | 0,5-2 | Na |
| Bakteroides thetaiotaomicron ATCC 29741 | 2-8 | Na |
| Clostridium difficile 2 ATCC 700057 | 2-8 | Na |
| Eggerthella lentta ATCC 43055 | 06-0,25 | Na |
| 1. Enterococcus faecalis byl zahrnut do této tabulky pouze pro účely kontroly kvality. 2. Kontrola kvality pro C. obtížné je prováděno pomocí metody ředění agaru, pouze všechny ostatní zavinuté anaeroby mohou být testovány buď metodami mikrodiluce vývaru nebo agaru. Na=Not applicable ATCC ® je registrovaná ochranná známka sbírky amerického typu kultury |
Reference
1. Smith RB Phillips JP: Vyhodnocení cleocinového HC1 a cleocinového fosfátu ve věku populace. Upjohn TR 8147-82-9122-021 prosinec 1982.
2. Clsi. Výkonné standardy pro testování antimikrobiální citlivosti: 26 th Ed. CLSI doplněk M100S. Wayne PA: Institut klinických a laboratorních standardů; 2016.
3. CLSI. Metody pro zředění antimikrobiálních testů citlivosti na bakterie, které aerobně rostou; Schválený standard -Centé vydání. Dokument CLSI M07-A10. Wayne PA: Institut klinických a laboratorních standardů; 2015.
4. Clsi. Metody testování antimikrobiální citlivosti anaerobních bakterií; Schválené standardní osmé vydání. Dokument CLSI M11-A8. Wayne PA: Institut klinických a laboratorních standardů; 2012.
5. CLSI. Výkonné standardy pro testy citlivosti na antimikrobiální disk; Schválené standardní vydání. Dokument CLSI M02-A12. Wayne PA: Institut klinických a laboratorních standardů; 2015.
Informace o pacientovi pro cleocin i.v.
Pacienti by měli být informováni, že antibakteriální léčiva včetně cleocinového fosfátu by se měla používat pouze k léčbě bakteriálních infekcí. Ne léčí virové infekce (např. Obecně nachlazení). Když je předepsán cleocin fosfát k léčbě pacientů s bakteriální infekcí, by měl být sdělen, že ačkoli je běžné cítit se lépe v průběhu terapie, lék by měl být považován za přesně podle pokynů. Přeskočení dávek nebo nedokončení úplného průběhu terapie může (1) snížit účinnost okamžité léčby a (2) zvýšit pravděpodobnost, že se bakterie v budoucnu vyvinou a v budoucnu nebudou léčitelné cleocinem fosfátem nebo jinými antibakteriálními léky.
Průjem je běžný problém způsobený antibiotiky, která obvykle končí, když je antibiotikum přerušeno. Někdy po zahájení léčby antibiotiky mohou pacienti vyvinout vodnatou a krvavou stolici (s křečemi a horečkou žaludku nebo bez něj), až dva nebo více měsíců po provedení poslední dávky antibiotiky. Pokud k tomu dojde, pacienti by se měli co nejdříve kontaktovat svého lékaře.
Pokyny pro použití pro systém doplňků.
Cleocin fosfát ®
Clindamycin sterilní roztok pro injekci USP
na doplnění ® Vial
Otevření kontejneru ředidla:
Oloupejte z rohu a odstraňte kontejner. Lze pozorovat určitou neprůhlednost plastu v důsledku absorpce vlhkosti během procesu sterilizace. To je normální a neovlivňuje kvalitu nebo bezpečnost řešení. Neprůhlednost se bude postupně snižovat.
Přes pult proti nevolnosti
Sestavení lahvičky a flexibilní ředidlové nádoby:
(Použijte aseptickou techniku)
- Odstraňte ochranné kryty z horní části lahvičky a port lahvičky na kontejneru ředidla následovně:
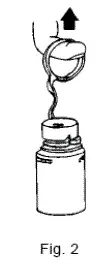
- Chcete -li odstranit odtrhnuté víčko lahvičky, otočte tahový kroužek přes horní část lahvičky a stáhněte dolů dostatečně daleko, abyste spustili otvor (viz obrázek 1.), pak vytáhněte rovně nahoru a odstraňte víčko. (Viz obrázek 2.) POZNÁMKA: Jakmile byla odtržená čepice odstraněna Nepřibližujte lahvičku pomocí injekční stříkačky.
- Chcete -li odstranit kryt portu Vial Port, uchopte kartu na tažném kroužku Vytáhněte se a rozbijte tři řetězce kravaty a poté se odtáhněte a odstraňte kryt. (Viz obrázek 3.)

- Zašroubujte lahvičku do portu lahvičky, dokud nebude nejde dál. Lahvička musí být pevně zašroubována, aby se zajistilo těsnění. K tomu dochází přibližně 1/2 otáček (180 °) po prvním zvukovém kliknutí. (Viz obrázek 4.) Zvuk kliknutí nezajišťuje těsnění; Lahvička musí být otočena tak daleko, jak to půjde. POZNÁMKA: Jakmile je lahvička sezení, nepokoušejte se ji odstranit. (Viz obrázek 4.)
- Znovu zkontrolujte lahvičku, abyste zajistili, že je těsná tím, že se pokusíte ji dále obrátit ve směru sestavení.
- Správně štítek.
 |
 |
Příprava příměsi:
- Jemně stiskněte dno kontejneru ředidla a nafoukněte část nádoby obklopující konec lahvičky s léčivem.
- Na druhou stranu zatlačte lékovou lahvičku dolů do kontejneru a na stěnách kontejneru. Uchopte vnitřní uzávěr lahvičky skrz stěny nádoby. (Viz obrázek 5.)
- Vytáhněte vnitřní čepici z lahvičky s léčivem. (Viz obrázek 6.) Ověřte, že gumová zátka byla vytažena, což umožňuje smíchat léčivo a ředidlo.
- Důkladně smíchejte obsah kontejneru a použijte ve stanoveném čase.
 |
 |
Příprava na správu: (Použijte aseptickou techniku)
- Potvrďte aktivaci a příměs obsahu lahvičky.
- Zkontrolujte úniky pevně stisknutím kontejneru. Pokud jsou nalezeny úniky, může být zhoršena jako sterilita.
- Svaza ovládání úzkého toku sady podávání.
- Odstraňte kryt z výstupního portu na dně kontejneru.
- Vložte propíchnutí kolíku podávání zasazeného do portu s krouceným pohybem, dokud není kolík pevně usazen. Poznámka: Viz Úplné pokyny na administrativní sadě Carton.
- Zvedněte volný konec smyčky věšáku na dně lahvičky, které rozbijí dva řetězce kravat. Ohněte smyčku směrem ven a zamkněte ji ve vzpřímené poloze a poté zavěste kontejner z věšáku.
- Stisknutím a uvolněte kapací komoru a stanovte správnou hladinu tekutin v komoře.
- Otevřená svorka ovládání toku a čirý vzduch ze sady. Close Clamp.
- Připojte nastavení na zařízení venipunktury. Pokud zařízení není přepravováno a vytvořte venipunkturu.
- Regulujte rychlost podávání se svorkou kontroly toku.
VAROVÁNÍ: Do not use flexible container in series connections.


